1.5: Координаційні полімери
- Page ID
- 19895
Полімери - це довголанцюгові молекули, утворені з окремих молекулярних будівельних блоків. Зазвичай будівельними блоками є органічні молекули, що утримуються разом за допомогою ковалентних зв'язків. Які ще види будівельних блоків доступні?
Освіта координаційних сполук є одним з багатьох важливих аспектів неорганічної хімії. У координаційній сполуці донор електронної пари, званий лігандом, ділиться своєю електронною парою з атомом металу. Часто атом металу є перехідним металом, і дуже часто це іон перехідного металу, але є й інші приклади.
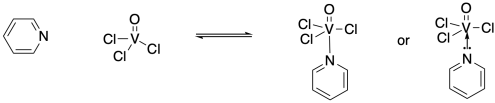
Наприклад, азот в піридиновому кільці має одиноку пару. Піридин може діяти як ліганд, якщо його самотня пара ділиться з металевим центром, таким як ванадій в трихлоро (оксо) ванадію. Самотня пара стає азотно-ванадієвої зв'язком. Іноді цей зв'язок малюють короткою стрілкою від одинокої пари до ванадію, підкреслюючи її походження, але частіше її просто малюють у вигляді лінії, як і будь-який інший зв'язок.
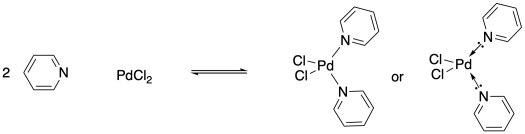
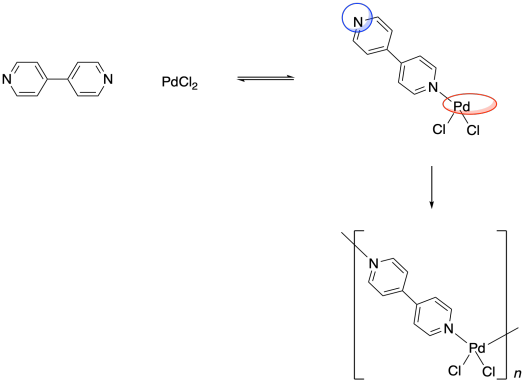
Однією з цікавих речей про атоми металів є їх здатність утворювати змінну кількість зв'язків. Хоча дихлорид паладію може утворювати координаційний комплекс шляхом зв'язування з одним піридиновим лігандом, він також може робити це з двома піридинами. У першому випадку це утворювало б трикоординатний комплекс, але останній випадок призведе до чотирикоординатного з'єднання паладію.
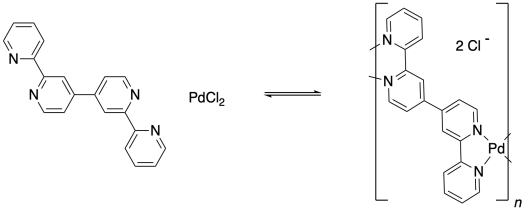
Пам'ятайте, здатність зв'язуватися з двома сусідніми групами, а не лише з однією, є важливою особливістю, яка може дозволити маленькій молекулі опинитися в полімері. Паладій тут є ланкою в ланцюжку, яка має три одиниці довжини. Що робити, якщо ліганд також мав цю здатність зв'язуватися з двома речами? Що робити, якщо замість піридину ліганд був 4,4'-біпіридин?
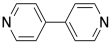
Ця молекула може зв'язувати атом паладію з обох кінців. Після того, як bpy (це абревіатура для біпіридину, вимовляється «біппі»), пов'язаний з атомом паладію, він все одно матиме другу одиничну пару азоту, яку він міг би використовувати для зв'язування іншого. Паладій теж міг би вільно зв'язувати другий хлопець. В результаті ці дві мономерні одиниці здатні утворювати змінну ланцюг.
Чому люди хочуть це зробити? Загальна ідея полягає в тому, щоб використовувати властивості цих атомів металів по-новому. Чим хороші метали? Вони добре проводять електрику, а іноді зберігають корисні магнітні властивості. Якщо ці властивості можна включити в матеріал, який більше схожий на органічні полімери, які, як правило, недорогі і дуже легкі, то, можливо, їх можна використовувати для виготовлення матеріалів, які матимуть всіляке застосування в повсякденному житті. Метали також є дуже хорошими каталізаторами для широкого спектру реакцій. Координаційний полімер служить для космічних атомів металів рівномірно всередині структури, яка має велику площу поверхні, що може сприяти каталітичній ефективності. Усі ці потенційні використання призвели до великих досліджень координаційних полімерів в останні роки (а також пов'язаних з ними «метало-органічних каркасів»).
Чи можуть всі зв'язки вздовж цього ланцюга метал-лігандів дійсно триматися разом, утворюючи полімер? Однією з ключових відмінностей між ковалентними зв'язками, які ви бачили в органічних полімерах, і давальними зв'язками тут є те, що давальні зв'язки є оборотними. Завжди існує рівновага між комплексом метал-ліганд і вільним металом і лігандом. Звичайно, цей зв'язок може бути дуже міцним, і в цьому випадку рівновага лежить до комплексу метал-ліганд. Іншими словами, велика частка матеріалу утворювала б комплекс метал-ліганд. Наскільки велика фракція? Реальна цінність не настільки важлива на даний момент. Для наших цілей, скажімо, ми складаємо метал і ліганд разом і 90% молекул утворюють комплекс. І припустимо, що це також вірно на наступному кроці, приведення іншого ліганда в картинку, щоб зв'язати з металом, і в кроці після цього, приведення іншого металу, щоб зв'язати з іншим кінцем одного з лігандів, і так далі. Отже, припустимо, кожне з цих подій призводить до 90% формування продукту.

Просто дістаючись до цієї чотириодиничної ланцюга спирається на три різні рівноваги. Якщо, як ми говоримо, кожен крок триває близько 90% шляху (що звучить досить добре; ви були б задоволені 90% прибутком на реакцію в лабораторії), то весь триступеневий процес дасть 0,90 х 0,90 х 0,90 = 0,73, або 73% продукту. Непогано. Але корисні полімерні ланцюги можуть бути довжиною тисячі одиниць або більше, і в цьому випадку кількість полімеру, фактично сформованого з належної довжини ланцюга, буде приблизно (0,90) 999 = 1,94 х 10 -46 або 1,94 х 10 -44%, і це смішно невелика кількість.
Зараз реальний розрахунок концентрації рівноваги, звичайно, більш складний, ніж це, але ця швидка вправа підкреслює важливий момент: щоб сформувати стійкий координаційний полімер помітної довжини, метал повинен дуже міцно зв'язувати ліганд. З цієї причини багато підходів до координаційних полімерів використовували багатодентатні ліганди, які, звичайно, зв'язуються більш щільно, ніж монодентатні ліганди. Наприклад, полімер, утворений за допомогою бідентатного зв'язування, показаного нижче, був би набагато стійкішим щодо деполімеризації (тобто знову розпадається на мономери), ніж приклад монодентату, показаний раніше.