9.1: Реакція гідроформулювання
- Page ID
- 20899
Карбонілювання ненасичених субстратів за допомогою каталізу перехідних металів забезпечує потужний інструмент для отримання тонких хімічних проміжних продуктів. Асиметричне карбонілювання є одним з найскладніших однорідних процесів, і їх потенціал ще належить зробити. Найбільш відомими прикладами реакцій асиметричного карбонілювання є каталізоване Rh-каталізоване гідроформулювання алкенів разом з PD-каталізованою гідрокси та алкоксикарбонілуванням алкенів. Важливою відмінністю між цими реакціями є резус-каталізоване гідроформулювання представляє більший промисловий інтерес, ніж процес карбонілювання на основі паладію.
Перетворення алкенів в альдегіди є найбільшим об'ємом гомогенної перехідної метало-каталізованої реакцією. Цей процес був широко досліджений і розроблено ряд методів і каталізаторів для контролю регіоселективності у внутрішніх і кінцевих альдегідах (Схема\(\PageIndex{1}\)).
9.1.1 Реакція вінілових аренів
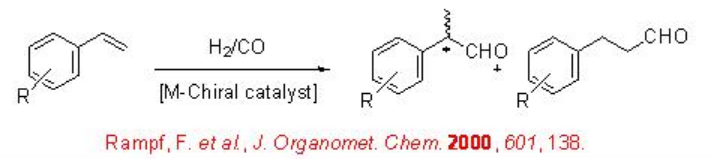
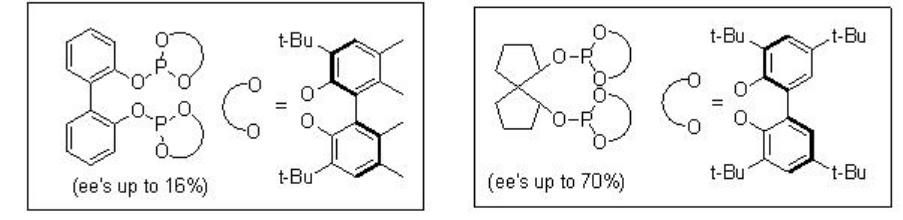
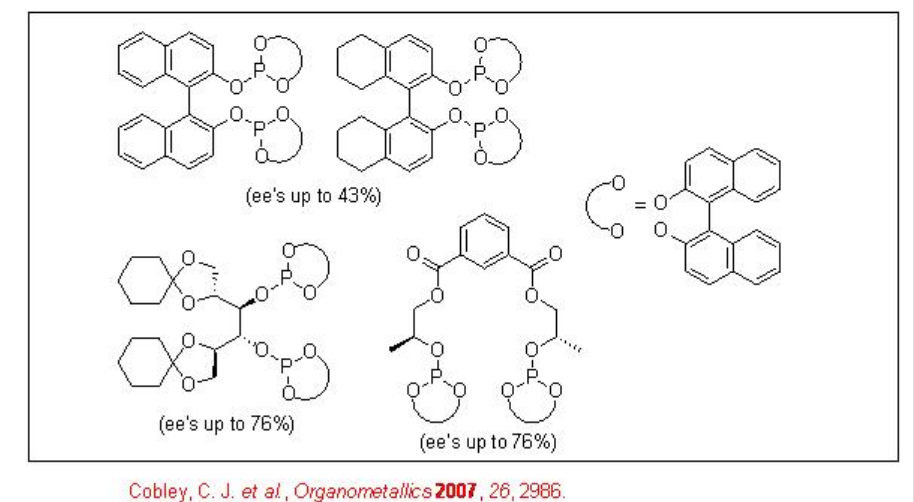
Асиметричне гідроформулювання вінілових аренів є привабливим шляхом дозволити собі оптично активні альдегіди, які є прекурсорами субстрату для синтезу високоцінних фармацевтичних препаратів, агрохімікатів, біорозкладаних полімерів та рідких кристалів (Схема\(\PageIndex{2}\)). З початку 1970 року в якості каталізаторів цього перетворення з помірною енантіоселективністю (нижче 60%) використовуються хіральні резус-дифосфінові комплекси. З початку 1990 року в якості альтернативи цій реакції виникло використання бісфофациклічних лігандів, дифосфітів і фосфін-фосфіту. Схема\(\PageIndex{3}\) узагальнює деякі нові дифосфітові ліганди, розроблені з біарілом, спіро, піранозидом, манітолом та макроциклічними кістками для асиметричного гідроформулювання вінілових аренів з низьким та помірним успіхом (її від 16% до 76%).
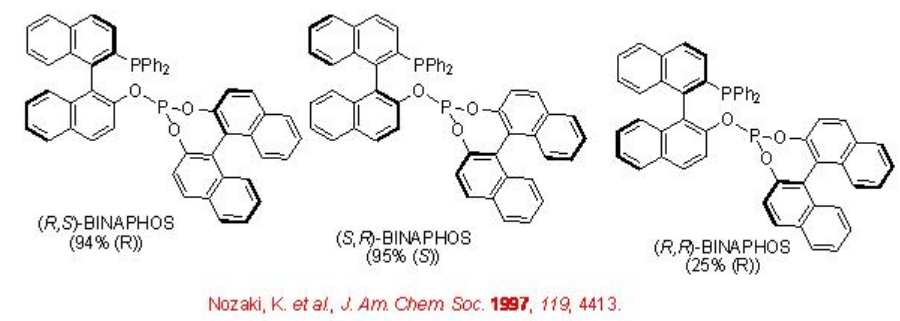
Схема\(\PageIndex{4}\) узагальнює деякі успішні фосфін-фосфітові ліганди для асиметричного гідроформулювання вінілової арени. Енантіоселективність залежить від конфігурації обох фрагментів бінафтілу. Найкраща енантіоселективність спостерігається, коли конфігурації двох бінафтілових фрагментів протилежні.
9.1.2 Реакція вінілацетату
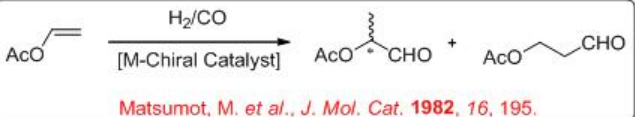
Реакція вінілацетату є більш складною порівняно з реакцією вініларенів. Цей процес дає 2- і 3- ацетоксипропанали з високою селективністю (Схема\(\PageIndex{5}\)). Як побічні продукти виробляють етилацетат і оцтову кислоту.
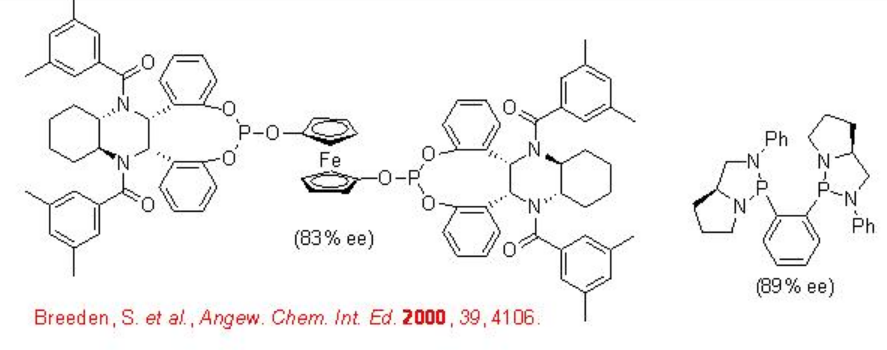
Схема\(\PageIndex{6}\) ілюструє деякі успішні ліганди для каталізованого резус-каталізованого гідроформулювання вінілацетату. У дужках показана енантіоселективність реакцій.
9.1.3 Реакція аллілціаніду
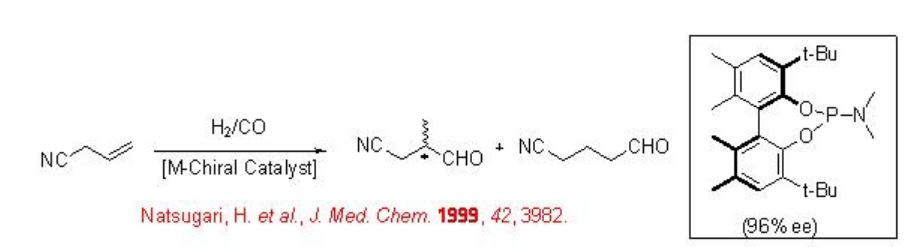
Асиметричне гідроформулювання алілціаніду представляє великий інтерес, оскільки похідне ізо-альдегіду може бути перетворено у 2-метил-4-бутанол, який є проміжним, для асиметричного синтезу тахікініну, нового агоніста рецептора NK1 (Схема\(\PageIndex{7}\)). Реакцію вивчали з використанням дифосфіту, фосфін-фосфіту, біс-фосфациклічних та фосфорамідитних лігандів з дотриманням до 96% е.
9.1.4 Реакція гетероциклічних алкенів
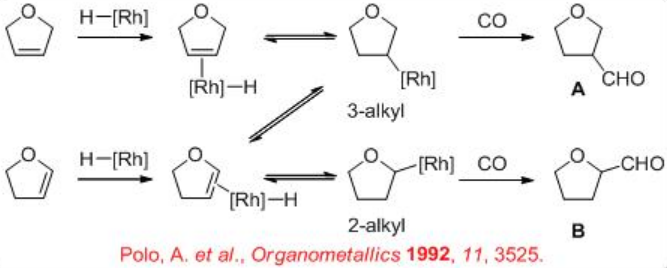
Мало досліджень зосереджені на гідроформулюванні гетероциклічних алкенів. Для цих субстратів особливий інтерес представляє регіоселективність, оскільки вона відрізняється від ациклічних алкенів. Наприклад, гідроформулювання 2,5-дигідрофурану може призвести до утворення як тетрагідрофуран-3-карбальдегіду А (очікуваний продукт), так і тетрагідрофуран-2-карбальдегіду В (може утворитися за допомогою процесу ізомеризації). Регіоселективність контролюється модифікацією лігандів та умов реакції.
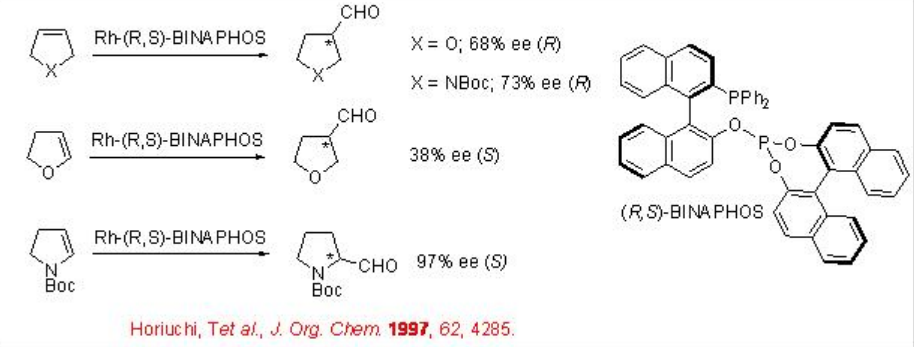
Схема\(\PageIndex{9}\) узагальнює реакцію 2,5-дидирофурану, похідного 3-піроліну та похідного 4,7-дидидиро-1,3-діоксепіну з використанням хірального резус-комплексу підшипника R, S-BINAPHOS. Оптично активні альдегіди отримані у вигляді одиничних продуктів з енантіоселективністю між 64-97%. При 2,5-дигідрофурані спостерігається до 64% регіоселективність для утворення тетрагідрофуран-3-карбальдегіду А, тоді як реакція 2,3-дигідрофурану призвела до утворення суміші А і В (1:1) з її 38% в А.
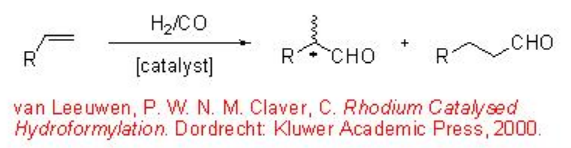
9.1.5 Реакція велосипедних водоростей
Асиметричному гідроформулюванню біциклічних алкенів приділялося мало уваги. Ця реакція цікава наступними особливостями: (i) реакція може призвести до утворення трьох хіральних центрів при утворенні одного C-C-зв'язку; (ii) немає проблеми регіоселективності; (iii) функціональні групи, розташовані навпроти подвійного зв'язку вуглець-вуглець, можуть бути універсальними. Схема\(\PageIndex{10}\) узагальнює деякі приклади асиметричного гідроформулювання біциклічних алкенів з використанням резус-тангфосу.