6.8: Роздільна здатність (поділ) енантіомерів
- Page ID
- 23633
Мета навчання
- пояснити, як вирішити (відокремити) пару енантіомерів
Вступ та огляд
Рацемічна суміш являє собою суміш 50:50 двох енантіомерів. Оскільки вони є дзеркальними відображеннями, кожен енантіомер обертає плоскополяризоване світло в рівному, але протилежному напрямку і оптично неактивний. Якщо енантіомери відокремлені, то суміш, як кажуть, була дозволена. Загальний експеримент в лабораторному компоненті вступної органічної хімії передбачає дозвіл рацемічної суміші.
Драматичні біохімічні наслідки хіральності ілюструються застосуванням у 1950-х роках препарату Талідомід, седативного засобу, який призначається вагітним жінкам для полегшення ранкової нудоти. Пізніше було зрозуміло, що, хоча (+) -форма молекули, була безпечним та ефективним седативним засобом, (−) -форма була активним тератогеном. Препарат викликав численні аномалії народження при прийомі на ранніх стадіях вагітності, оскільки він містив суміш двох форм.
Хіральна резолюція
Як зазначалося раніше, хіральні сполуки, синтезовані з ахіральних вихідних матеріалів і реагентів, як правило, рацемічні (тобто суміш енантіомерів 50:50). Поділ рацематів на їх складові енантіомери - це процес, який називається роздільною здатністю. Оскільки енантіомери мають ідентичні фізичні властивості, такі як розчинність і температура плавлення, роздільна здатність вкрай важка. Діастереомери, з іншого боку, мають різні фізичні властивості, і цей факт використовується для досягнення роздільної здатності рацематів. Реакція рацемата з енантіомерно чистим хіральним реагентом дає суміш діастереомерів, які можна розділяти. Наприклад, якщо рацемічна суміш хірального спирту вступає в реакцію з енантіомерно чистою карбоновою кислотою, в результаті виходить суміш діастереомерів: в цьому випадку, оскільки був використаний чистий (R) ентантіомер кислоти, продукт являє собою суміш (R-R) і (R-S) діастереомерних ефірів, які можуть, теоретично, бути розділені своїми різними фізичними властивостями. Подальший гідроліз кожного відокремленого ефіру дасть «дозволені» (енантіомерно чисті) спирти. Використовувані в цій техніці відомі як «естери Мошера», після Гаррі Стоуна Мошера, хіміка, який став піонером методу в Стенфордському університеті.
Як зазначалося раніше, хіральні сполуки, синтезовані з ахіральних вихідних матеріалів і реагентів, як правило, рацемічні (тобто суміш енантіомерів 50:50). Поділ рацематів на їх складові енантіомери - це процес, який називається роздільною здатністю. Оскільки енантіомери мають ідентичні фізичні властивості, такі як розчинність і температура плавлення, роздільна здатність вкрай важка. Діастереомери, з іншого боку, мають різні фізичні властивості, і цей факт використовується для досягнення роздільної здатності рацематів. Реакція рацемата з енантіомерно чистим хіральним реагентом дає суміш діастереомерів, які можна розділяти. Реверсування першої реакції потім призводить до відокремлених енантіомерів плюс відновлений реагент.
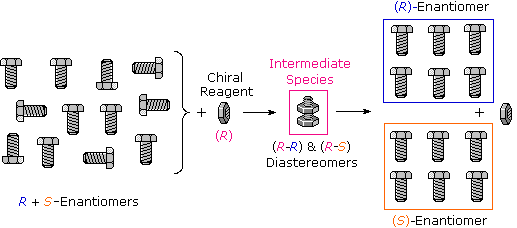
Багато видів хімічних та фізичних реакцій, включаючи утворення солі, можуть бути використані для досягнення діастереомерних проміжних продуктів, необхідних для поділу. Малюнок 5.8.1 ілюструє цей загальний принцип, показуючи, як гайка, що має правосторонню різьбу (R), може служити «реагентом» для розрізнення та відокремлення суміші правих і ліворуких болтів однакового розміру та ваги. Тільки два правші партнери можуть взаємодіяти, щоб дати повний проміжний проміжний, тому поділ досить простий. Розсмоктуючий фрагмент, тобто гайку, потім знімають, залишаючи болти розділеними на їх праву і лівосторонню форми. Хімічні реакції енантіомерів в нормі не так різко відрізняються, але практичне розмежування все ж можливо.
Оскільки фізичні властивості енантіомерів ідентичні, їх рідко можна розділити простими фізичними методами, такими як фракційна кристалізація або дистиляція. Тільки під впливом іншого хірального речовини енантіомери поводяться по-різному, і практично всі методи дозволу енантіомерів засновані на цьому факті. Ми включаємо сюди обговорення основних методів вирішення
Хіральні аміни як розчинники та роздільна здатність рацемічних кислот
Найбільш часто використовувана процедура поділу енантіомерів полягає в перетворенні їх в суміш діастереомерів, які матимуть різні фізичні властивості: температуру плавлення, температуру кипіння, розчинність і так далі (розділ 5-5). Наприклад, якщо у вас є рацемічна або D, L суміш енантіомерів кислоти і перетворити це на сіль з хіральною основою, що має конфігурацію D, сіль буде сумішшю двох діастереомерів, (D кислота. D основа) і (Л кислота. D база). Ці діастереомерні солі не ідентичні і вони не є дзеркальними відображеннями. Тому вони будуть в деякій мірі відрізнятися своїми фізичними властивостями, і може бути можливим поділ фізичними методами, такими як кристалізація. Якщо діастереомерні солі можуть бути повністю відокремлені, кислота, регенерується з кожної солі, буде або виключно D, або L-енантіомером:
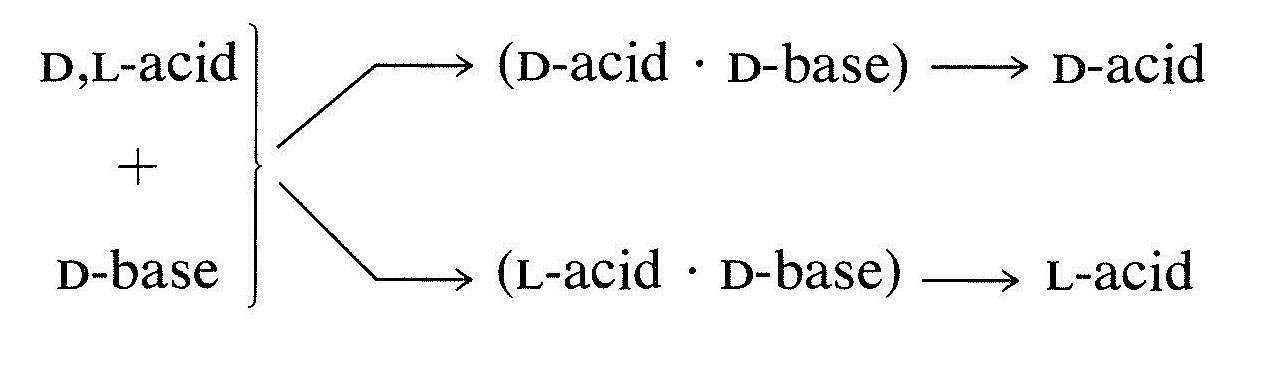
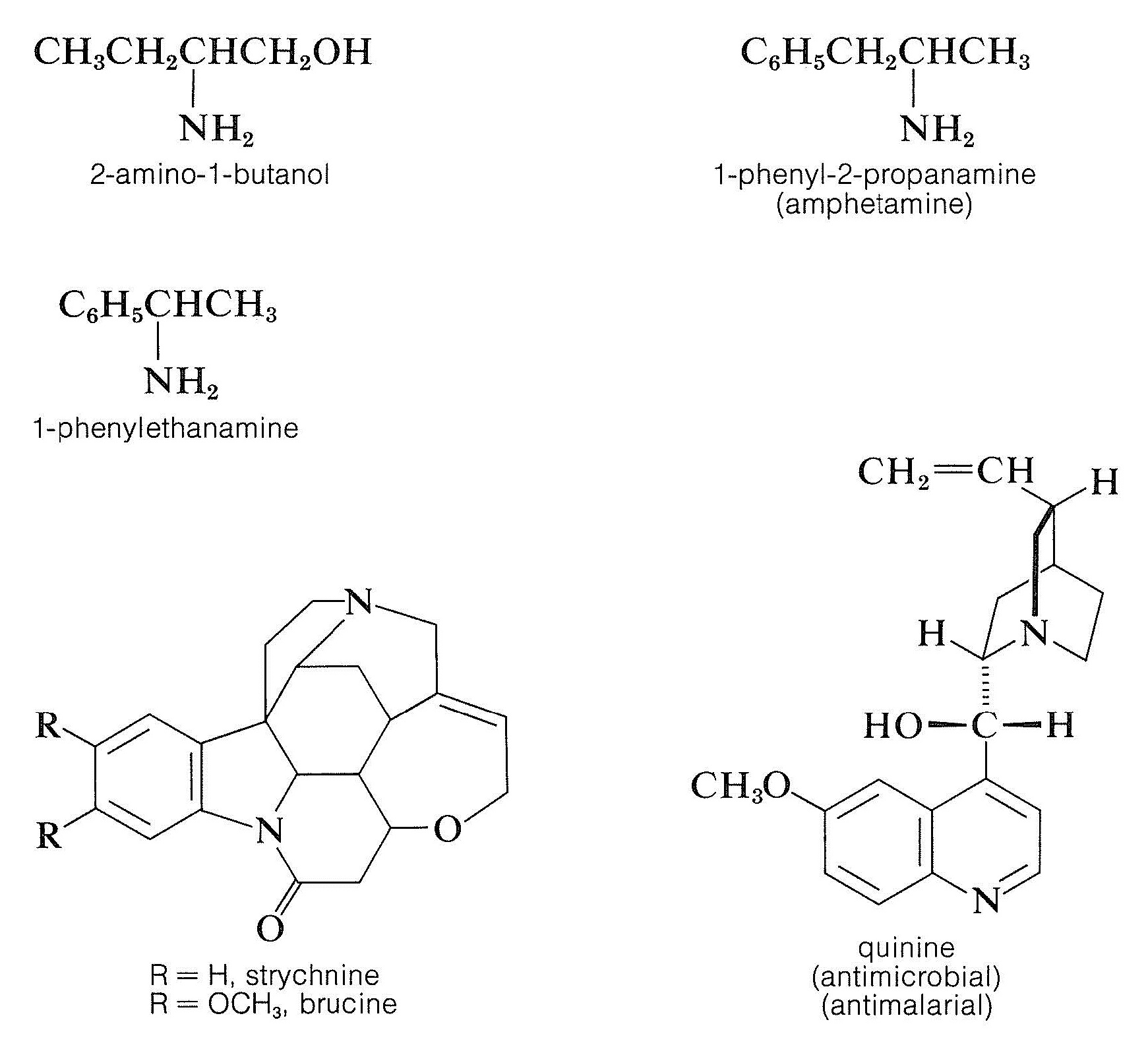
Дозвіл хіральних кислот за рахунок утворення діастереомерних солей вимагає адекватних запасів відповідних хіральних підстав. Бруцин, стрихнін та хінін часто використовуються для цієї мети, оскільки вони легко доступні, природно зустрічаються хіральні основи. Також можна використовувати більш прості аміни синтетичного походження, такі як 2-аміно- 1 -бутанол, амфетамін і 1 -фенілетанамін, але спочатку вони повинні бути вирішені самі.
Дозвіл рацемічних основ
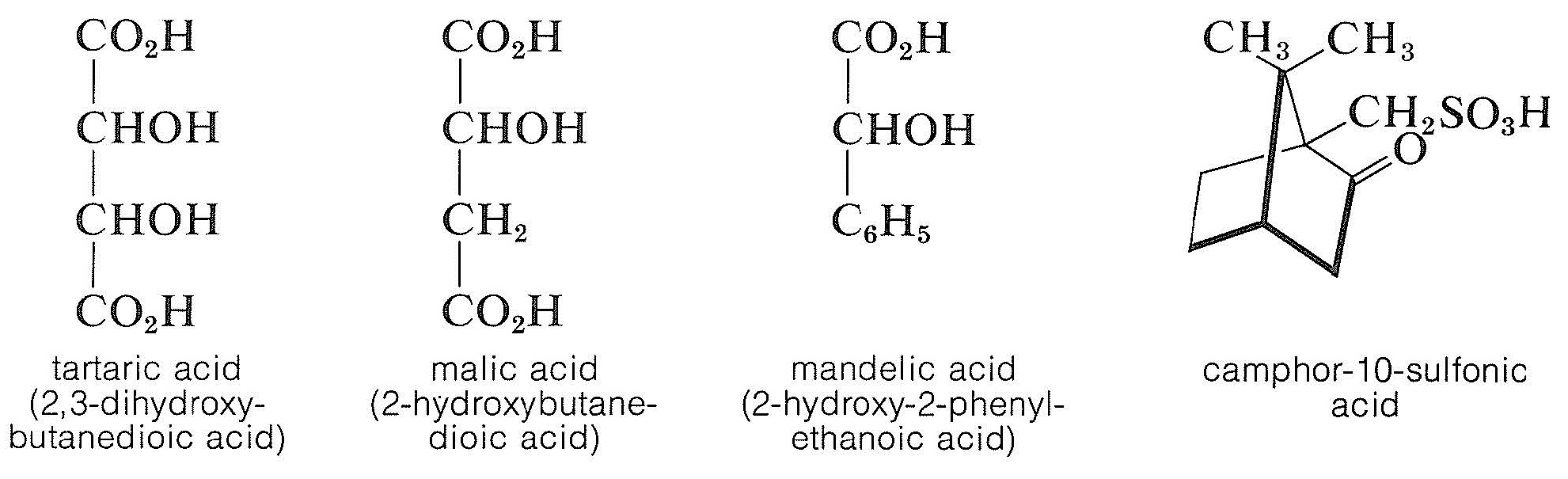
Для дозволу рацемічної основи використовують хіральні кислоти, такі як (+) -винна кислота, (-) -яблучна кислота, (-) -мигдальна кислота, і (+) -камфора- 10-сульфонова кислота.
Принцип такий же, як і для дозволу рацеміновой кислоти з хіральною основою, причому вибір кислоти буде залежати як від легкості відділення діастереомерних солей, так і, звичайно ж, від доступності кислоти для шкали задіяного дозволу. Методи дозволу такого роду можуть бути стомлюючими, оскільки численні перекристалізації в різних розчинниках можуть знадобитися для поступового збагачення кристалів у менш розчинному діастереомері. Щоб визначити, коли роздільна здатність завершена, суміш діастереомерів перекристалізується до подальшої зміни вимірюваного оптичного обертання кристалів. На цьому етапі можна сподіватися, що кристалічна сіль є чистим діастереомером, з якого можна відновити один чистий енантіомер. Оптичне обертання цього
енантіомера буде максимальним значенням, якщо воно «оптично» чисте, оскільки будь-яка кількість іншого енантіомера може лише зменшити величину вимірюваного обертання\(\alpha\).
Роздільна здатність рацемічних спиртів
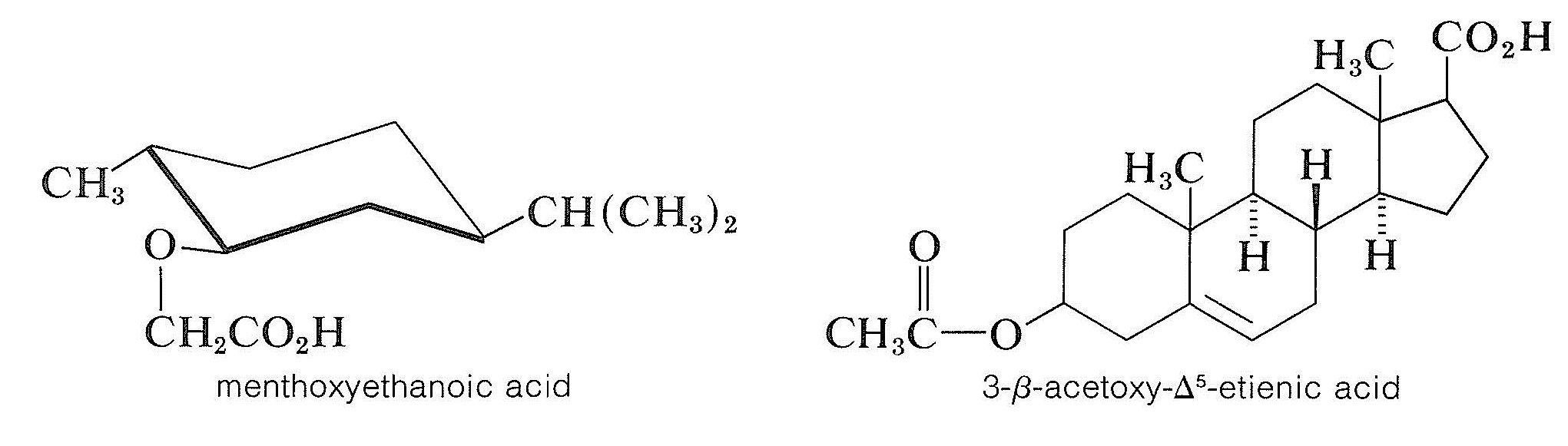
Для розчинення рацемічного спирту можна використовувати хіральну кислоту для перетворення спирту в суміш діастереомерних ефірів. Це не так взагалі корисно, як можна подумати, оскільки ефіри, як правило, є рідинами, якщо вони не є дуже високомолекулярними сполуками. Якщо діастереомерні ефіри не є кристалічними, вони повинні бути розділені іншим способом, ніж фракційна кристалізація (наприклад, методами хроматографії, розділ 9-2). Дві хіральні кислоти, які є корисними розчинниками для спиртів, є:
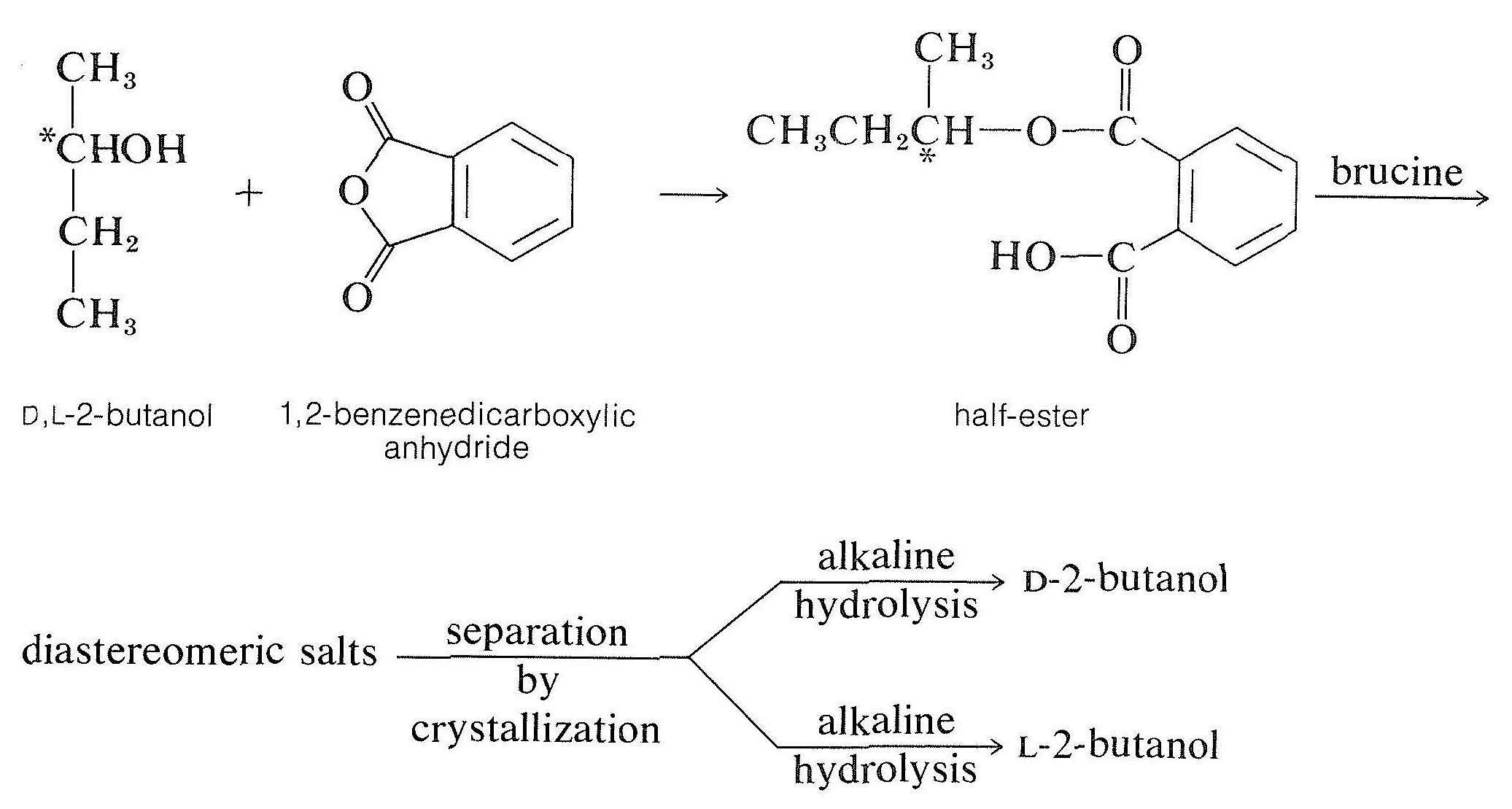
Найпоширенішим методом розчинення спирту є перетворення його в напівефір дикарбонової кислоти, наприклад бутандіової (бурштинової) або 1,2-бензолдикарбонової (фталевої) кислоти, з відповідним ангідридом. Отриманий напівефір має вільну карбоксильну функцію і потім може бути розчинний з хіральною основою, як правило, бруцином:
Інші способи вирішення
Однією з головних цілей в області органічної хімії є розробка реагентів з властивістю «хірального розпізнавання» таким чином, що вони можуть впливати на чисте поділ енантіомерів за одну операцію, не руйнуючи жодного з енантіомерів. Ми ще не досягли цього ідеалу, але це може бути не далеко в майбутньому. Хроматографічні методи (Розділ 9-2), за допомогою яких стаціонарна фаза є хіральним реагентом, який адсорбує один енантіомер сильніше, ніж інший, були використані для розчинення рацемічних сполук, але такі дозволи рідко призвели до того, що обидва чисті енантіомери в препаративному масштабі. Інші методи, звані кінетичними дозволами, відмінні, коли вони застосовні. Процедура використовує відмінності в швидкості реакції енантіомерів з хіральними реагентами. Один енантіомер може реагувати швидше, тим самим залишаючи надлишок іншого енантіомеру позаду. Наприклад, рацемічна винна кислота
може бути вирішена за допомогою певних пеніцилінових форм, які споживають декстроротаторний енантіомер швидше, ніж леворотаторний енантіомер. В результаті з суміші можна витягти майже чисту (-) винну кислоту:
(±) -винна кислота+цвіль\(\rightarrow\) (-) -винна кислота+більше цвілі
Недоліком дозволів цього типу є те, що більш реактивний енантіомер зазвичай не підлягає відновленню з реакційної суміші.
Процедура кристалізації, яку застосовував Пастер для його класичної роздільної здатності (±) -винної кислоти (Розділ 5-1C), була успішною лише в дуже небагатьох випадках. Ця процедура залежить від утворення окремих кристалів кожного енантіомера. Таким чином, якщо кристалізація тартрату натрію амонію здійснюється нижче 27", звичайна сіль рацемата не утворюється; замість них утворюється суміш кристалів (+) і (-) солей. Два різних види кристалів, які пов'язані як об'єкт з його дзеркальним відображенням, можуть бути розділені вручну за допомогою мікроскопа і згодом можуть бути перетворені в енантіомери винної кислоти сильною кислотою. Варіацією цього способу дозволу є посів насиченого розчину рацемічної суміші кристалами одного чистого енантіомера в надії викликати кристалізацію якраз того одного енантіомера, тим самим залишивши інший в розчині. На жаль, таким чином було досягнуто дуже
мало практичних рішень.
Навіть при досягненні успішного вирішення залишаються деякі суттєві проблеми. Наприклад, сама роздільна здатність не надає інформації про фактичну конфігурацію (+) або (-) енантіомера. Це необхідно визначити іншими способами (див. Розділ 19-5). Також неможливо сказати енантіомерную чистоту (оптичну чистоту) дозволених енантіомерів без додаткової інформації. Цей момент розглядається далі в наступному розділі.