5.11: Реактивність та вибірковість
- Page ID
- 23415
Порівняння реактивності
Враховуючи знання про те, що певна реакція буде протікати з відповідною швидкістю, для задовільної роботи необхідний ряд практичних міркувань. Ці міркування включають втручання можливими побічними реакціями, які дають продукти, відмінні від бажаних, легкість відділення потрібного продукту від реакційної суміші, а також витрати на матеріали, апарати та працю. Ці проблеми ми розглянемо у зв'язку з важливими синтетичними реакціями, розглянутими в цій книзі.
Хлорування насичених вуглеводнів може бути індуковано світлом, але також може здійснюватися при температурах приблизно\(300^\text{o}\) в темряві. За таких обставин механізм подібний до механізму світлоіндукованого хлорування, за винятком того, що атоми хлору утворюються шляхом термічної дисоціації молекул хлору. Тверді вуглецеві поверхні каталізують термічне хлорування, можливо, сприяючи розщепленню молекул хлору.
Пряме моногалогенування насичених вуглеводнів працює задовільно тільки з хлором і бромом. Для загальної реакції

розрахункове\(\Delta H^\text{0}\) значення негативне і дуже велике для фтору, негативне і помірне для хлору і брому і позитивне для йоду (див. Таблицю 4-7). З фтором реакція виділяє стільки тепла, що її може бути важко контролювати, і можуть бути отримані продукти від розщеплення вуглецево-вуглецевих зв'язків, а також вуглецево-водневих зв'язків. Єдина успішна процедура прямого фторування вуглеводнів включає дифузію дрібних кількостей фтору, змішаного з гелієм, в рідкі або тверді вуглеводні при низьких температурах, як правило,\(-78^\text{o}\) (температура сухого льоду). У міру протікання фторування концентрація фтору може бути збільшена. Процес найкраще підходить для отримання повністю фторованих сполук, і вдалося отримати таким способом кількості і\(\left( CF_3 \right)_3 C-C \left( CF_3 \right)_3\) з 2,2-диметилпропану\(\left( CF_3 \right)_4C\) і 2,2,3,3-тетраметилбутану, що відповідають\(10\) -\(15\%\) врожайності на основі використовуваного фтору.
Бром, як правило, набагато менш реагує на вуглеводні, ніж хлор, як при високих температурах, так і при активації світлом. Тим не менш, зазвичай можна успішно броміровать насичені вуглеводні. Йод нереактивний.
| Галоген (X) | \(\Delta H^o\)(ккал/моль) |
|---|---|
| F | \ (\ Дельта H^o\) (ккал/моль) a">-116 |
| Cl | \ (\ Дельта H^o\) (ккал/моль) a">-27 |
| Br | \ (\ Дельта H^o\) (ккал/моль) a">-10 |
| Я | \ (\ Дельта H^o\) (ккал/моль) a">13 |
| a Розрахований з енергій зв'язку таблиці 4-3. | \ (\ Дельта H^o\) (ккал/моль) a"> |
Хлорування метану не повинно припинятися з утворенням хлорметану (метилхлориду). Зазвичай при хлоруванні метану отримують деякі з вищих продуктів хлорування: дихлорметан (метиленхлорид), трихлорметан (хлороформ) та тетрахлорметан (тетрахлорметан):
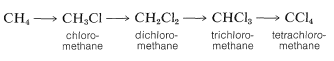
На практиці можна в значній мірі контролювати ступінь заміщення, контролюючи співвідношення метан-хлор. Наприклад, для переважання монохлорування необхідно високе співвідношення метан-хлор таке, щоб атоми хлору вступали в реакцію з,\(CH_4\) а не з\(CH_3Cl\).
Селективність в алканової галогенації
Для пропану та вищих вуглеводнів, для яких, як правило, можливо більше одного продукту монозаміщення, складні проблеми розділення виникають, коли потрібний конкретний продукт. Наприклад, хлорування\(3\) 2-метилбутану при\(300^\text{o}\) дає всі чотири можливих продукту монозаміщення. На чисто статистичній основі можна очікувати співвідношення продуктів з 2-метилбутану корелювати з кількістю наявних воднів при різних позиціях заміщення в співвідношенні 6:1:2:3 (\(50\%\):\(8\%\):\(17\%\):\(25\%\):). Однак, як видно з сильних сторін зв'язків між воднем та первинними, вторинними та третинними вуглецями, не однакові, і ми очікуємо, що слабкі\(C-H\) зв'язки переважно реагуватимуть з\(Cl \cdot\). Таким чином, частка третинного галогеніду приблизно в три рази більше, ніж очікується на статистичній основі, що відповідає нашим очікуванням, що третинний\(C-H\) зв'язок 2-метилбутану повинна бути найслабшою з\(C-H\) зв'язків.

Атоми брому набагато селективніші, ніж атоми хлору. Це не несподівано, оскільки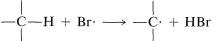 є ендотермічним, тоді як відповідні реакції з атомами хлору зазвичай екзотермічні (дані з таблиці 4-6). Бром видаляє тільки ті водні, які відносно слабо пов'язані з атомом вуглецю. Як і передбачалося, напад 2-метилбутану призводить здебільшого до 2-бром-2-метилбутану, деякого вторинного броміду і, по суті, немає первинних бромідів:\(Br \cdot\)
є ендотермічним, тоді як відповідні реакції з атомами хлору зазвичай екзотермічні (дані з таблиці 4-6). Бром видаляє тільки ті водні, які відносно слабо пов'язані з атомом вуглецю. Як і передбачалося, напад 2-метилбутану призводить здебільшого до 2-бром-2-метилбутану, деякого вторинного броміду і, по суті, немає первинних бромідів:\(Br \cdot\)
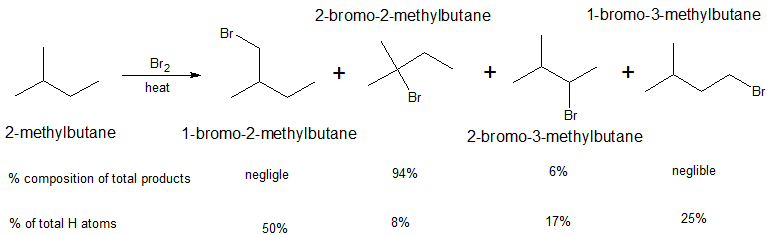
Коли структура алкана симетрична, то для ефективності можна використовувати швидку реакційну здатність хлорування. Коли структура алкану може виробляти цілий ряд моногалогенізованих продуктів, то селективність бромування може бути використана для отримання найбільш стабільного продукту в найбільшому відсотку.
Вправи
1. Вкажіть оптимальні умови галогенування (Cl 2 /тепло або Br 2 /тепло) для отримання зазначеного основного продукту.
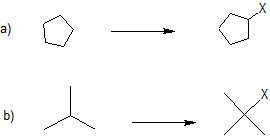
Рішення
1.
