10.3: Нуклеофільне та електрофільне додавання та абстракція
- Page ID
- 17675
Цілі навчання
У цій лекції ви дізнаєтеся наступне
- Активація ліганду металом, що призводить до прямої зовнішньої атаки на ліганд.
- Нуклеофільні реакції приєднання та нуклеофільної абстракції.
- Електрофільні реакції приєднання та електрофільні абстракції.
Нуклеофільні та електрофільні реакції заміщення та абстракції можна розглядати як способи активації субстратів, що дозволяють зовнішньому реагенту безпосередньо атакувати активований металом ліганд, не вимагаючи попереднього зв'язування зовнішнього реагенту з металом. Атакуючим реагентом може бути нуклеофіл або електрофіл. Нуклеофільна атака зовнішнього реагенту сприятлива, якщо фрагмент L n M є поганою π−основою та хорошою π−кислотою i. е., коли комплекс є катіонним та/або коли інші пов'язані з металом ліганди відводять електрон таким чином, що ліганд, що активується, виснажується електронної щільності і може зазнати зовнішньої атаки нуклеофіла Nu −, як LiMe або OH −. Атака нуклеофілів може призвести до утворення зв'язку між нуклеофілами та активованим ненасиченим субстратом, в цьому випадку він називається нуклеофільним додаванням, або може призвести до абстрагування частини або цілого активованого ліганду, і в цьому випадку він називається нуклеофільним абстракція. Нижче розглядаються нуклеофільні приєднання та реакції абстракції.
Нуклеофільна добавка
Приклад реакції нуклеофільного приєднання показаний нижче.
Оксид вуглецю (СО) як ліганд може піддаватися нуклеофільній атаці при з'єднанні з металевим центром поганої π−основності, оскільки вуглецевий центр ліганду СО є дефіцитним електроном через донорство ліганду до металу σ−донорство не повністю компенсується металом до ліганду π−назад донорство. Таким чином, активований СО ліганд піддається нуклеофільній атаці літієвим реагентом, щоб дати аніонний ациловий ліганд, який при алкілуванні генерує знаменитий комплекс Карбена Фішера.

Нуклеофільна абстракція
Приклад реакції нуклеофільної абстракції показаний нижче.
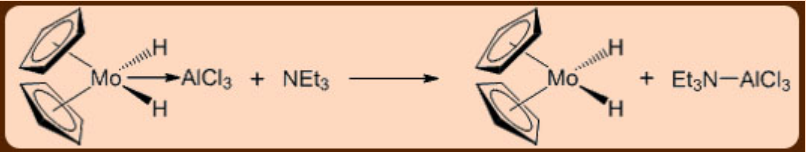
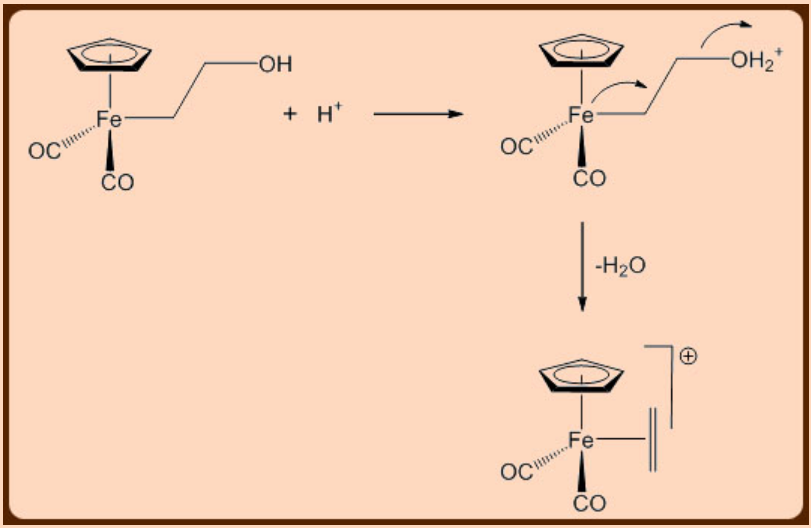
електрофільна добавка
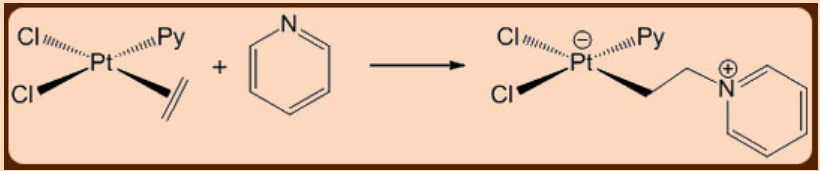
Подібно до реакцій нуклеофільного приєднання та абстрагування, електрофільні аналоги цих реакцій також існують. Електрофільна атака сприятлива, якщо фрагмент L n M є хорошою π−основою та поганою σ−кислотою, тобто коли комплекс є аніонним з центром металу в низькому ступені окислення та/або коли інші пов'язані з металом ліганди пожертвують електронами таким чином, що ліганд активується стає електрон багатий від π−зворотного пожертвування металевого центру і, таким чином, може зазнати зовнішньої атаки електрофілом E +, як H + і CH 3 I. Атака електрофілів може призвести до утворення зв'язку між електрофілом і активованим ненасиченим субстрат, в цьому випадку він називається електрофільним доповненням, або може призвести до абстрагування частини або цілого активованого ліганда, в цьому випадку його називають електрофільної абстракцією.
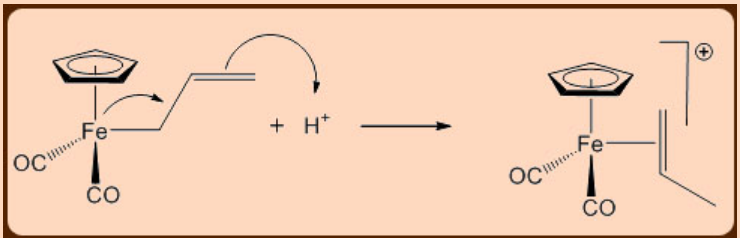
Електрофільна абстракція
Приклад електрофільної реакції абстракції показаний нижче.
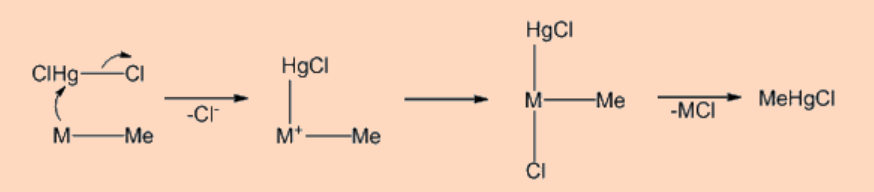
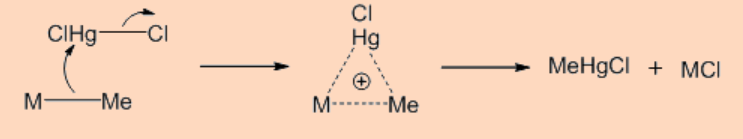
Алкільні абстракції часто досягаються Hg 2+, що може протікати двома способами: (i) атакою α−вуглецю алкільного зв'язку металу, що призводить до інверсії конфігурації у алкільного вуглецю та (ii) нападом на металевий центр, що призводить до збереження конфігурації на алкілвуглець. Інверсія конфігурації протікає наступним шляхом.
Збереження конфігурації протікає наступним шляхом.