8.11.2.1: Озон
- Page ID
- 33463
Озон - аллотропна форма кисню. Його молекулярна формула - O 3, а молярна маса - 48 г моль -1.
виникнення озону
Шенбейн (1840) дійшов висновку, що спостереження Ван Марума в 1785 році своєрідного запаху, коли електричний розряд пропускався через кисень (або повітря), насправді був новим газом. Він назвав його Озон, що походить від грецького слова ozoaterr, що означає запах. Сорету в 1860 році присвоєно молекулярну формулу O 3. Виникнення озону відбувається в невеликих кількостях, у верхньому шарі атмосфери, де він утворюється внаслідок дії ультрафіолетових променів на кисень повітря. Він також присутній в морській воді, де утворюється внаслідок реакції фтору з водою.
У структурі озону довжина зв'язку 127,8 пм є проміжною між єдиним зв'язком (довжина зв'язку 148 пм) і подвійним зв'язком (довжина зв'язку 110 пм). Тому озон вважається резонансним гібридом наступних канонічних форм:

Використання озону
- Для очищення повітря в місцях скупчення людей, таких як кінотеатри та тунельні залізниці. Завдяки своїй сильній окислювальній здатності він також знищує неприємний запах у бійнях.
- При стерилізації питної води шляхом окислення всіх мікробів і бактерій.
- Для консервації м'яса в холодному зберіганні.
- Для відбілювання делікатних тканин, таких як шовк, слонова кістка, масла, крохмаль і віск.
- Це допомагає знайти подвійний зв'язок у будь-якій ненасиченій органічній сполуці шляхом озонолізу.
приготування озону
Коли безшумний електричний розряд пропускається через сухий кисень, утворюється озон. Кисень ніколи не перетворюється в озон повністю, і ми завжди отримуємо суміш кисню та озону. Цю суміш називають озонованим киснем.
\[ \ce{3O_2 ->[\text{electric}][\text{discharge}] 2O_3} \;\;\; \Delta{H} = +284.5\;kJ/mol\]
Реакція ініціюється безблискучим або безшумним електричним розрядом, щоб виробляти менше тепла, оскільки озон схильний до розкладання назад на кисень із збільшенням температури (Принцип Ле Шательє). Отже, озон готується в спеціально розробленому апараті, званому озонатором для полегшення вищезазначених умов. «Озонілер» - це апарат, який використовується для приготування озону шляхом проходження безшумного електричного розряду. Зазвичай використовуються два типи озонаторів: Siemen's та Brodie Озонатори.
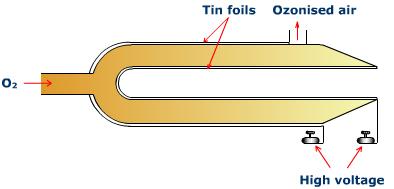
Озонатор Сімена
Він складається з двох співвісних скляних трубок, сплавлених між собою. Олов'яна фольга використовується для покриття внутрішньої сторони внутрішньої трубки та зовнішньої сторони зовнішньої трубки. Внутрішнє і зовнішнє олов'яні покриття з'єднані з висновками індукційної котушки, яка виробляє струм високої напруги. Через кільцевий простір пропускається повільний струм чистого і сухого кисню. При підданні кисню безшумного електричного розряду утворюється озонований кисень, що містить 10-15% озону. Вживаючи наступні запобіжні заходи, вихід озону може бути збільшений в озонованому кисні:
- Слід використовувати тільки чистий і сухий кисень.
- Озонатор повинен бути ідеально сухим.
- Слід підтримувати досить низьку температуру (близько 0° C).
- Не повинно бути іскріння.
Озонатор Броді
В принципі, цей озонатор схожий на озонатор Siemen, але розведена сірчана кислота замінює олов'яну фольгу. Два вуглецевих електрода занурюються в кислоту і з'єднуються з індукційною котушкою. Через простір між трубками пропускається струм сухого кисню. Озонований кисень, що містить близько 5%,\(O_3\) виходить на іншому кінці. Якщо апарат тримати в прохолодному стані, частка озону може піднятися на 20-25%.

Проблеми
- Як утворюється озон у верхніх слоях атмосфери?
Рішення
- Озон утворюється у верхній атмосфері в два етапи:
i) Фотодисоціація кисню ультрафіолетовими випромінюваннями довжиною хвилі менше 240 нм.
\[ \ce{O_2 ->[h\nu] O^{\boldsymbol{\cdot}} + O^{\boldsymbol{\cdot}} }\]
Атоми кисню дійсно є дірадикалами з двома непарними p-орбітальними електронами, але тут представлені одним електроном.
ii) Поєднання високоактивних атомів кисню з молекулами кисню.
\[ \ce{O_2 + O^{\boldsymbol{\cdot}} \rightarrow O_3 }\]
12. Який принцип приготування озону?