8.7.4.2: Кремній та група 14 Елементи
- Page ID
- 33572
Цілі навчання
- Передбачити деякі хімічні реакції для набору умов.
- Охарактеризуйте деякі хімічні та фізичні властивості\(\ce{C}\) і\(\ce{Si}\).
Група 14 Елементи C, Si, Ge, Sn, Pb
Елементи групи 14 відіграють більш важливу роль у нашому житті та нашій цивілізації, ніж елементи будь-якої іншої групи. Таким чином, кожна освічена людина повинна щось знати про них.
- Вуглець - елемент органічної хімії і життя.
- Кремній - елемент інформаційних технологій.
- Германій - елемент транзисторної бази.
- Олово і свинець - елементи, відомі алхімікам.
хімія вуглецю
Вуглець існує як алмаз, графіт, фулерени та деревне вугілля. Їх структури цікаві; так само і їх властивості. Ви, напевно, багато знаєте про алмаз і графіт, але фулерени були виявлені після 1970 року, і це відкриття відкрило двері для безлічі цікавих досліджень. Читайте про них в книгах, журналах і журналах. Ви можете знайти себе працювати з ними коли-небудь.
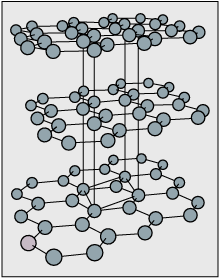
Серед фулеренів одна з найпоширеніших «молекул» має 60\(\ce C\) атомів, і представлена\(\ce{C60}\); діаграма показана тут. Якщо з'єднати 60 атомів вуглецю зв'язками, то структура виглядає як клітина з 5- і 6-членними кільцями. Синтез, склеювання, симетрія і стійкість кліткоподібних фулеренів вже привернули велику увагу, а їх властивості ще більш захоплюючі.

Щодо вуглецевих сполук, ви вже знаєте щось про\(\ce{CO2}\) та\(\ce{CO}\) включаючи їх роль у навколишньому середовищі. Тверді карбіди, такі як\(\ce{Fe3C}\)\(\ce{WC}\), і\(\ce{TiC}\) більш цікаві матеріалознавцям та інженерам для їх застосування в ріжучих інструментах. Карбід кальцію,\(\ce{CaC2}\) отриманий\(\ce{CaO}\) шляхом відновлення вуглецем, був цінним товаром свого часу завдяки його реакції з водою для отримання ацетиленового газу:
\(\ce{CaC_2 + 2 H_2O \rightarrow Ca(OH)_2 + C_2H_{2\large{(g)}}}\)
Ацетилен є важливим промисловим газом, для виготовлення полімерів.
Кремній
Чи знаєте ви, що:
- \(\ce{Si}\)складає 27,7% земної кори?
- силікати,\(\ce{SiO2}\) на основі мінералів, є всюди?
- \(\ce{Si}\)є важливим елементом для росту кісток?
- \(\ce{Si}\)кристали - це основи комп'ютерних чіпів?
- структура така ж, як у алмаза, і ця особливість важлива для комп'ютерних чіпів?\(\ce{Si}\)
- Як ми\(\ce{SiO2}\) перетворюємо в\(\ce{Si}\) елемент?
Силікати
За вагою кремній є найпоширенішим елементом в земній корі. Він зазвичай існує у вигляді оксиду,\(\ce{SiO2}\). Ця формула не відповідає дійсності представляти стільки різних матеріалів, які ми називаємо силікатами, але ці речовини дійсно є\(\ce{SiO2}\). Деякі з мінералів містять домішки.
У чистому вигляді,\(\ce{SiO2}\) це кварц. Дрібні частинки кварцу - це пісок. Вони важкі. У структурі на атомарному рівні кожен атом кремнію пов'язаний з 4 атомами кисню, і кожен кисень пов'язаний з двома\(\ce{Si}\) атомами. Чотири\(\ce{Si-O}\) зв'язку вказують на кути тетраедра, як і\(\ce{C-C}\) зв'язки в алмазній структурі. Коли домішка присутня, кварц може бути пофарбований. Завдяки різному розташуванню\(\ce{Si-O-Si}\) зв'язків одна і та ж речовина з'являється у багатьох формах.
Основною одиницею силікатних конструкцій є\(\ce{SiO4^4-}\). Драгоцінний камінь циркон має формулу\(\ce{ZrSiO4}\), а олівін має хімічну формулу\(\ce{(MgFe)2SiO4}\). Дві\(\ce{SiO4^4-}\) одиниці об'єднуються, щоб дати піросилікатний блок\(\ce{Si2O7^6-}\), і він з'являється в акерманіті,\(\ce{Ca2MgSi2O7}\). Коли кількість одиниць збільшується, чотиригранні одиниці об'єднуються, утворюючи кільця, ланцюги, шари і тривимірні мережі. Таким чином, структура і класифікація силікату є основною частиною мінералів. (На цьому сайті є кілька цікавих фотографій.)
Кремній і силан
Елементарний кремній можна отримати з відновлення силікатів. Зменшення піску,\(\ce{SiO2}\) вуглецем при 3300 К в реакції,
\(\ce{SiO_2 + 2 C \rightarrow Si_{\large{(l)}} + 2 CO} \;\;\; \textrm{at 3300 K}\)
дає рідкий кремній. Отриманий таким чином кремній зазвичай не чистий, а для комп'ютерної промисловості елемент повинен бути очищений. Зростання кристалів і виготовлення кремнію домінують у промисловості в 1980-х і 1990-х роках, і, можливо, в наступному столітті, і виробництво елемента є лише початком процесу.
Якщо утворюється більш реактивний елемент\(\ce{Mg}\),, який використовується при\(\ce{Mg2Si}\) відновленні,
\(\ce{SiO_2 + 4 Mg \rightarrow Mg_2Si + 2 MgO}\)
\(\ce{Mg2Si}\)є сполукою, і вона реагує з водою з утворенням силану.
Силан,\(\ce{SiH4}\), може вироблятися, реагуючи\(\ce{Mg2Si}\) з кислотами
\(\ce{Mg_2Si + 4 H_2O \rightarrow 2 Mg(OH)_2 + SiH_4}\)
і\(\ce{SiH4}\) запалюється при контакті з повітрям, набагато більш реактивним, ніж метан,
\(\ce{SiH_4 + O_2 \rightarrow SiO_2 + H_2O}\)
У базовому розчині\(\ce{SiH4}\) реагує з водою, щоб дати\(\ce{SiO(OH)3-}\),
\(\ce{SiH_4 + OH^- + 3H_2O \rightarrow SiO(OH)_3^- + 4 H_2}\)
галогеніди кремнію
Тетрафторид кремнію утворюється\(\ce{HF}\), коли скло (\(\ce{SiO2}\)) піддається впливу і коли\(\ce{Si}\) реагує з\(\ce{F2}\),
\(\ce{SiO2 + 4 HF_{\large{(aq)}} \rightarrow 2 H2O + SiF_{4\large{(g)}}}\)
\(\ce{Si + 2 F2 \rightarrow SiF_{4\large{(g)}}}\)
Коли хлор проходить через гарячий пісок (\(\ce{SiO2}\)) і вуглець,\(\ce{SiCl4}\) утворюється,
\(\ce{SiO2 + Cl + 2 C2 \rightarrow 2CO + SiCl_{4\large{(g)}}}\)
\(\ce{SiCl4}\)і\(\ce{SiF4}\) реагувати з водою, щоб дати кремнієву кислоту,
\(\ce{SiCl4 + 4H2O \rightarrow 4 HCl + Si(OH)_{4\large{(aq)}}}\),
\(\ce{SiF4 + 4H2O \rightarrow 4 HF + Si(OH)_{4\large{(aq)}}}\).
силіконові полімери
Силікони - це полімери із загальною формулою\(\mathrm{(R_2SiO_2)_{\large n}}\) або\(\mathrm{(RSiO_3)_{\large n}}\), (\(\ce{R}\)=\(\ce{CH3}\),\(\ce{C2H5}\)\(\ce{C6H5}\), і т.д.). Ланцюг скріплюється\(\ce{Si-O-Si}\) зв'язками. Простий є\(\mathrm{((CH_3)_2SiO_2)_{\large n}}\),
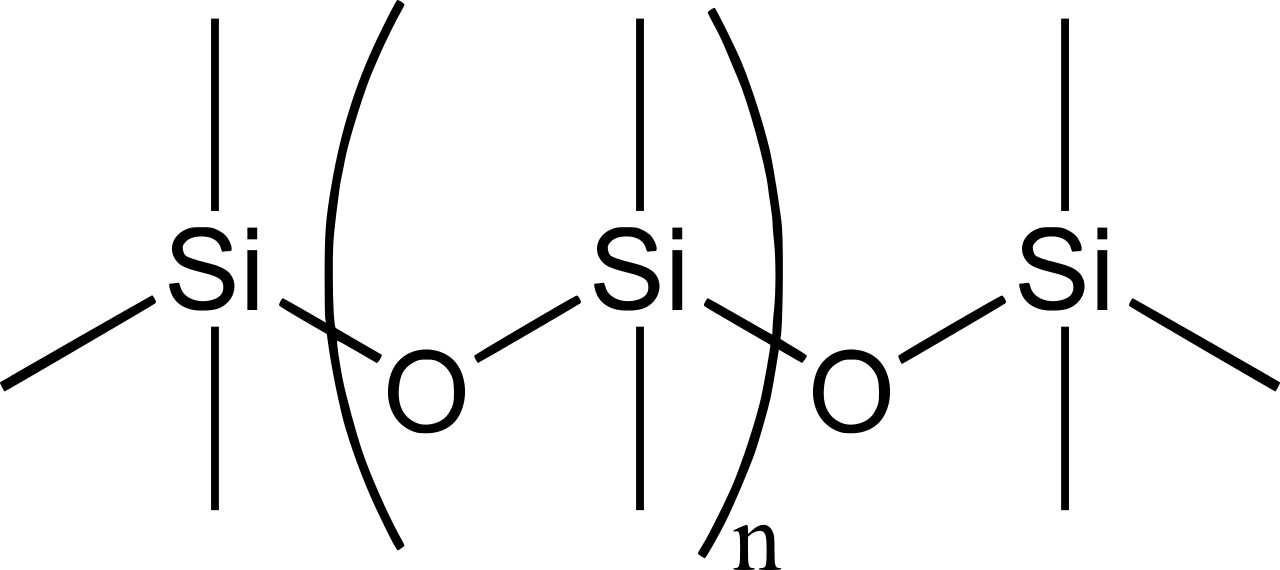
Малюнок 2: Хімічна структура силіконового полідиметилсилоксану (PDMS).
Звичайно, 4 облігації навколо\(\ce{Si}\) atoms point to the corners of a tetrahedron. These siloxane polymers are widely used as sealants, adhesives, additives, flame retardants, and lubricants. They have a wide application in industries. Depending on the organic group attached to silicon, the inorganic polymer Silicones has been an important class of materials.
Questions
- Which one lists the group 14 elements in order of increasing atomic weight?
- \(\textrm{B Al Ga In Tl}\)
- \(\textrm{C Si Ge Sn Pb}\)
- \(\textrm{N P As Sb Bi}\)
- \(\textrm{O S Se Te Po}\)
- \(\textrm{F Cl Br I At}\)
- Which allotrope of carbon is the hardest: diamond, graphite, or fullerenes?
- What compound of carbon reacts with water to give acetylene gas?
- When you want to extract silicon element, what do you use to reduce the sand: \(\ce{SiO2}\), \(\ce{C}\) or \(\ce{Mg}\)?
- Which is stable towards air: methane or silane?
- Give the name of polymers whose chains are held together by \(\ce{Si-O-Si}\) bonds.
- In the crystal structure of \(\ce{Si}\), how many other \(\ce{Si}\) atoms are connected to a particular \(\ce{Si}\) atom?
Solutions
- Answer b
Hint...
Knowing the groups of elements enables us to correlate their chemical properties. Each list of choices is a group of elements on the period table.
a = 3A, b = 14, c = 5A, d = 6A, e = 7A. -
Answer diamond
Hint...
Diamond is the hardest thing in the world. Fullerenes are large molecules consisting of 40 to hundreds of carbon atoms, with \(\mathrm{C_{60}}\) being the most common. -
Answer . . .\(\ce{CaC2}\)
Hint...
The reaction to produce acetylene gas is\(\ce{CaC2 + H2O \rightarrow C2H2 + Ca(OH)2}\)
Acetylene is still an important industrial gas, as raw material for polymers.
-
Answer ...\(\ce{C}\)
Hint...
Carbon or coke is used for silicon metal, because \(\ce{Mg2Si}\) is formed if \(\ce{Mg}\) is used. -
Answer ... methane is stable
Hint...
Methane is the major component of natural gas, and it will not react with air until ignited, whereas silane ignites explosively as soon as it contacts air. -
Answer ...silicones
Hint...
Silicon polymers are an important class of materials invented not too long ago. - Answer ... 4
Hint...
Silicon and diamond have the same crystal structure. The edge of unit cells of \(\ce{Si}\) is larger than that of diamond.
