6.13: Грати Браве та кришталева упаковка
- Page ID
- 27720
Браве решітки
Для опису кристала потрібно два інгредієнта: решітка і основа. Іншим чином, решітка описує, як атоми розташовані просторово: у кристалі це звичайний, впорядкований візерунок, який плитки тривимірного простору. Основою є одиниця, яка копіюється по шаблону: вона зазвичай складається з одного або декількох атомів. Кристалографи використовують набір скорочень, званих гратами Браве, для опису способів розташування атомів для утворення кристалічних твердих тіл. В\(3.091\), ми зупинимося на підмножині грат Браве, які є кубічними: масштаб у всіх трьох вимірах однаковий.
Існує три кубічні решітки: прості кубічні (SC), кубічні кубічні (BCC) та кубічні (FCC).
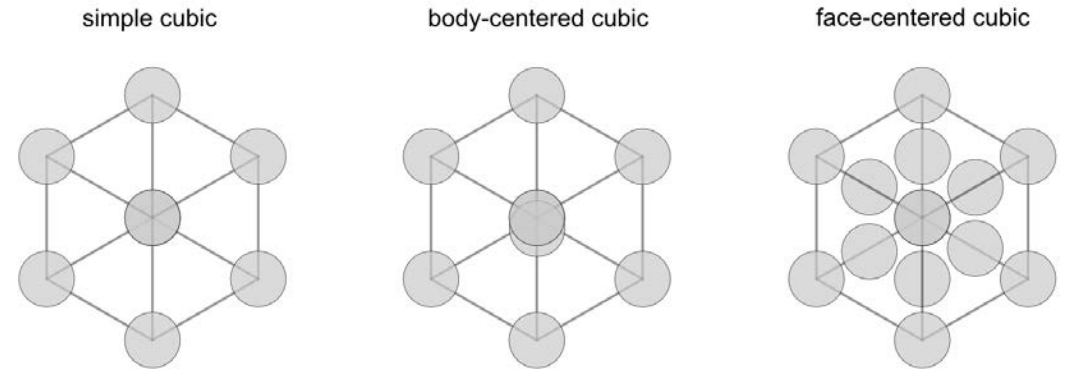
На малюнку вище сіра сітка показує контур одиничної комірки, а кожне коло представляє атом. Для атомів уздовж кутів одиничної клітини кожен атом ділиться між вісьмома сусідніми клітинами, тому кожна клітина містить\(1 / 8\) атом. Аналогічно, кожен з лицьових атомів у клітинці одиниці FCC поділяються між двома клітинами, тому кожна\(1 / 2\) містить атом. Ми можемо обчислити, скільки атомів знаходиться в кожній з кубічних одиничних комірок:
\(N_{S C}=8\)кути\(* \dfrac{1}{8}\) атомів на кут\(=1\) атома на\(\mathrm{SC}\) одиницю осередку
\(N_{B C C}=8\)кути\(* \dfrac{1}{8}\) атомів на кут атомів\(+1\) центрального\(=2\) атома на одиницю ОЦК осередку
\(N_{F C C}=8\)кутів\(* \dfrac{1}{8}\) атомів на кут\(+6\) грані атомів\(* \dfrac{1}{2}\) атомів на обличчя\(=4\) атомів на\(\mathrm{FCC}\) одиницю клітини
Кришталева упаковка
Тепер ми можемо визначити деякі відповідні метрики для опису атомної щільності в різних гратах і навіть у різних напрямках всередині кристала. Ми будемо говорити про щільність як за площею, так і за обсягом. Щоб визначити кілька термінів:
- щільність упаковки: відношення простору, зайнятого атомами, до загального доступного простору. Одиниці бувають\(\left[\frac{\text { atoms }}{n m^2}\right]\) (за площею) або\(\left[\frac{\text { atoms }}{n m^3}\right]\) за обсягом
- атомний коефіцієнт упаковки: частка простору, зайнятого атомами, в 2D (співвідношення площі) або 3D (коефіцієнт об'єму). Це безодиничне значення між 0 і 1.
Нам також потрібно запам'ятати кілька речей з геометрії: площа кола - це\(\pi r^2\), а обсяг сфери -\(\frac{4}{3} \pi r^3\). Для кубічної системи з довжиною сторони\(a\) має довжину діагоналі\(\sqrt{2} * a\) грані і довжину діагоналі корпусу\(\sqrt{3} * a\). Хитрість для успішного вирішення питань упаковки полягає в тому, щоб зв'язати радіус атомів (припускаючи, що вони є твердими сферами і якомога ближче упаковані) та довжину сторони одиничної комірки. Звідти це просто трохи алгебри, щоб знайти рішення.
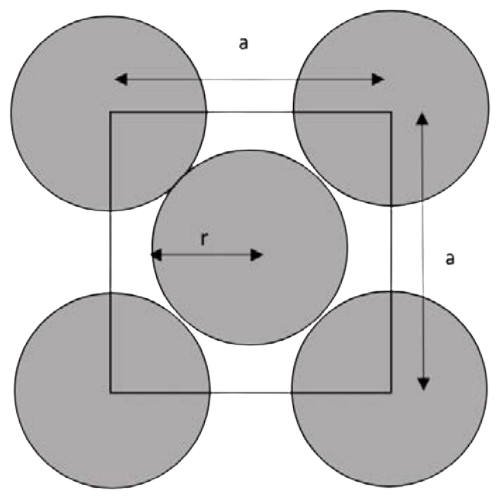
Приклад: Нижче наведено розділ комірки блоку FCC: це відріз однієї грані. Спочатку знайдіть зв'язок між радіусом атомів\(r\), і одиничною шириною комірки,\(a\). Потім визначте, скільки атомів знаходиться в\(2 \mathrm{D}\) одиничній клітині. Нарешті, обчислити щільність упаковки цієї площини (припускаючи\(a=3.5 \AA\)) та 2D атомну фракцію упаковки.
- Відповідь
-
По-перше, нам потрібно ставитися\(r\) до\(a\). Найпростіший спосіб зробити це, як правило, дивитися уздовж найближчого упакованого напрямку: тут, якщо ми йдемо вниз по діагоналі, атоми завжди контактують вздовж свого центру.
\[r+2 r+r=\sqrt{2} * a \nonumber\]
\[r=\dfrac{\sqrt{2}}{4} a \nonumber\]
Потім ми хочемо з'ясувати, скільки атомів укладено в квадратну,\(2 \mathrm{~d}\) одиничну клітинку. Посередині є один повний атом і чотири кути, кожен\(1 / 4\) з яких містить атом.
4 кутових\(* \dfrac{1}{4}\) атомів на кутовий\(+1\) центр\(=2\) атомів атомів на одиницю клітинки
Щільність упаковки в двох вимірах - це кількість атомів на квадратний нм. Ми можемо просто розділити кількість атомів в одиничній комірці на площу одиничної клітини:
\[\text { packing density }=\dfrac{2 \text { atoms per unit cell }}{(3.5 \AA)^2 \text { per unit cell }}\left(\dfrac{100 \AA^2}{1 \mathrm{~nm}^2}\right) \approx 16.33 \text { atoms } / \mathrm{nm}^2 \nonumber\]
Фракція упаковки в двох вимірах - це частка простору, зайнятого атомами:
\ begin {зібраний}
\ текст {дріб упаковки} =\ frac {\ text {площа, зайнята атомами}} {\ text {загальна площа}} =2 [\ текст {атоми}/\ текст {одинична комірка}] *\ вліво (\ frac {\ pi r^2 [\ text {площа на одиницю комірки}]}\ праворуч)\\
=\ frac {2\ pi *\ ліворуч (\ frac {\ sqrt {2}} {4 } a\ праворуч) ^2} {a^2} =\ frac {\ pi} {4} =0.7854
\ кінець {зібраний}