6.6: Принцип Ауфбау, заповнення електронів, позначення коробки та фотоелектронна спектроскопія
- Page ID
- 27710
Принцип Ауфбау
Квантові числа - це зручний спосіб обліку електронів, які заповнюють атомні оболонки, але їх може бути складно відстежувати. Натомість ми часто використовуємо скорочення для позначення квантових чисел:
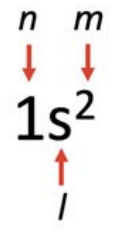
Принцип Aufbau - це трюк, щоб відстежувати порядок заповнення кожної підоболонки:
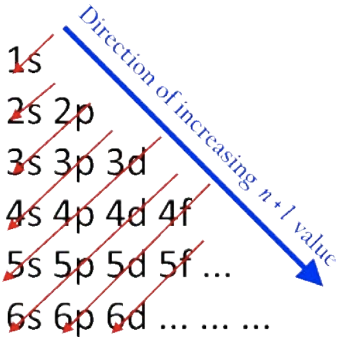
Верхній індекс після кожної підоболонки вказує кількість електронів у підоболонці: кожен повинен бути повним, крім самої зовнішньої оболонки, яка заповнюється виходячи з кількості валентних електронів.
Приклад: Запишіть як повну електронну конфігурацію, так і позначення благородного газу\(\mathrm{Br}\).
\(\mathrm{Br}\)має 35 валентних електронів, тому ми можемо заповнити весь шлях до аргону. Повна конфігурація, яка в основному слідує за Aufbau, є
\(1 \mathrm{~s}^2 2 \mathrm{~s}^2 2 \mathrm{p}^6 3 \mathrm{~s}^2 3 \mathrm{p}^6 3 \mathrm{~d}^{10} 4 \mathrm{~s}^2 4 \mathrm{p}^5\)
Відзначимо тут, що\(3 \mathrm{~d}^{10}\) і\(4 \mathrm{~s}^2\) відбуваються в несподіваному порядку: є деякі винятки з принципу Ауфбау. Ми не очікуємо, що ви запам'ятовуєте ці винятки для\(3.091\), але знаємо, що вони відзначені в таблиці Менделєєва! Конфігурація благородного газу якраз показує електрони за межами останньої повної оболонки:
\([\mathrm{Ar}] 3 \mathrm{~d}^{10} 4 \mathrm{~s}^2 4 \mathrm{p}^5\)
Електронне заповнення та позначення коробки
Можна відзначити конфігурацію і орієнтацію електронів візуально за допомогою коробкових позначень. Зазвичай найпростіше використовувати принцип Ауфбау (або таблицю Менделєєва!) записати електронну конфігурацію, а потім перевести її в поле позначення. Важливо згадати правило Гунда: кожна орбіталь у підоболонці повинна бути зайнята окремо, перш ніж будь-яка орбіталь буде зайнята подвійно.
Приклад: Намалюйте електронну конфігурацію\(\mathrm{Br}\) та позначення\(\mathrm{C}\) в коробці.
- Відповідь
-
Ми написали конфігурацію благородного газу вище, тому ми можемо просто дати поле позначення валентних електронів тут:
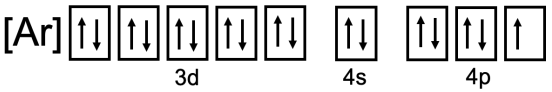
Для карбону електронна конфігурація є\(1 \mathrm{~s}^2 2 \mathrm{~s}^2 2 \mathrm{p}^2\). У полі позначення, ми заповнюємо\(1 \mathrm{~s}\) і\(2 \mathrm{~s}\) стани, і заповнюємо\(2 \mathrm{p}\) відповідно до правила Гунда:
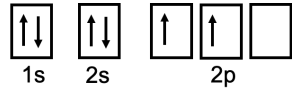
Фотоелектронна спектроскопія (ПЕС)
Фотоелектронна спектроскопія (ПЕС) - експериментальний метод, який використовується для визначення електронної структури. Спочатку зразок бомбардують фотонами високої енергії для іонізації атомів. Потім вимірюється кінетична енергія випромінюваних електронів. Енергію зв'язування можна визначити за допомогою
\(E_{b i n d i n g}=h \nu-K E_{e-}\)
Шляхом побудови відносних підрахунків електронів, що випромінюються з різними енергіями зв'язку, елементний склад зразка можна визначити за допомогою PES!
Приклад: Визначте, який елемент відповідає наступному спектру PES:
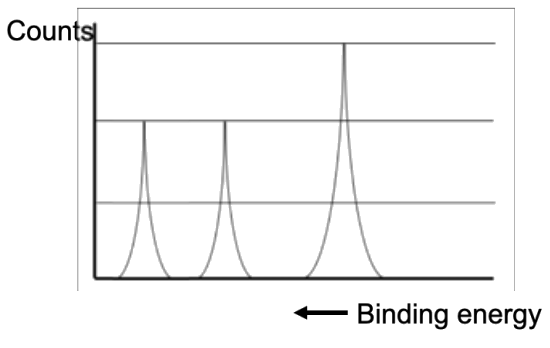
- Відповідь
-
На цій ділянці енергія зв'язування збільшується вліво. Електрони, що знаходяться ближче до ядра, повинні володіти найвищою енергією зв'язку, тому крайній лівий пік повинен відповідати\(1 \mathrm{~s}\) електронам. Відносна висота піку відповідає відносній частоті, на якій випромінюються електрони: оскільки є два 1s електрона, висота крайнього лівого піку повинна відповідати двом електронам. Середній пік повинен відповідати двом\(2 \mathrm{~s}\) електронам. Потім, оскільки крайній правий пік в\(1.5\) рази вище, він повинен представляти 3 електрони в\(2 \mathrm{p}\) підоболонці. Електронна конфігурація елемента на цій схемі ПЕС повинна бути\(1 \mathrm{~s}^2 2 \mathrm{~s}^2 2 \mathrm{p}^3\), яка відповідає азоту.