1.2: Ентальпія
- Page ID
- 27677
Термодинаміка - це вивчення взаємозв'язку між теплом (або енергією) і роботою. Ентальпія є центральним фактором термодинаміки. Це тепловміст системи. Тепло, яке проходить в систему або з неї під час реакції, - це зміна ентальпії. Чи збільшується ентальпія системи (тобто при додаванні енергії) або зменшується (тому що енергія виділяється) є вирішальним фактором, який визначає, чи може відбутися реакція.
Іноді ми називаємо енергію молекул, що зазнають змін, «внутрішньою ентальпією». Іноді ми називаємо це «ентальпією системи». Ці дві фрази відносяться до одного і того ж.
Аналогічно, енергія молекул, які не беруть участі в реакції, називається «зовнішньою ентальпією» або «ентальпією оточення».
Грубо кажучи, енергетичні зміни, які ми розглядали при введенні в термодинаміку, були змінами ентальпії. У наступному розділі ми побачимо, що є ще один енергетичний фактор - ентропія, який нам також потрібно враховувати в реакціях. Поки що ми просто розглянемо ентальпію.
- Ентальпія - це вміст тепла в системі.
- Зміна ентальпії реакції приблизно еквівалентна кількості енергії, втраченої або отриманої під час реакції.
- Реакція сприятлива, якщо ентальпія системи зменшується над реакцією.
Це останнє твердження дуже схоже на опис енергетики на попередній сторінці. Якщо система зазнає реакції і виділяє енергію, її власна енергетична зміст зменшується. Він має менше енергії, що залишилося, якщо він віддав деякі.
Чому енергія набору молекул змінюється при виникненні реакції? Щоб відповісти на це, нам потрібно подумати про те, що відбувається в хімічній реакції.
У реакції відбувається зміна хімічного зв'язку. Деякі зв'язки в реагентах розриваються, і нові зв'язки виготовляються для формування продуктів. Це коштує енергії, щоб розірвати зв'язки, але енергія виділяється при виготовленні нових зв'язків.
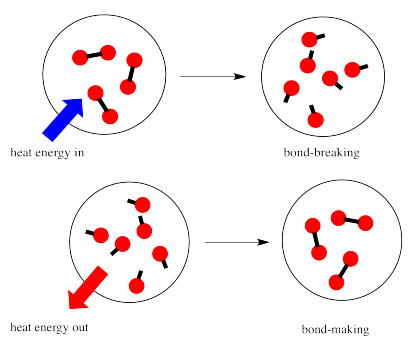
Чи здатна реакція йти вперед, може залежати від балансу між цими кроками створення облігацій та розриву облігацій.
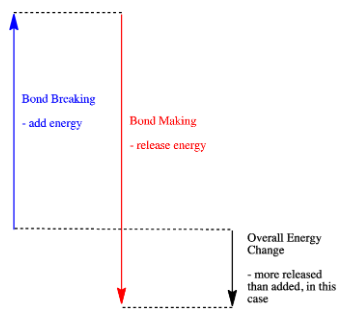
- Реакція екзотермічна, якщо при утворенні нових зв'язків виділяється більше енергії, ніж витрачається при розриві старих зв'язків.
- Реакція екзотермічна, якщо більш слабкі зв'язки торгуються на більш міцні.
- Реакція є ендотермічною, якщо розрив облігацій коштує більше енергії, ніж те, що забезпечується при виготовленні облігацій.
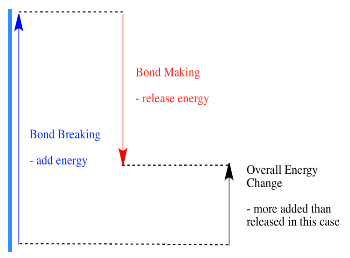
одна багато роботи з вимірюванням міцності зв'язків, і вони зібрали інформацію в таблицях, тому, якщо вам потрібно знати, наскільки міцна зв'язок, ви можете просто подивитися потрібну інформацію.
| Бонд | Енергія облігацій (ккал/моль) | Бонд | Енергія облігацій (ккал/моль) | |
|---|---|---|---|---|
| Ч Ч | 104 | О-Ч | 111 | |
| С-С | 83 | С-Ч | 99 | |
| О = О | 119 | Н-Ч | 93 | |
| N = N | 226 | С=О | 180 |
Наприклад, припустимо, ви хотіли дізнатися, чи було спалювання метану екзотермічною або ендотермічною реакцією. Я збираюся здогадатися, що це екзотермічно, тому що ця реакція (та інші подібні) використовується для забезпечення тепла для багатьох будинків шляхом спалювання природного газу в печах.
«Горіння» метану означає, що він спалюється на повітрі, завдяки чому вступає в реакцію з киснем. Продукти горіння вуглеводнів - це в основному вуглекислий газ і вода. Атом вуглецю в метані (CH 4) потрапляє в молекулу вуглекислого газу. Атоми водню включаються в молекули води. У метані є чотири атоми водню, тому цього достатньо, щоб зробити дві молекули H 2 O.
- Чотири С-Н зв'язку повинні бути розірвані при згорянні метану.
- Чотири нові O-H зв'язки створюються при додаванні водню з метану в нові молекули води.
- Дві нові зв'язки C = O утворюються, коли вуглець з метану додається в молекулу CO 2.
Інша частина головоломки є джерелом кисню для реакції. Кисень присутній в атмосфері переважно у вигляді O 2. Оскільки нам потрібні два атоми кисню в молекулі CO 2 і ще два атоми кисню для двох молекул води, нам потрібно загалом чотири атоми кисню для реакції, які можуть бути забезпечені двома молекулами O 2.
- Два зв'язку O = O повинні бути розірвані, щоб забезпечити атоми кисню для продуктів.
Загалом, це чотири C-H та дві облігації O = O, плюс дві зв'язки C = O та чотири O-H. Це 4 х 99 ккал/моль для зв'язків C-H та 2 х 119 ккал/моль для облігацій O = O, загалом додано 634 кДж/моль. Реакція випускає 2 х 180 ккал/моль для зв'язків C = O і 4 х 111 ккла/моль для OH облігацій, загальною кількістю 804 ккал/моль. Загалом, виділяється 170 ккал/моль більше, ніж споживається.
Це означає, що реакція екзотермічна, тому вона виробляє тепло. Це, мабуть, хороший спосіб обігріти свій будинок.
Порівняйте згоряння етану з спалюванням метану.
- Напишіть реакцію на згоряння етану, СН 3 СН 3, на вуглекислий газ і воду.
- Скільки молекул вуглекислого газу буде вироблено з однієї молекули етану?
- Скільки молекул води буде вироблено з однієї молекули етану?
- Скільки молекул кисню знадобиться для забезпечення атомів кисню для виконання кроків у питаннях (b) та (c)?
- Скільки енергії споживає/виробляється реакцією? Порівняйте цей результат з результатом для метану.
- Відповідь
- Відповідь на
-
Реакція наведена з структурами нижче:

- Відповідь б
-
Оскільки в етані є два вуглеці, одна молекула етану призведе до появи двох молекул СО 2.
- Відповідь c
-
Оскільки в етані є шість воднів, одна молекула етану дасть початок трьом молекулам H 2 O.
- Відповідь d
-
Для того, щоб зробити дві молекули вуглекислого газу (чотири атоми кисню) і три молекули води (три атоми кисню), нам знадобиться сім атомів кисню загалом. Оскільки молекули кисню містять пари атомів кисню, нам знадобиться лише 3,5 молекули кисню.
- Відповідь e
-
Енергетичні потреби викладені в наступній таблиці. В цілому реакція виділяє 375,5 ккал на моль спаленого етану. Негативний знак в таблиці часто використовується для позначення того, що це надлишок енергії, що виділяється (тоді як позитивний знак буде вказувати на те, що енергія як споживана в цілому).
Розрив облігацій Витрати (ккал/моль) Сума вартості Виготовлення облігацій Релізи (ккал/моль) Сума випуску Загальний (ккал/моль) 6 х С-Н 6 * 99 594 6 х О-Н 6 * 111 666 3,5 х О = О 3,5 * 119 416,5 4 х С = О 4 * 180 720 1 х С-С 83 83 Всього л порушення: 1093.5 виготовлення: 1386 -292.5 Це більше енергії, ніж було вироблено з молекули метану (-170 ккал/моль).
Процес Хабер-Бош використовується для виготовлення аміаку для добрив. Він використовує реакцію газоподібного водню (H 2) з атмосферним азотом (N 2) у співвідношенні 3:1 для отримання аміаку (NH 3).
- Напишіть реакцію на процес Хабер-Боша.
- Скільки молекул аміаку буде вироблено з однієї молекули азоту?
- Скільки енергії споживає/виробляється реакцією?