12.2: Хімічні реакції
- Page ID
- 24653
Хімічні реакції
Хімічні реакції постійно відбуваються в організмі. Вони є нормальним аспектом життя, беручи участь в:
- Нарощування нової тканини.
- Відривання старої тканини.
- Перетворення їжі в енергію.
- Утилізація відпрацьованих матеріалів.
- Усунення токсичних ксенобіотиків.
Усередині організму знаходиться чудова збірка хімічних реакцій, яка добре організована і закликається в міру необхідності. Більшість цих хімічних реакцій протікають зі значними темпами лише тому, що для їх каталізації, тобто прискорюють реакцію, присутні специфічні білки, відомі як ферменти. Каталізатор - це речовина, здатне прискорити хімічну реакцію іншої речовини, не зазнаючи себе постійної хімічної зміни.
Ферменти
Ферменти є каталізаторами майже всіх біохімічних реакцій в організмі. Без цих ферментів необхідні реакції біотрансформації відбувалися б повільно або зовсім не відбуватимуться, викликаючи серйозні проблеми зі здоров'ям.
Ти знав?
Фенілкетонурія (ФКУ) - генетичний стан, при якому фермент, який біотрансформує фенілаланін в тирозин (іншу амінокислоту), дефектний. В результаті фенілаланін може накопичуватися в організмі і викликати сильну розумову відсталість. Немовлят регулярно перевіряють при народженні на ПКУ. Якщо у них є ФКУ, їм потрібно дотримуватися спеціальної дієти, щоб обмежити прийом фенілаланіну в дитячому і дитячому віці.

Малюнок\(\PageIndex{1}\). Тестування фенілкетонуї (ПКУ) у немовляти
(Джерело зображення: Wikimedia Commons, отримане за ліцензією Public Domain). Автор: Фотографічні архіви ВПС США)
Ці ферментативні реакції не завжди є простими біохімічними реакціями. Деякі ферменти вимагають наявності кофакторів або коферментів на додаток до субстрату (речовини, що підлягає каталізації), перш ніж їх каталітична активність може бути проявлена. Ці кофактори існують як нормальний компонент у більшості клітин і часто беруть участь у загальних реакціях на перетворення поживних речовин в енергію (вітаміни є прикладом кофакторів). Саме лікарський засіб або хімічно трансформують ферменти, які тримають ключ до ксенобіотичної трансформації. Взаємозв'язок субстрату, ферменту, коензиму та перетвореного продукту можна показати як:
\(substrate*\dfrac{enzyme}{co-enzyme} = transformed product\)
Більшість біотрансформаційних ферментів - це високомолекулярні білки, що складаються з ланцюгів амінокислот, пов'язаних між собою пептидними зв'язками. Існує велика різноманітність біотрансформаторних ферментів. Більшість ферментів каталізують реакцію лише декількох субстратів, а це означає, що вони мають високу специфічність. Специфічність - це функція структури ферменту та його каталітичних ділянок. Хоча фермент може зіткнутися з багатьма різними хімічними речовинами, лише ті хімічні речовини (субстрати), які вписуються в заплутану структуру ферменту та просторове розташування, будуть заблоковані та уражені. Це іноді називають відносинами «замок і ключ».
Як показано на малюнку\(\PageIndex{2}\), коли субстрат вписується в структуру ферменту, може утворюватися ферментно-субстратний комплекс. Це дозволяє ферменту вступати в реакцію з субстратом в результаті чого утворюються два різних продукту. Якщо субстрат не вписується в фермент («несумісний»), ніякого комплексу утворюватися не буде і таким чином ніякої реакції виникнути не може.

Малюнок\(\PageIndex{2}\). Якщо субстрат не вписується в фермент, ніякого комплексу утворюватися не буде і ніякої реакції не відбудеться.
(Джерело зображення: NLM)
ферментна специфічність
Ферменти варіюються від абсолютної специфічності до широкої та перекривається специфічності. В цілому виділяють три основних види специфіки:
- Абсолютний — фермент буде каталізувати тільки одну реакцію. Приклади:
- Формальдегіддегідрогеназа каталізує тільки реакцію на формальдегід.
- Ацетилхолінестераза біотрансформує нейротрансмісірующую хімічну речовину ацетилхолін.
- Група — фермент буде діяти тільки на молекули, які мають певні функціональні групи, такі як амінофосфатні або метильні групи.
- Наприклад, алкогольдегідрогеназа може біотрансформувати кілька різних спиртів, включаючи метанол і етанол.
- Зв'язка - фермент буде діяти на певний тип хімічного зв'язку незалежно від решти молекулярної структури.
- Наприклад, N-окислення може каталізувати реакцію азотного зв'язку, замінюючи азот киснем.
Угода про іменування ферментів
Назви, присвоєні ферментам, спочатку можуть здатися заплутаними. Однак, за винятком деяких спочатку вивчених ферментів (таких як пепсин і трипсин), прийнята конвенція про назву ферментів. Назви ферментів закінчуються на «ази» і зазвичай поєднують субстрат, що діє на і тип реакції, що каталізується.
Наприклад, алкогольдегідрогеназа - це фермент, який біотрансформує спирти шляхом видалення водню. В результаті виходить зовсім інша хімічна речовина, альдегід або кетон.
Біотрансформація етилового спирту в ацетальдегід зображена на малюнку\(\PageIndex{3}\).
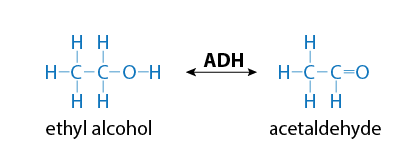
АДГ = алкогольдегідрогеназа, специфічний каталізуючий фермент
Малюнок\(\PageIndex{3}\). Біотрансформація етилового спирту
(Джерело зображення: NLM)
|
Корисно чи шкідливо? |
Малюнок\(\PageIndex{4}\). Загальні ацетамінофен таблетки |
Фази реакції біотрансформації
Реакції біотрансформації класифікуються не тільки за характером їх реакцій, наприклад, окислення, але і за нормальною послідовністю, з якою вони схильні реагувати з ксенобіотиком. Зазвичай їх класифікують як реакції фази I та фази II.
Реакції фази I - це, як правило, реакції, які змінюють хімічну речовину, додаючи функціональну структуру. Це дозволяє речовині «вписатися» в другий, або фермент II фази, завдяки чому воно може кон'югуватися (з'єднатися) з іншою речовиною.
Реакції II фази складаються з тих ферментативних реакцій, які кон'югують модифікований ксенобіотик з іншою речовиною. Кон'юговані продукти - це більші молекули, ніж субстрат і, як правило, полярні в природі (розчинні у воді). Таким чином, вони можуть легко виводитися з організму. Кон'юговані сполуки також мають погану здатність перетинати клітинні мембрани.
У деяких випадках ксенобіотик вже має функціональну групу, яку можна кон'югувати, а ксенобіотик може бути біотрансформований реакцією фази II, не проходячи реакції фази I.
Наприклад, фенол може бути безпосередньо кон'югований в метаболіт, який потім може виводитися з організму. Біотрансформація бензолу вимагає реакцій як фази I, так і фази II. Як показано на малюнку\(\PageIndex{5}\), бензол спочатку біотранформується в фенол реакцією фази I (окислення). Фенол має структуру, що включає функціональну гідроксильну групу, яка потім кон'югована реакцією фази II (сульфатація) до фенілсульфату.

Малюнок\(\PageIndex{5}\). Біотрансформація бензолу в фенол у фазі 1 (окислення), яка потім кон'югується реакцією фази 2 (сульфатація) до фенілсульфату
(Джерело зображення: NLM)
У таблиці 1 наведено основні реакції трансформації ксенобіотиків, розбитих на реакції фази I та фази II. Ці реакції більш детально розглянуті нижче.

Реакції фази I
Реакції біотрансформації фази I - це прості реакції порівняно з реакціями фази II. У реакціях фази I невелика полярна група (що містить як позитивні, так і негативні заряди) або піддається впливу токсиканту, або додається до токсиканту. Три основні реакції фази I - 1) окислення; 2) відновлення; і 3) гідроліз.
Окислення
Окислення - це хімічна реакція, при якій субстрат втрачає електрони. Існує ряд реакцій, за допомогою яких можна домогтися видалення електронів з підкладки.
- Додавання кисню, або оксигенація, було першою з цих реакцій виявлено, і, таким чином, реакція була названа окисленням. Однак багато окислювальних реакцій не залучають кисень.
- Найпростіший вид реакції окислення - дегідрування, що представляє собою видалення водню з молекули.
- Іншим прикладом окислення є перенесення електронів, який складається просто з перенесення електрона з підкладки.
\(\PageIndex{6}\)На малюнку показані ці види окислювальних реакцій.

Малюнок\(\PageIndex{6}\). Три типи реакцій окислення
(Джерело зображення: NLM)
Специфічних окислювальних реакцій і окислювальних ферментів безліч і цьому предмету присвячено кілька підручників. Більшість реакцій описуються назвою реакції або бере участь фермент. Деякі з цих окислювальних реакцій включають:
- Дегідрування спирту
- дегідрування альдегіду
- Алкіл/ациклічне гідроксилювання
- Ароматичне гідроксилювання
- Десамінація
- десульфурація
- N-деалкілування
- N-гідроксилювання
- N-окислення
- О-деалкілування
- сульфоксидування
Зменшення
Редукція - це хімічна реакція, при якій субстрат набирає електрони. Скорочення, швидше за все, відбуваються з ксенобіотиками, в яких вміст кисню низький. Скорочення може відбуватися через подвійні зв'язки азот і азот (азо відновлення) або на нітрогрупах (NO2). Часто отримані аміносполуки окислюються, що утворює токсичні метаболіти. Деякі хімічні речовини, такі як чотирихлористий вуглець, можуть бути зведені до вільних радикалів, які досить реагують з біологічними тканинами. Таким чином, реакції зниження часто призводять до активації ксенобіотика, а не детоксикації. Приклад реакції відновлення, при якій знижується нітрогрупа, проілюстрований на рис\(\PageIndex{7}\).

Існує менше специфічних реакцій відновлення, ніж окислювальні реакції. Характер цих реакцій також описується їх назвою. Деякі відновлювальні реакції включають:
- Зменшення азо
- Дегалогенація
- Зниження дисульфіду
- Зниження нітро
- Зниження N-оксиду
- Зниження сульфоксиду
Гідроліз
Гідроліз - це хімічна реакція, при якій додавання води розщеплює токсикант на два фрагменти або більш дрібні молекули. Гідроксильна група (ОН-) включена в один фрагмент, а атом водню включений в інший. Більші хімічні речовини, такі як ефіри, аміни, гідразини та карбамати, як правило, біотранформуються шляхом гідролізу.
Приклад гідролізу ілюструється в біотрансформації прокаїну (місцевого анестетика), який гідролізується до двох менших хімічних речовин (рис.\(\PageIndex{8}\)).
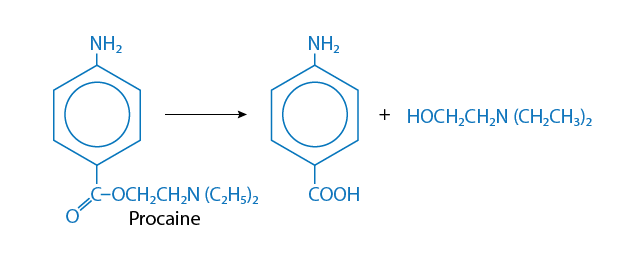
Малюнок\(\PageIndex{8}\). Гідроліз прокаїну
(Джерело зображення: адаптовано з Державного університету Гумбольдта, хімічний факультет. Автор: Річард Паселк, заслужений професор. Переглянути оригінальне зображення.)
Токсиканти, які зазнали фази I біотрансформації, перетворюються в метаболіти, які є достатньо іонізованими або гідрофільними, які або виводяться з організму без подальшої біотрансформації, або перетворюються на проміжний метаболіт, готовий до біотрансформації фази II. Проміжні продукти перетворення фази I можуть бути фармакологічно більш ефективними і в багатьох випадках більш токсичними, ніж батьківський ксенобіотик.
Реакції фази II
Ксенобіотик, який пройшов реакцію фази I, тепер є новим проміжним метаболітом, який містить реактивну хімічну групу, таку як гідроксил (-OH), аміно (-NH2) та карбоксил (-COOH). Багато з цих проміжних метаболітів не володіють достатньою гідрофільністю, щоб дозволити виведення з організму. Ці метаболіти повинні пройти додаткову біотрансформацію як реакція фази II.
Реакції фази II - це реакції кон'югації, коли молекула, яка зазвичай присутня в організмі, додається до реактивного місця метаболіту фази I. Результатом є кон'югований метаболіт, який є більш розчинним у воді, ніж вихідний ксенобіотик або метаболіт фази I. Зазвичай метаболіт II фази досить гідрофільний і може бути легко виведений з організму. Первинними реакціями фази II є:
- Кон'югація глюкуроніду - найважливіша реакція (докладно нижче)
- Кон'югація сульфату - важлива реакція (докладно нижче)
- ацетилювання
- Кон'югація амінокислот
- Кон'югація глутатіону
- метилювання
Кон'югація глюкуроніду
Кон'югація глюкуроніду - одна з найважливіших і поширених реакцій II фази. У цій реакції використовується молекула глюкуронової кислоти. Він отримується з глюкози, загального вуглеводу (цукру), який є основним джерелом енергії для клітин. У цій реакції глюкуронова кислота додається безпосередньо до токсиканту або його метаболіту фази I. Місцями реакцій глюкуронідації є субстрати, що мають кисень, азот або сірчаний зв'язок, які застосовуються до широкого спектру ксенобіотиків, а також ендогенних речовин, таких як білірубін, стероїдні гормони та гормони щитовидної залози.
Глюкуронідація - це шлях, який кон'югує ксенобіотики з високою потужністю («шлях високої ємності»). Кон'югація глюкуроніду зазвичай зменшує токсичність, хоча є деякі помітні винятки, наприклад, коли це може призвести до утворення канцерогенних речовин. Кон'югати глюкуроніду, як правило, досить гідрофільні і виводяться ниркою або жовчю, залежно від розміру кон'югату. Кон'югація глюкуроніду аніліну проілюстрована на малюнку\(\PageIndex{9}\).
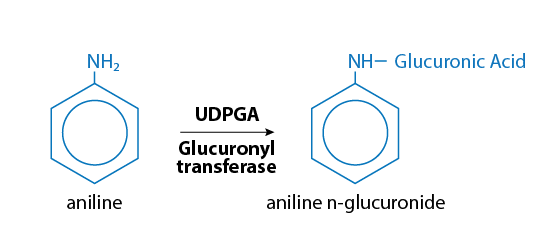
Малюнок\(\PageIndex{9}\). Глюкуронідна кон'югація аніліну (який використовується для виготовлення поліуретану, фармацевтичних препаратів та промислових хімічних речовин)
(Джерело зображення: NLM)
Кон'югація сульфату
Кон'югація сульфатів - ще одна важлива реакція фази II, яка виникає з багатьма ксенобіотиками. В цілому сульфатація знижує токсичність ксенобіотиків. На відміну від кон'югатів глюкуронової кислоти, які часто виводяться з жовчю, високополярні сульфатні кон'югати легко секретуються з сечею. Взагалі сульфатація - це шлях низької ємності для кон'югації ксенобіотиків. Часто глюкуронідація або сульфатація можуть кон'югувати одні і ті ж ксенобіотики.
1) Речовини в організмі, що прискорюють хімічні реакції, відомі як:
а) амінокислоти
б) ферменти
в) субстрати
- Відповідь
-
ферменти - це правильна відповідь.
Ферменти - це білки, які каталізують практично всі біохімічні реакції в організмі.
2) Конвенція, що використовується для назви конкретних ферментів, складається з
поєднання: а) Назва субстрату з типом хімічної реакції
б) Орган-мішень та тип хімічної реакції
c) Назва субстрату з формою токсичності
- Відповідь
-
Назва субстрату з типом хімічної реакції - Це правильна відповідь.
Назви ферментів закінчуються на «ази» і зазвичай поєднують субстрат, що діє на і тип реакції, що каталізується.
3) Реакції біотрансформації класифікуються як фази I і фази II. Основна відмінність полягає в:
а) реакції фази I кон'югують субстрат, тоді як реакції фази II окислюють речовину
б) реакції фази I, як правило, додають функціональну структуру, тоді як реакції фази II кон'югують речовину
c) реакція фази I, як правило, робить речовину більш гідрофільною, ніж реакція фази II
- Відповідь
-
Реакції фази I зазвичай додають функціональну структуру, тоді як реакції фази II кон'югують речовину - це правильна відповідь.
Реакції фази I - це, як правило, реакції, які змінюють хімічну речовину, додаючи функціональну структуру. Це дозволяє речовині «вписатися» в фермент II фази, щоб воно могло кон'югуватися (з'єднатися) з іншою речовиною. Реакції II фази складаються з тих ферментативних реакцій, які кон'югують модифікований ксенобіотик з іншою речовиною.
4) Різниця між реакціями окислення та відновлення полягає в:
а) Підкладка отримує електрони від реакції окислення, тоді як вона втрачає електрони реакцією відновлення
b) Кисень видаляється з підкладки при окисленні та додається при відновленні реакція в
) субстрат втрачає електрони від реакції окислення, тоді як він отримує електрони реакцією відновлення
- Відповідь
-
Субстрат втрачає електрони від реакції окислення, тоді як він отримує електрони реакцією відновлення - Це правильна відповідь.
Окислення - це хімічна реакція, при якій субстрат втрачає електрони. Редукція - це хімічна реакція, при якій субстрат набирає електрони.
5) Яка реакція кон'югації найбільш поширена при біотрансформації ксенобіотиків?
а) Кон'югація амінокислот
б) Кон'югація глюкуроніду в
) Метилювання
- Відповідь
-
Кон'югація глюкуроніду - це правильна відповідь.
Кон'югація глюкуроніду - одна з найважливіших і поширених реакцій II фази. Глюкуронідація - це шлях високої ємності для кон'югації ксенобіотиків.
