14.2: Вода в природі
- Page ID
- 20668
- Знати розподіл земної води.
- Опишіть водний (гідрологічний) цикл.
- Знайте різні природні забруднення води
На вплив води на навколишній світ впливають її унікальні властивості, деякі з яких розглядалися в попередньому розділі. Без води життя може не існувати на Землі, і воно, безумовно, не матиме величезної складності та різноманітності, які ми бачимо.
Розподіл земної води
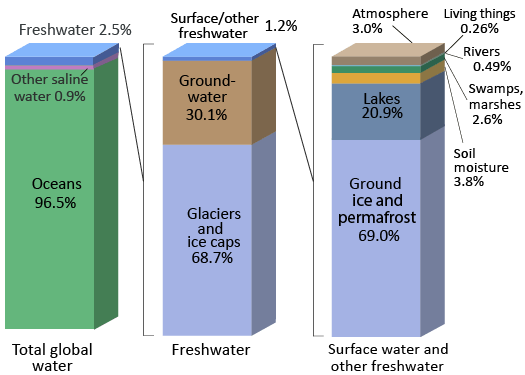
Океани Землі містять 97% води планети, тому всього 3% - це прісна вода, вода з низькими концентраціями солей (рис.\(\PageIndex{1}\)). Більшість земної води можна класифікувати як сольові (або солі, що містять). Більшість прісної води потрапляють у пастку як лід у величезних льодовиках та крижаних покривах Гренландії. Місце для зберігання води, таких як океан, льодовик, ставок або навіть атмосфера, відомий як водосховище.
Водний (гідрологічний) цикл і природні забруднювачі
Оскільки вода Землі присутня у всіх трьох державах, вона може потрапити в різні середовища по всій планеті. Рух води навколо поверхні Землі - це кругообіг води (рис.\(\PageIndex{2}\)).
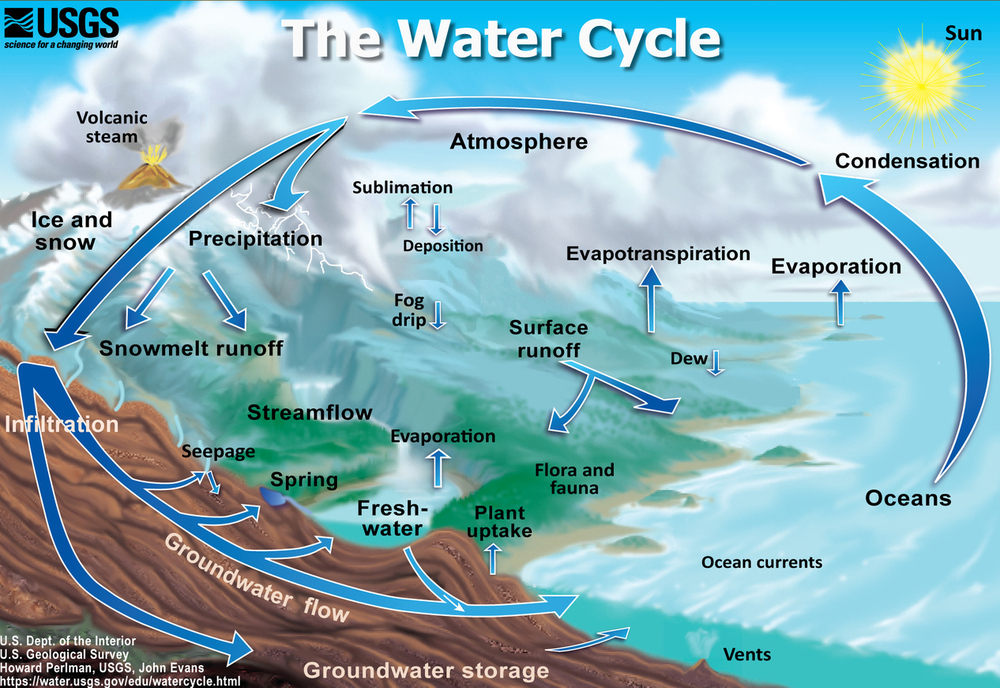
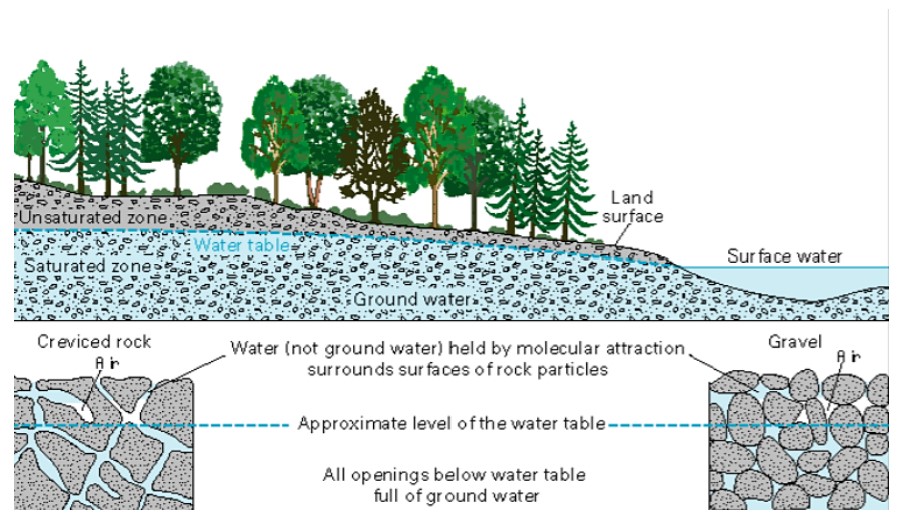
Вода змінюється від рідини до газу шляхом випаровування, щоб стати водяною парою. Енергія Сонця може випаровувати воду з поверхні океану або з озер, струмків або калюж на суші. Випаровуються тільки молекули води; солі залишаються в океані або прісноводному резервуарі. Водяна пара залишається в атмосфері до тих пір, поки не піддається конденсації, а потім випадання опадів. Опадами можуть бути дощ, мокрий сніг, град або сніг. На поверхні, вода або тала вода, може з часом випаруватися і знову потрапити в атмосферу. Значна кількість води проникає в грунт. Вода може просочуватися через бруд і породу нижче грунту через пори, що проникають в землю, щоб перейти в систему ґрунтових вод Землі (рис.\(\PageIndex3}\)). Грунтові води потрапляють у водоносні горизонти, які є тілами гірської породи або осаду, які зберігають (і дають) велику кількість корисної води у своїх порах. Як варіант, вода може вийти на поверхню через джерела або знайти свій шлях назад до океанів.
Речовини, присутні в природних водах
Кількість води, присутня в атмосфері та на суші (як поверхневий стік, озера та струмки), достатньо велика, щоб зробити її значним агентом у транспортуванні речовин між літосферою (жорсткою поверхнею землі) та океанами. Вода взаємодіє як з атмосферою, так і з літосферою (жорсткою поверхнею землі), отримуючи розчинені речовини з кожного, і, таким чином, забезпечує основний хімічний зв'язок між цими двома царствами. Різні перетворення, зазнали води на різних етапах гідрологічного циклу, діють для транспортування як розчинених, так і твердих речовин між різними географічними місцями.
Закон про безпечну питну воду визначає термін «забруднювач» як означає будь-яку фізичну, хімічну, біологічну або радіологічну речовину або речовину у воді. Тому закон визначає «забруднювач» дуже широко як щось інше, ніж молекули води.
Гази
Вуглекислий газ в природній воді створює цікаве явище. Дощова вода насичується СО 2, і вона розчиняє вапняки. При втраті СО 2 через перепади температур або виходу з крапель води відбувається зворотна реакція. Однак утворюється тверда речовина може бути менш стабільною фазою під назвою арагоніт, яка має ту ж хімічну формулу, що і, але іншу кристалічну структуру, ніж у кальциту.
Дощ розчиняє карбонат кальцію двома реакціями, показаними вище. Вода несе з собою іони, потягує крізь тріщину гірських порід. Коли вона дійшла до стелі печери, крапля довго бовтається там, перш ніж впав. За цей час викидається вуглекислий газ і підвищується рН води. Починають з'являтися кристали карбонату кальцію. Кальцит, арагоніт, сталактит та сталагміт - це чотири загальні тверді речовини, знайдені в утворенні печер.
розчинені мінерали
У таблиці\(\PageIndex{1}\) наведено основні іони, присутні в морській воді. Склад змінюється, залежно від регіону, глибини, широти та температури води. Води біля гирла річок містять менше солі. Якщо іони утилізуються живим організмом, його вміст змінюється залежно від популяцій організмів.
Частинки пилу та іони, присутні в повітрі, є центром зародження крапель води. Так, води від дощу і снігу також містять такі іони: Ca 2+, Mg 2+, Na +, K +, NH 4 +. Ці катіони врівноважуються аніонами, HCO 3 -, SO 4 -, NO 2 -, Cl -, і NO 3 -. РН дощу становить від 5,5 до 5,6. Дощові та снігові води з часом стають річковими або озерними водами. Коли випадають дощові або снігові води, вони взаємодіють з рослинністю, верхнім грунтом, гірською породою, руслом річки та руслом озера, розчиняючи все, що розчиняється. Бактерії, водорості та водні комахи також процвітають. Розчинності неорганічних солей регулюються кінетикою і рівновагами розчинення. Найбільш поширені іони в озерних і річкових водах такі ж, як і в дощовій воді, але в більш високих концентраціях. Рівень рН цих вод залежить від русла річки і русла озера. Природні води містять розчинені мінерали. Води, що містять іони Ca 2+ і Mg 2+, зазвичай називають жорсткою водою.
|
катіони
|
г/кг
|
аніони
|
г/кг
|
|---|---|---|---|
| На + |
10.77
|
Cl — |
19.354
|
| Мг 2 + |
1.29
|
ТАК 4 2— |
2.712
|
| Са 2 + |
0,412
|
Бр — |
0.087
|
| К + |
0,399
|
||
| Ср 2 + |
0.0079
|
||
| Всі 3 + |
0,005
|
Хоча більшість елементів містяться в морській воді лише на слідових рівнях, морські організми можуть вибірково поглинати їх і зробити їх більш помітними. Йод, наприклад, був виявлений у морських водоростях (морських водоростях) за 14 років до того, як його знайшли в морській воді. Інші елементи, які не були виявлені в морській воді до тих пір, поки вони не були виявлені в морських організмах, включають барій, кобальт, мідь, свинець, нікель, срібло та цинк. Si-32, імовірно, походить від бомбардування космічними променями Ар, був виявлений у морських губках.
Жорстка вода
Мінерали зазвичай розчиняються в природних водоймах, таких як озера, річки, джерела та підземні водні шляхи (грунтові води). Карбонат кальцію, CaCo 3, є одним з найбільш поширених неорганічних сполук в земній корі. Це інгредієнт як для кальциту, так і арагоніту. Ці два мінерали мають різну кристалічну структуру і зовнішній вигляд. На цій фотографії зображені кристали типового кальциту.
Кальцієво-карбонатні мінерали розчиняються у воді з продуктом розчинності, як показано нижче.
\[CaCO_3 \rightleftharpoons Ca^{2+} + CO_3^{2-} \;\;\; K_{sp} = 5 \times 10^{-9} \nonumber \]
З продукту розчинності ми можемо (див. Приклад 1) оцінити молярну розчинність в 7,1х10 -5 М або 7,1 мг/л (7,1 проміле СаСО 3 у воді). Розчинність збільшується в міру зниження рН (підвищення кислотності). Це посилюється при насиченні води вуглекислим газом, СО 2. Насичений розчин СО 2 містить вугільну кислоту, яка сприяє розчиненню за рахунок реакції:
\[H_2O + CO_2 \rightleftharpoons H_2CO_3 \nonumber \]
\[CaCO_3 + H_2CO_3 \rightleftharpoons Ca^{2+} + 2 HCO_3^- \nonumber \]
Через ці реакції деякі природні води містять більше 300 ppm карбонатів кальцію або його еквівалентів.
Склад океану привернув увагу деяких з більш відомих в науці імен, серед яких Роберт Бойл, Антуан Лавуазьє і Едмунд Галлей. Їх ранні дослідження, як правило, важко відтворити через різні умови, за яких вони кристалізували різні солі. Цілих 54 солей, подвійних солей і гідратованих солей можна отримати шляхом випаровування морської води до сухості. Щонайменше 73 елементи зараз, як відомо, присутні в морській воді.
Органічні речовини
Велика частина органічного вуглецю в морській воді присутня як розчинений матеріал, з лише близько 1-2% в частинках. Загальний вміст органічного вуглецю коливається від 0,5 мг/л у глибокій воді до 1,5 мг/л біля поверхні. До цих пір існують значні розбіжності щодо складу розчиненої органічної речовини; значна частина її, здається, має високу молекулярну масу і може бути полімерною. Речовини, якісно схожі з гуміновими кислотами, що знаходяться в грунтах, можна виділити. Зеленуватий колір, який часто асоціюється з прибережними водами, обумовлений сумішшю флуоресцентних високомолекулярних речовин невизначеного складу, відомого як «Гельбстофф». Цілком ймовірно, що значення органічної фракції морської води може бути набагато більшим, ніж припускає її низька кількість. З одного боку, багато з цих речовин є ліпідними і, як правило, адсорбуються на поверхнях. Показано, що будь-яка частинка, що потрапляє в океан, швидко покривається органічною поверхневою плівкою, яка може впливати на швидкість і ступінь її розчинення або розкладання. Деякі неорганічні іони можуть сильно комплексуватися гуміноподібними речовинами. Поверхня океану в основному покрита органічною плівкою, товщиною всього кілька молекулярних шарів. Вважається, що це складається з вуглеводнів, ліпідів тощо, але повідомлялося про глікопротеїни та протеоглікани. Якщо цю плівку акуратно вийняти з ємності з морською водою, вона швидко відновиться. Наскільки значуща ця плівка за своїм впливом на газообмін з атмосферою, невідомо.
Резюме
- Водний (гідрологічний) цикл описує безперервний рух води по, над і нижче поверхні Землі. Вода рухається з одного водосховища в інший, наприклад, з річки в океан, або з океану в атмосферу, фізичними процесами випаровування, конденсації, опадів, інфільтрації, поверхневого стоку та підземного потоку. При цьому вода проходить через різні форми: рідку, тверду (крижану) і капорну.
- Різні речовини, які можна знайти в природних водах, включають розчинені мінерали, розчинені гази та органічні речовини.
Автори та атрибуція
- Template:ContribCandelaGeo
- Template:contribgordon
- TextMap: Introduction to Environmental Science (Zendher et al.)
- Template:Contribchieh
- Template:ContribAgnewM
- Template:ContribLower