12.1: Органічні реакції
Результати навчання
- Визначте та опишіть реакції заміщення, усунення, додавання, гідролізу та конденсації.
- Прогнозуйте продукти кожного типу реакції.
- Прогнозують продукти реакцій гідратації виходячи з правила Марковникова.
- Поясніть, чому реакції конденсації також називають реакціями зневоднення.
- Визначте «полімер».
Органічні реакції вимагають розриву міцних ковалентних зв'язків, що забирає значний внесок енергії. Для того щоб відносно стабільні органічні молекули реагували з розумною швидкістю, їх часто необхідно модифікувати з використанням високореактивних матеріалів або в присутності каталізатора. У цьому уроці ви дізнаєтеся про кілька загальних категоріях органічних реакцій.
Реакції заміщення
Реакція заміщення, яка така ж, як і одна реакція заміщення в неорганічних реакціях, - це реакція, при якій один або кілька атомів в молекулі замінюються іншим атомом або групою атомів. Алкілгалогеніди утворюються шляхом заміщення атома галогену на атом водню. Коли метан вступає в реакцію з газом хлору, ультрафіолетове світло може виступати каталізатором реакції.
CH4(g)+Cl2(g)UV light→CH3Cl(g)+HCl(g)
В результаті реакції утворюється хлорометан і хлористий водень. Коли суміші дають вступати в реакцію протягом більш тривалих періодів часу, можуть виникнути подальші реакції заміщення.
CH3Cl(g)+Cl2(g)UV light→CH2Cl2(g)+HCl(g)
Вищевказаний продукт - дихлорметан. Далі продукти заміщення трихлорметаном і тетрахлорметаном, зазвичай називають тетрахлорметаном вуглецю. Суміш продуктів відбувається в реакції, причому відносні кількості залежать від часу, коли реакція дозволена протікати. Хлорфторуглеці виробляються шляхом взаємодії хлороалканів зHF, оскільки атом фтору робить більш міцний зв'язок з атомом вуглецю, ніж хлор.
CCl4(g)+HF(g)SbF5→CCl3F(g)+HCl(g)
Атом фтору замінює атом хлору в реакції.
Реакції ліквідації
Реакція елімінації передбачає видалення сусідніх атомів з молекули. Це призводить до утворення множинного зв'язку і вивільнення невеликої молекули, тому їх називають реакціями елімінації. Вони мають загальну форму.

Типовим прикладом є перетворення етилхлориду в етилен:
CH3CH2Cl→CH2=CH2+HCl
Значна частина приблизно 26 мільйонів тонн етилену, виробленого на рік у Сполучених Штатах, використовується для синтезу пластмас, таких як поліетилен. У вищезгаданій реакції усунена молекула A—B є HCl, компоненти якої вилучаються як H + з атома вуглецю зліва та Cl - з вуглецю праворуч. Коли кислота виробляється, як це відбувається тут, реакція, як правило, проводиться в присутності основи (наприклад, NaOH) для нейтралізації кислоти. Інші реакції елімінації спричинятимуть H 2, X 2 (де X = галоген) або H 2 O. Ці реакції часто називають більш описовими термінами, такими як дегідрування (видалення водню) або дехлорування (видалення хлору).
Реакції на додавання
Реакція додавання - це реакція, при якій атом або молекула додається до ненасиченої молекулі, утворюючи єдиний продукт. Реакцію додавання часто можна розглядати як додавання молекули через подвійний зв'язок алкена або через потрійний зв'язок алкіну. Знаючи, що «ація» означає додати, конкретні назви цих реакцій, такі як гідрування, гідратація або хлорування, повинні мати сенс. Зверніть увагу, що гідрування (додавання Н 2) і гідратація (додавання Н 2 О) - це дуже різні процеси.
Один з видів реакції приєднання називається гідрування. Гідрування - це реакція, яка виникає, коли молекулярний водень додається до алкену для отримання алкану або водень додається до алкіну для отримання алкена або алкану. Реакція зазвичай виконується з використанням каталізатора перехідного металу. Наприклад, етин вступає в реакцію з воднем з утворенням етану.
CH2=CH2(g)+H2(g)Pt→CH3CH3(g)
Зверніть увагу, що реакція гідрування також є окислювально-відновною реакцією. Етен зменшується, тому що кількість окислення атомів вуглецю змінюється від−2 до в−3 результаті реакції.
Рослинні масла складаються з довгих вуглецевих ланцюгів з карбоксильними групами на кінці; ці молекули іменуються жирними кислотами. Вуглецеві ланцюги жирних кислот в рослинних оліях ненасичені, зазвичай містять множинні подвійні зв'язки. Коли газ водню продувається через зразок нафти, атоми водню додають через подвійні зв'язки. Це перетворення перетворює речовину з рідкого масла в твердий жир. «Гідрогенізований» на харчовому продукті є свідченням того, що масло (рідина) за допомогою цього процесу було перетворено в жир (твердий). Маргарин виготовляється з ненасиченої рослинної олії таким чином шляхом гідрогенізації деяких подвійних зв'язків, що робить його «частково гідрогенізованим рослинним маслом».
Реакції приєднання також є корисними способами введення нової функціональної групи в органічну молекулу. Алкілгалогеніди можуть бути отримані з алкену шляхом додавання або елементарного галогену або галогеніду водню. Монозаміщений алкілгалогенід може бути отриманий шляхом додавання галогеніду водню до алкену. Нижче показано утворення хлоретану.
CH2=CH2(g)+HCl(g)→CH3CH2Cl(g)
Коли реагентом є двоатомний галоген, продукт є двозаміщеним алкілгалогенідом, як на додаванні брому до етена.
CH2=CH2(g)+Br2(l)→CH2BrCH2Br(g)
Додавання брому до невідомого органічної сполуки може бути використано в якості тесту на ненасичення в з'єднанні. Бром має характерний коричнево-оранжевий колір, в той час як більшість бромоалканів безбарвні. Коли бром повільно додається до розчину сполуки, помаранчевий колір буде тьмяніти, якщо він піддається реакції додавання, щоб отримати алкілгалогенід. Якщо залишився помаранчевий колір, значить, вихідне з'єднання вже було насиченим, і ніякої реакції не відбулося.
Реакція гідратації - це реакція, при якій до алкену додається вода. Реакції гідратації можуть відбуватися, коли алкен і вода нагріваються майже100oC в присутності сильної кислоти, яка виступає каталізатором. Нижче показано гідратацію етену для отримання етанолу.
CH2=CH2(g)+H2O(l)→CH3CH2OH(g)
На відміну від реакцій додаванняBr2, що включаютьH2 або, додавання води може мати два можливі продукти, тому що an−H і an−OH додаються до вуглецю в подвійному зв'язку. Правило Марковникова допомагає передбачити основний продукт в реакції гідратації. Правило стверджує, що атом водню з води додасть до вуглецю, який спочатку мав більше атомів водню. Наприклад, подивіться на гідратацію 1-бутену.
Зауважимо, що перший вуглець в 1-бутені починався з двох атомів водню, а другий вуглець починався з одного водню. Тому водень з води додає до першого вуглецю, а−OH група додає до другої вуглецю. Коли на обох вуглеводах є однакова кількість атомів водню в подвійному зв'язку, то два продукти утворюватимуться приблизно в рівних кількостях. Наприклад, гідратація 2-пентену призводить до отримання двох продуктів. У першому продукті−OH група знаходиться на третьому вуглеці, а в другому продукті−OH група знаходиться на другому вуглеці. Хоча ці дві молекули матимуть схожі властивості, будуть відмінності.
Реакції конденсації
Реакція конденсації - це реакція, в якій дві молекули об'єднуються, утворюючи єдину молекулу. Невелика молекула, часто вода, зазвичай видаляється під час реакції конденсації. Амінокислоти - важливі біологічні молекули, які мають амінну функціональну групу на одному кінці молекули і функціональну групу карбонової кислоти на іншому кінці. Коли дві амінокислоти об'єднуються в реакції конденсації, між амінним азотом однієї амінокислоти і карбоксильним вуглецем другої амінокислоти утворюється ковалентний зв'язок. Потім молекула води видаляється як другий продукт (див. Малюнок нижче).

Ця реакція утворює молекулу, звану дипептидом, а отриманий вуглець-азот ковалентний зв'язок часто називають пептидним зв'язком. При багаторазовому повторенні в кінцевому підсумку виробляється довга молекула, яка називається білком.
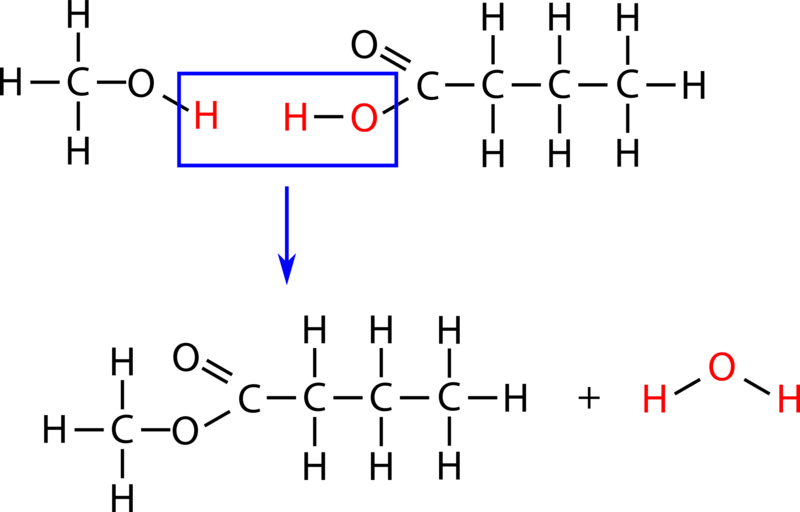
Етерифікація - це реакція конденсації, при якій з спирту і карбонової кислоти утворюється складний ефір. Етерифікація є підкатегорією реакцій конденсації, оскільки молекула води утворюється в реакції. Реакцію може каталізувати сильна кислота, як правило, сірчана кислота. При нагріванні карбонової кислоти, бутанової кислоти з надлишком метанолу і декількох крапель сірчаної кислоти, утворюється ефір метилбутаноат. Метилбутаноат має аромат ананасів. Реакція показана нижче як з молекулярними, так і структурними формулами. Реакції етерифікації оборотні.
CH3CH2CH2COOH+HOCH3H2SO4→CH3CH2CH2COOCH3+H2O
Омилення описує реакцію лужного гідролізу ефіру. Термін омилення спочатку описував гідроліз довголанцюгових ефірів, які називаються ефірами жирних кислот для отримання молекул мила, які є солями жирних кислот. Однією з таких молекул мила є стеарат натрію, що утворюється в результаті гідролізу етилстеарата.
C17H35COOC2H5+NaOH→C17H35COO−Na++C2H5OHethyl stearatesodium stearate (soap)
Реакції гідролізу
Гідроліз - зворотний процес конденсації. «Гідро» вказує на те, що вода бере участь і «лізис» означає розпастися. У реакції гідролізу додається вода і молекула розпадається, як правило, приC−O−C зв'язці.
Полімеризація
Полімери сильно відрізняються від інших видів органічних молекул, які ви бачили досі. Тоді як інші сполуки мають відносно низьку молярну масу, полімери - гігантські молекули дуже високої молярної маси. Полімери є первинними компонентами всіляких пластмас і споріднених сполук. Полімер - це велика молекула, утворена з багатьох менших молекул, ковалентно пов'язаних один з одним повторюваним малюнком. Дрібні молекули, що входять до складу полімеру, називаються мономерами. Полімери, як правило, утворюються реакціями додавання або конденсації. Тефлон (див. Малюнок нижче) - це нереактивне антипригарне покриття, яке використовується на посуді, а також в контейнерах і трубах для реактивних або агресивних хімічних речовин.