1.2: Стани матерії
- Page ID
- 21762
Цілі навчання
- Описати тверду, рідку та газову фази речовини.
Вода може приймати різні форми. При низьких температурах (нижче\(0^\text{o} \text{C}\)) він являє собою тверду речовину. Коли при «нормальних» температурах (між\(0^\text{o} \text{C}\) і\(100^\text{o} \text{C}\)), це рідина. У той час як при температурі вище\(100^\text{o} \text{C}\), вода є газом (парою). Стан, в якому знаходиться вода, залежить від температури. Кожен стан (тверде, рідке, газове) має свій унікальний набір фізичних властивостей.



Матерія зазвичай існує в одному з трьох станів: твердому, рідкому або газовому, і ці різні стани речовини мають різні властивості (Таблиця\(\PageIndex{1}\)):
- Газ - це стан речовини, в якому атоми або молекули мають достатньо енергії, щоб вільно рухатися. Молекули контактують один з одним лише тоді, коли вони випадковим чином стикаються. Сили між атомами або молекулами недостатньо сильні, щоб утримувати їх разом.
- Рідина - це стан речовини, в якому атоми або молекули постійно контактують, але мають достатньо енергії, щоб продовжувати змінювати положення відносно один одного. Сили між атомами або молекулами досить сильні, щоб зберегти молекули відносно близько один до одного, але недостатньо сильні, щоб запобігти їх переміщенню один одного.
- Тверде тіло - це стан речовини, в якому атомам або молекулам не вистачає енергії для переміщення. Вони постійно знаходяться в контакті і в фіксованих положеннях відносно один одного. Сили між атомами або молекулами досить сильні, щоб зберегти молекули разом і не дати їм рухатися повз один одного.
Держава, яку експонує дана речовина, є фізичною властивістю. Деякі речовини існують у вигляді газів кімнатної температури (кисень і вуглекислий газ), а інші, як вода і ртутний метал, існують у вигляді рідин. Більшість металів існують як тверді речовини при кімнатній температурі. Всі речовини можуть існувати в будь-якому з цих трьох станів. \(\PageIndex{2}\)На малюнку показані відмінності між твердими речовинами, рідинами та газами на молекулярному рівні. Тверда речовина має певний обсяг і форму, рідина має певний обсяг, але не визначену форму, а газ не має ні певного обсягу, ні форми (табл.\(\PageIndex{1}\)).
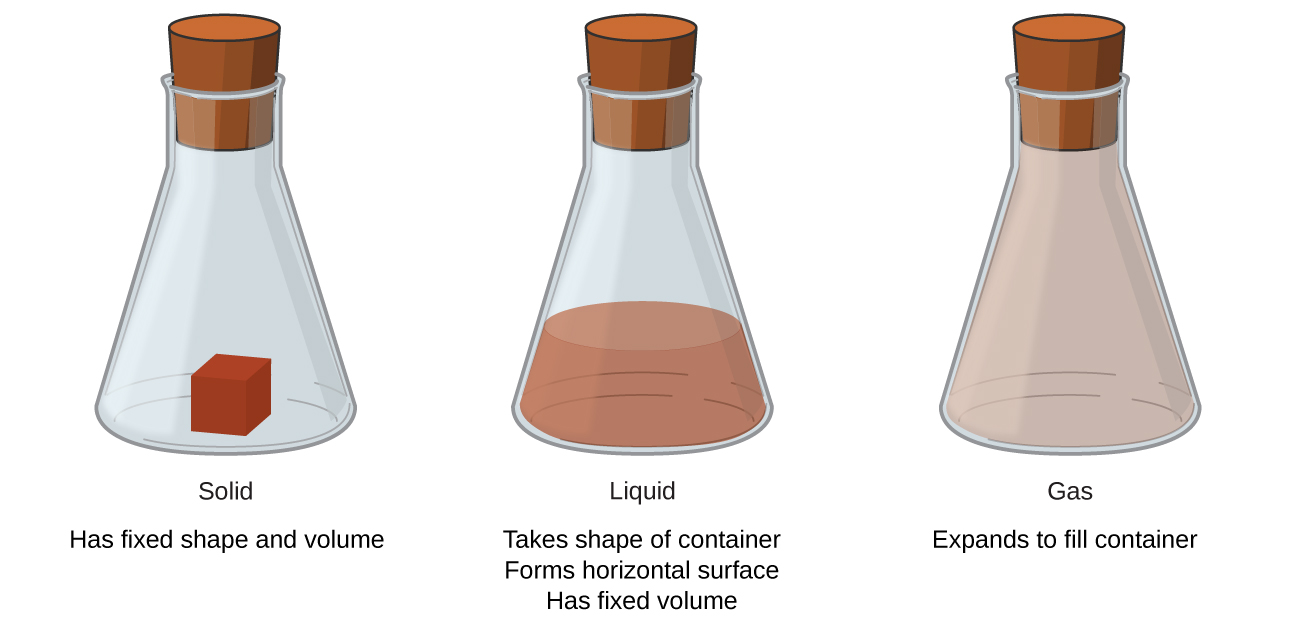
Ці три описи мають на увазі, що речовина має певні фізичні властивості, коли в цих станах. Тверда речовина має певну форму і певний обсяг. Рідини зазвичай мають певний обсяг, але не певну форму; вони приймають форму своїх контейнерів. Гази не мають ні певної форми, ні певного обсягу, і вони розширюються, щоб заповнити свої ємності. Ми стикаємося з матерією на кожній фазі щодня; насправді ми регулярно стикаємося з водою у всіх трьох фазах: лід (тверда), вода (рідина) та пара (газ).
| Газ | Рідина | Тверді | |
|---|---|---|---|
|
Форма |
немає певної форми (приймає форму свого контейнера) |
немає певної форми (приймає форму свого контейнера) |
певна форма (жорстка) |
|
Обсяг |
частинки рухаються у випадковому русі з невеликим або зовсім відсутнім потягом один до одного |
має певний обсяг |
певний обсяг |
|
Мобільність |
частинки рухаються у випадковому русі з невеликим або зовсім відсутнім потягом один до одного |
частинки вільно переміщаються один над одним, але все одно притягуються один до одного |
частинки вібрують навколо нерухомих осей |
|
стисливість |
високо стисливий |
слабо стисливий |
слабо стисливий |
Додавання енергії до речовини дає її атомам або молекулам здатність протистояти деяким силам, що тримають їх разом. Наприклад, нагрівання льоду до температури плавлення дає його молекулам достатньо енергії для переміщення. Лід тане і стає рідкою водою. Аналогічно, нагрівання рідкої води до температури кипіння дає її молекулам достатньо енергії, щоб витягнути один від одного, щоб вони більше не мали контакту. Рідина вода випаровується і стає водяною парою.
Стан речовини залежить від зовнішніх умов
Температура плавлення і кипіння залежать від ідентичності речовини і атмосферного тиску. Кожна речовина має свої температури кипіння і плавлення, які залежать від властивостей речовини. Як приклад значення для води наведені в табл\(\PageIndex{2}\). Зверніть увагу, як температура кипіння води сильно змінюється в залежності від тиску.
| Висота над рівнем моря (ft) | Тиск (атм) | Температура кипіння (o C) |
|---|---|---|
| -500 | 1.05 | 100.5 |
| 0 | 1.00 | 100 |
| 4000 | 0,892 | 96 |
| 7000 | 0.797 | 93 |
Приклад\(\PageIndex{1}\)
Ізопропіловий спирт - безбарвне, легкозаймиста хімічна сполука з сильним запахом. Його температура плавлення становить -89° C, а температура кипіння 82,5° C. ізопропіловий спирт твердим, рідким або газом при кімнатній температурі (25° C).
Рішення
Оскільки кімнатна температура (25° C) вище температури плавлення ізопропілового спирту (-89° C), але нижча за температуру кипіння (82,5° C), це рідина кімнатної температури.
Вправа\(\PageIndex{1}\)
Фреон-12 використовується в якості холодоагенту і аерозольного розпилювача палива. Його температура плавлення становить -157,7° C, а температура кипіння -29,8° C. ізопропіловий спирт твердим, рідким або газом при кімнатній температурі (25° C).
- Відповідь
-
Фреон-12 - газ кімнатної температури