2.2: Субатомні частинки та сучасний погляд на атом
- Page ID
- 25394
Атоми складаються з фундаментальних субатомних частинок: електронів, протонів і нейтронів.
Електрон був першою відкритою субатомною частинкою. Відкриття електронів пов'язане з вивченням катодних променів і базовими знаннями зарядів, тобто існує два типи зарядів +ve і —ve; подібні заряди відштовхують один одного; протилежні заряди притягують один одного, як показано на рис. 2.2.1; електричне і магнітне поле відхиляє рухомі заряди.
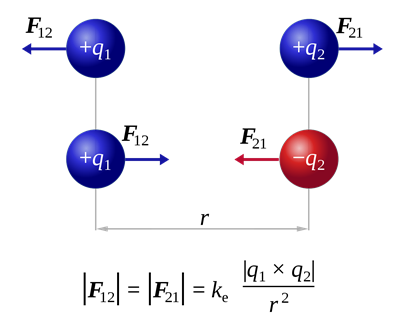
Відкриття електрона
катодні промені
Катодні промені - це вид випромінювання, що випромінюється від катода (негативно зарядженого електрода) при накладенні на пару електродів високого електричного поля в умовах зниженого тиску, як показано на рис. 2.2.2. Катодні промені рухаються в міжелектродному просторі. Якщо в аноді є отвір, катодні промені можуть проходити через отвір і продовжувати рухатися прямим шляхом. Катодні промені випромінюють світло, коли вони вдаряють по люмінесцентному екрану.
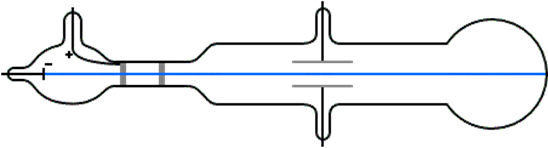
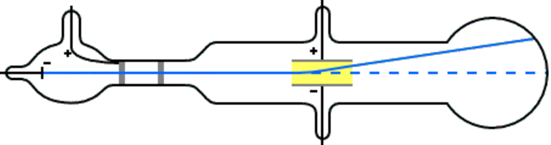
Експерименти Джей Джей Томсона -відкриття електронів
Джей Томсон вивчив катодні промені і виявив, що електричне поле відхиляє катодні промені в бік позитивного електрода. Це спостереження вказує на те, що катодні промені були негативними зарядами. Зміна матеріалу катода не змінила властивостей катодних променів. Дж. Томсон зробив висновок з цих спостережень, що катодні промені представляли собою потоки частинок, званих електронами, які присутні в атомах всіх елементів.
Подальші відкриття виявили, що заряд на електрони становить 1,602 х 10 -19 С, а їх маса становить 9,10 х 10 -28 м Електрони неймовірно легкі, приблизно в дві тисячі разів легше найлегшого атома.
Сливовий пудинг Модель атома
Виходячи з інформації електронно-променевих експериментів, Джей Джей Томсон дійшов висновку, що існують —ve зарядні електрони та речовин+ve, що представляють майже всю масу атома. Він запропонував сливово-пудингову модель атомів, тобто позитивна речовина схожа на розсіяне хмара або желе, яке займає простір атома, а електрони вбудовані в нього як фрукти в желе у випадку зі сливово-пудинговим десертним стравою, як показано на рис. 2.2.3.

Відкриття ядра атома
\({\alpha}\)-Промені
\({\alpha}\)-Промені, виражені як альфа-промені, є високоенергетичними випромінюваннями, що випромінюються з деяких радіоактивних джерел. The\({\alpha}\) -промені складаються з\({\alpha}\) -частинок, які є атомами гелію без будь-яких електронів.
Експеримент Резерфорда із золотої фольги -відкриття ядра
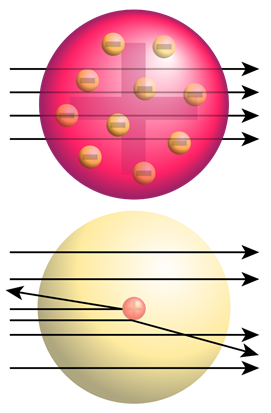
Резерфорд випробував модель атома сливового пудингу, бомбардуючи\({\alpha}\) -промені на тонкій золотій фользі. Він очікував, що\({\alpha}\) -частинки пройдуть через золоту фольгу, не відхилені, як кулі, випущені через лист пінопласту. Він зауважив, що хоча більшість\({\alpha}\) -частинок пройшли через золоту фольгу невідхилені, одна в ~ 20 000 відхилена під більшими кутами, як показано на рис. 2.2.4.
Оскільки модель сливи пудингу атома не могла пояснити відхилення\({\alpha}\) -частинок, Резерфорд зробив висновок, що в центрі атома є крихітна, але дуже щільна область, яка тепер називається ядром, яка\({\alpha}\) відхиляла частинки. Експеримент Резерфорда із золотої фольги призвів до відкриття ядра.
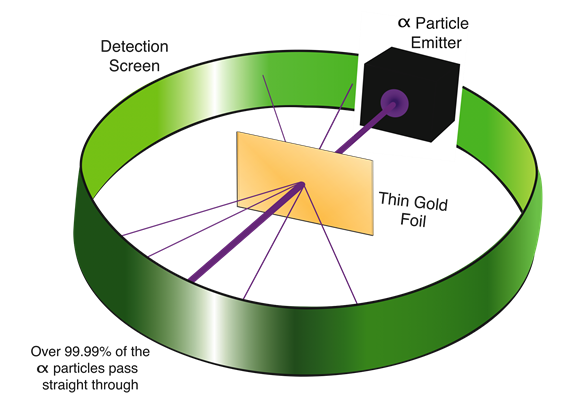
відкриття протона
Резерфорд передбачив, що позитивно заряджена фундаментальна частка атомів повинна перебувати в ядрі. Пізніше Резерфорд зауважив, що сяючі\({\alpha}\) промені на газі азоту утворюють позитивно заряджені частинки, звані протонами. Протони приблизно в 20 000 разів важчі за електрони, але несуть заряд +ve, рівний за величиною заряду —ve на електроні.
Відкриття нейтрона
Маса протонів і електронів не враховувала загальну масу атома, що призвело до пошуку іншої субатомної частинки. Джеймс Чедвік виявив, що бомбардування\({\alpha}\) -променів по мішені берилію виробляло високопроникаюче випромінювання, що складається з пучка нейтральних частинок, тепер званих нейтронами. Наявність нейтронів в ядрі припадає на відсутню масу атомів.
Були виявлені інші субатомні частинки, наприклад, кварки, які складають протони та нейтрони, але їх знання не є критичними для розуміння базової хімії.
Сучасний погляд на атом
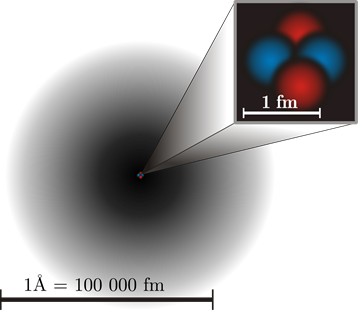
Протони і нейтрони мешкають в ядрі діаметром 10 -15 м Електрони займають область поза ядра діаметром 10 -10 м, як показано на рис.2.2.5. Якщо ядро розміром приблизно з мармур, атом був би розміром з футбольне поле.
Властивості субатомних частинок
Основні одиниці SI маси, електричного заряду та відстані занадто великі для вимірювання атомної шкали. Для цього визначаються нові одиниці, тобто:
Атомна одиниця маси (amu), яка становить 1/12 маси одного атома вуглецю, який має в ньому 6 протонів і 6 нейтронів.
\[1 \mathrm{~amu}=1.660539606660(50) \times 10^{-27} \mathrm{~kg}\nonumber\]
Заряд на одному електроні - це електронний заряд (е). \[1 ~e=1.602176634 \times 10^{-19} \mathrm{~C}\nonumber\]
1 Å = 10 -10 м
Ці одиниці зазвичай використовуються для мас, зарядів і діаметрів атомів. У таблиці 1 наведені основні властивості субатомних частинок.
|
Частинка |
Заряд (е) |
Маса (аму) |
|---|---|---|
|
Протон |
+1 |
1,0073 |
|
Нейтронний |
0 |
1.0078 |
|
Електрон |
-1 |
5,486 х 10 -4 |
Як субатомні частинки утримуються в атомі
Гравітаційна сила незначна у випадку поведінки субатомних частинок в атомах. Хоча електрони відштовхують інші електрони, вони залишаються в крихітному просторі через тяжіння до ядра. Аналогічно протони відштовхуються один одного, але електрична сила невелика в порівнянні з сильною ядерною силою, яка утримує протони і нейтрони разом в ядрі.
