17.4: Розпізнавання збудників і фагоцитоз
- Page ID
- 3879
Цілі навчання
- Поясніть, як лейкоцити мігрують з периферичної крові в заражені
- Поясніть механізми, за якими лейкоцити розпізнають збудників
- Поясніть процес фагоцитозу і механізми, за допомогою яких фагоцити знищують і деградують хвороботворні мікроорганізми
Кілька типів клітин, розглянутих у попередньому розділі, можна описати як фагоцити - клітини, основною функцією яких є пошук, прийом всередину та знищення патогенів. Цей процес, званий фагоцитозом, вперше спостерігався у морських зірок в 1880-х роках лауреатом Нобелівської премії зоологом Іллею Мечникоффом (1845—1916), який здійснив зв'язок з лейкоцитами (WBC) у людини та інших тварин. У той час Пастер та інші вчені вважали, що WBC поширюють патогенні мікроорганізми, а не вбивають їх (що справедливо для деяких захворювань, таких як туберкульоз). Але в більшості випадків фагоцити забезпечують сильний, швидкий і ефективний захист від широкого спектру мікробів, роблячи їх критичним компонентом вродженого неспецифічного імунітету. У цьому розділі мова піде про механізми, за допомогою яких фагоцити здатні шукати, розпізнавати та знищувати патогенні мікроорганізми.
Екстравазація (діапедез) лейкоцитів
Деякі фагоцити - це лейкоцити (WBC), які в нормі циркулюють в крові. Для досягнення хвороботворних мікроорганізмів, розташованих в інфікованої тканини, лейкоцити повинні проходити крізь стінки дрібних капілярних кровоносних судин всередині тканин. Цей процес, званий екстравазацією, або діапедезом, ініціюється фактором комплементу С5а, а також цитокінами, що виділяються в безпосередній близькості резидентними макрофагами і клітинами тканин, що реагують на присутність інфекційного агента (рис.\(\PageIndex{1}\)). Подібно до C5a, багато з цих цитокінів є прозапальними і хемотаксичними, і вони зв'язуються з клітинами дрібних капілярних кровоносних судин, ініціюючи відповідь в ендотеліальних клітині, що вистилають внутрішню частину стінок кровоносних судин. Ця відповідь включає в себе регуляцію і експресію різних молекул клітинної адгезії і рецепторів. Лейкоцити, що проходять крізь, будуть злегка прилипати до молекул адгезії, сповільнюючись і перекочуючись по стінках кровоносних судин поблизу зараженої ділянки. Коли вони досягають клітинного з'єднання, вони зв'язуються з ще більшою кількістю цих молекул адгезії, сплющуючись і стискаючись через клітинний спай у процесі, відомому як трансендотеліальна міграція. Цей механізм «згортання адгезії» дозволяє лейкоцитам вийти з кровоносного русла і потрапляти в заражені ділянки, де вони можуть почати фагоцитозування вторглися збудників.
Зверніть увагу, що екстравазація не відбувається в артеріях або венах. Ці кровоносні судини оточені більш товстими багатошаровими захисними стінками, на відміну від тонких одноклітинних стінок капілярів. Крім того, кровотік в артеріях занадто турбулентний, щоб забезпечити зчеплення кочення. Також деякі лейкоцити, як правило, реагують на інфекцію швидше, ніж інші. Першими, хто прибуває, як правило, є нейтрофіли, часто протягом декількох годин після бактеріальної інфекції. За контрактом моноцитам може знадобитися кілька днів, щоб покинути кровотік і диференціюватися на макрофаги.
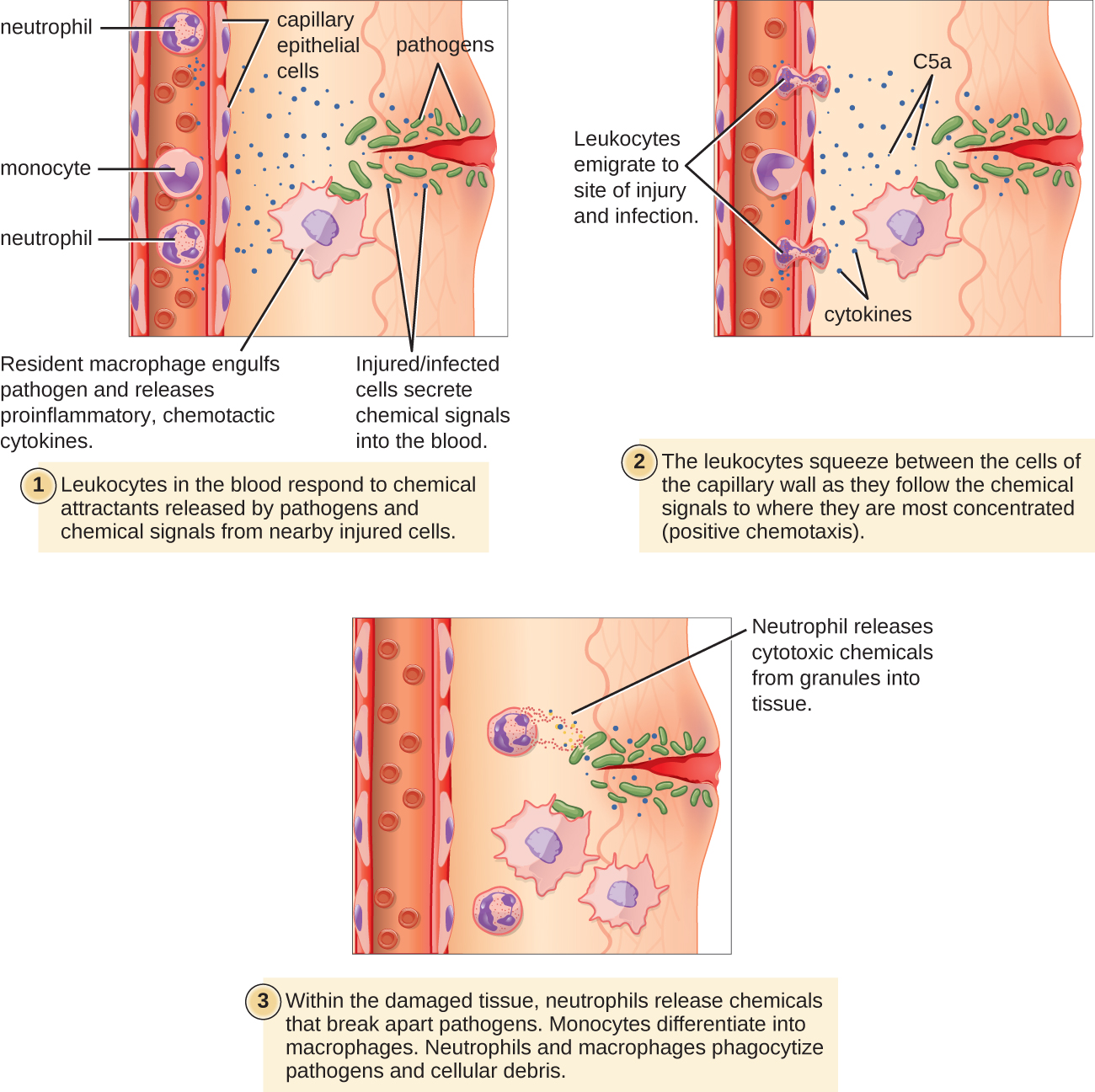
Перегляньте наступні відео про екстравазацію лейкоцитів та прокатки лейкоцитів, щоб дізнатися більше.
Вправа\(\PageIndex{1}\)
Поясніть роль молекул адгезії в процесі екстравазації.
Розпізнавання збудників
Як описано в попередньому розділі, опсонізація патогенів антитілами; фактори комплементу C1q, C3b та C4b; і лектини можуть допомогти фагоцитарним клітинам у розпізнаванні патогенів та приєднанні до початку фагоцитозу. Однак не всі розпізнавання збудників залежать від опсоніна. Фагоцити також можуть розпізнавати молекулярні структури, які є загальними для багатьох груп патогенних мікробів. Такі структури називаються патогенасоційованими молекулярними паттернами (ПАМПа). Загальні ПАМПи включають в себе наступне:
- пептидоглікан, виявлений в клітинних стінках бактерій;
- джгутики, білок, виявлений в бактеріальних джгутиках;
- ліпополісахарид (ЛПС) із зовнішньої мембрани грамнегативних бактерій;
- ліпопептиди, молекули, виражені більшістю бактерій; і
- нуклеїнові кислоти, такі як вірусна ДНК або РНК.
Як і численні інші ПАМПи, ці речовини є невід'ємною частиною структури широких класів мікробів.
Структури, що дозволяють фагоцитарним клітинам виявляти PAMP, називаються рецепторами розпізнавання образів (PRR). Однією з груп PRR є toll-подібні рецептори (TLR), які зв'язуються з різними PAMP і спілкуються з ядром фагоцита, щоб викликати відповідь. Багато ТЛР (та інші ПРР) розташовані на поверхні фагоцита, але деякі також можуть бути знайдені вбудованими в мембрани внутрішніх відділень і органел (рис.\(\PageIndex{2}\)). Ці внутрішні PRR можуть бути корисними для зв'язування та розпізнавання внутрішньоклітинних патогенів, які, можливо, отримали доступ до внутрішньої частини клітини до фагоцитозу. Наприклад, вірусні нуклеїнові кислоти можуть зіткнутися з внутрішнім PRR, викликаючи вироблення противірусного цитокінового інтерферону.
Крім забезпечення першого кроку розпізнавання збудника, взаємодія між ПАМПС і ПРР на макрофагах забезпечує внутрішньоклітинний сигнал, який активує фагоцит, викликаючи його перехід з сплячого стану готовності і повільної проліферації до стану гіперактивності, проліферації, вироблення/секреція цитокінів та посилене внутрішньоклітинне вбивство. PRR на макрофагах також реагують на хімічні сигнали лиха від пошкоджених або напружених клітин. Це дозволяє макрофагам поширювати свої реакції за межі захисту від інфекційних захворювань на більш широку роль у запальній реакції, ініційованої внаслідок травм або інших захворювань.
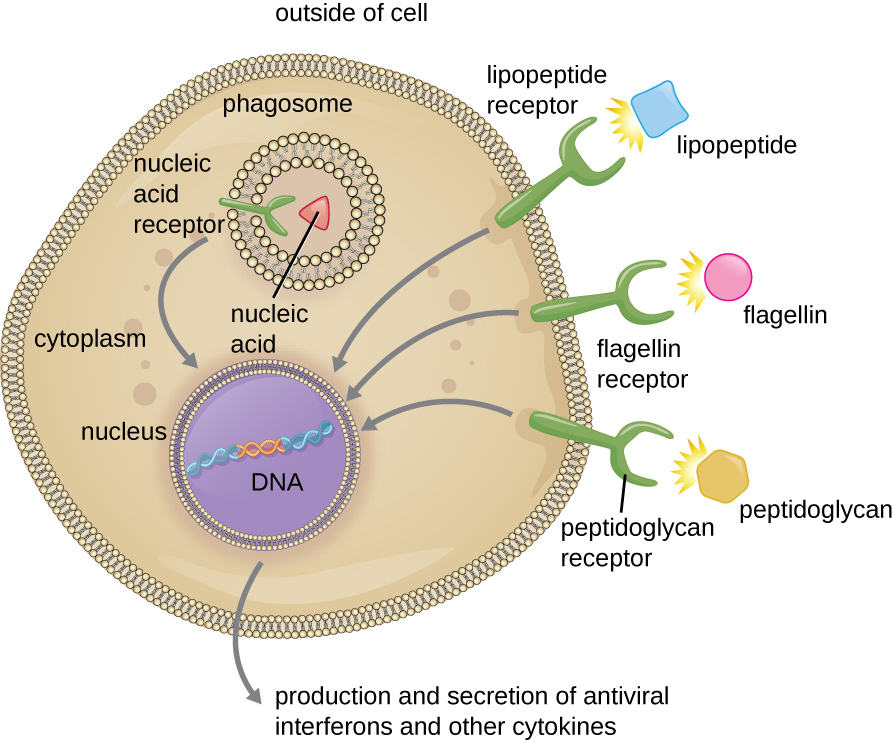
Вправа\(\PageIndex{2}\)
- Назвіть чотири асоційовані патогеном молекулярні моделі (ПАМПи).
- Опишіть процес активації фагоцитів.
Деградація збудника
Як тільки відбувається розпізнавання і приєднання збудника, збудник поглинається везикулою і заноситься у внутрішній відсік фагоцита в процесі, званому фагоцитозом (рис.\(\PageIndex{3}\)). PRR можуть допомогти при фагоцитозі, спочатку зв'язуючись з поверхнею збудника, але фагоцити також здатні охопити прилеглі предмети, навіть якщо вони не пов'язані з конкретними рецепторами. Щоб поглинути збудника, фагоцит утворює псевдопод, який обертається навколо збудника, а потім відщипує його в мембранну везикулу, звану фагосомою. Підкислення фагосоми (рН знижується до діапазону 4-5) забезпечує важливий ранній антибактеріальний механізм. Фагосома, що містить збудника, зливається з однією або декількома лізосомами, утворюючи фаголізосому. Утворення фаголізосоми посилює підкислення, що має важливе значення для активації рН-залежних травних лізосомальних ферментів і вироблення пероксиду водню та токсичних активних форм кисню. Лізосомальні ферменти, такі як лізоцим, фосфоліпаза і протеази перетравлюють збудника. Інші ферменти беруть участь в дихальному сплеску. Під час респіраторного сплеску фагоцити будуть збільшувати їх поглинання і споживання кисню, але не для вироблення енергії. Підвищене споживання кисню орієнтовано на виробництво супероксидного аніону, пероксиду водню, гідроксильних радикалів та інших активних форм кисню, які є антибактеріальними.
На додаток до активних форм кисню, що утворюються дихальним сплеском, також можуть утворюватися реактивні сполуки азоту з цитотоксичним (вбивство клітин) потенціалом. Наприклад, оксид азоту може реагувати з супероксидом з утворенням пероксинітриту, високоактивної сполуки азоту з деструктивними можливостями, подібними до активних форм кисню. Деякі фагоцити навіть містять внутрішнє джерело мікробіцидних білків дефензину (наприклад, гранули нейтрофілів). Ці руйнівні сили можуть виділятися в область навколо клітини, щоб погіршити мікроби зовні. Нейтрофіли, особливо, можуть бути досить ефективними при цьому вторинному протимікробному механізмі.
Після завершення деградації залишки продуктів життєдіяльності виводяться з клітини в екзоцитарному бульбашку. Однак важливо відзначити, що не всі залишки збудника виводяться у вигляді відходів. Макрофаги та дендритні клітини також є антигенпрезентуючими клітинами, які беруть участь у специфічній адаптивній імунній відповіді. Ці клітини додатково обробляють залишки деградованого збудника і представляють ключові антигени (специфічні білки збудника) на їх клітинній поверхні. Це важливий крок для стимуляції деяких адаптивних імунних реакцій, про що буде розглянуто більш детально в наступному розділі.
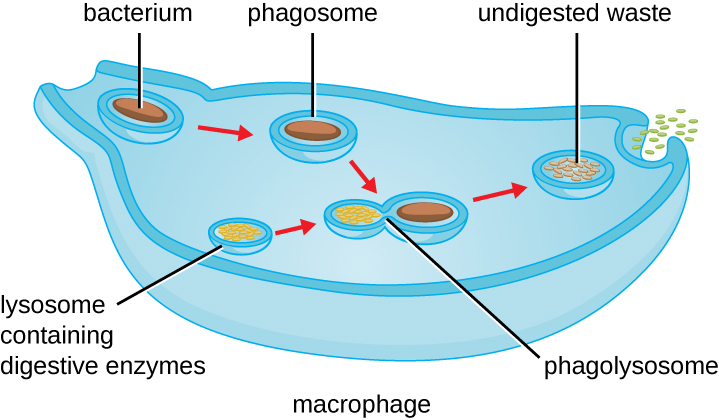
Відвідайте це посилання, щоб переглянути фагоцити, що переслідують і поглинають збудника.
Вправа\(\PageIndex{3}\)
У чому різниця між фагосомою і лізосомою?
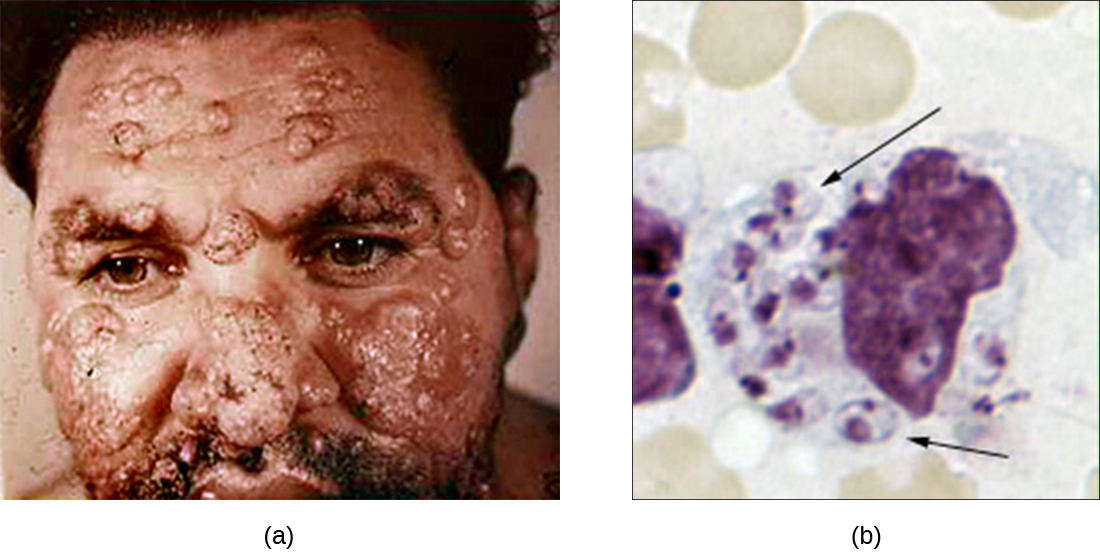
Хоча фагоцитоз успішно знищує багатьох патогенних мікроорганізмів, деякі здатні вижити і навіть експлуатувати цей захисний механізм, щоб розмножуватися в організмі і викликати поширену інфекцію. Найпростіші з роду Лейшманія - один із прикладів. Ці облігатні внутрішньоклітинні паразити являють собою джгутики, що передаються людині при укусі піщаної мухи. Інфекції викликають серйозні і іноді спотворюють виразки і виразки на шкірі та інших тканині (рис.\(\PageIndex{4}\)). У всьому світі приблизно 1,3 мільйона людей щороку заражаються лейшманіозом. 1
Слинні пептиди від піщаної мухи активізують макрофаги господаря в місці їх укусу. Класичний або альтернативний шлях активації комплементу відбувається з опсонізацією паразита C3b. Клітини лейшманії фагоцитозуються, втрачають свої джгутики і розмножуються у формі, відомій як амастігот (тіло Лейшмана-Донована) у фаголізосомі. Хоча багато інших збудників знищуються в фаголізосомі, виживання амастіготів Leishmania підтримується наявністю поверхневого ліпофосфоглікану і кислої фосфатази. Ці речовини пригнічують макрофаг респіраторний сплеск і лізосомальні ферменти. Потім паразит розмножується всередині клітини і лізує заражений макрофаг, звільняючи амастіготів для зараження інших макрофагів в межах одного господаря. Якщо інша піщана муха вкусить заражену людину, вона може проковтнути амастіготів, а потім передавати їх іншій особі через інший укус.
Існує кілька різних форм лейшманіозу. Найбільш поширеною є локалізована шкірна форма захворювання, спричинена L. tropica, яка, як правило, розсмоктується спонтанно з часом, але з деякою значною інфільтрацією лімфоцитів і постійним рубцюванням. Слизисто-шкірна форма захворювання, викликана L. viannia brasilienfsis, спричиняє ураження в тканині носа та рота і може бути небезпечною для життя. Вісцеральна форма хвороби може бути викликана декількома різними видами лейшманії. Він вражає різні системи органів і викликає аномальне збільшення печінки і селезінки. Нерегулярні лихоманки, анемія, дисфункція печінки та втрата ваги - все це ознаки та симптоми вісцерального лейшманіозу. Якщо не лікувати, це, як правило, смертельно.
Ключові поняття та резюме
- Фагоцити - це клітини, які розпізнають хвороботворні мікроорганізми і знищують їх за допомогою фагоцитозу.
- Розпізнавання часто відбувається за допомогою рецепторів фагоцитів, які зв'язують молекули, які зазвичай зустрічаються на патогенах, відомих як асоційовані з патогенами молекулярні моделі (ПАМПи).
- Рецептори, які зв'язують PAMP, називаються рецепторами розпізнавання образів, або PRR. Toll-подібні рецептори (TLR) - це один з типів PRR, виявлених на фагоцитах.
- Екстравазація лейкоцитів з кровотоку в інфіковану тканину відбувається через процес трансендотеліальної міграції.
- Фагоцити деградують збудників через фагоцитоз, який передбачає поглинання збудника, вбивство і перетравлення його всередині фаголізосоми, а потім виведення неперетравленої речовини.
Виноски
- 1 Всесвітня організація охорони здоров'я. «Лейшманіоз». 2016 рік. http://www.who.int/mediacentre/factsheets/fs375/en/.
