17.2: Хімічний захист
- Page ID
- 3874
Цілі навчання
- Опишіть, як ферменти в рідині організму забезпечують захист від інфекції або хвороб
- Перерахуйте та опишіть функцію антимікробних пептидів, компонентів комплементу, цитокінів та білків гострої фази
- Опишіть подібності та відмінності між класичними, альтернативними та лектиновими шляхами комплементу
Крім фізичних захисних сил, вроджена неспецифічна імунна система використовує ряд хімічних медіаторів, які пригнічують мікробних загарбників. Термін «хімічні медіатори» охоплює широкий спектр речовин, що містяться в різних рідинях організму і тканині по всьому тілу. Хімічні медіатори можуть працювати поодинці або спільно один з одним, щоб пригнічувати мікробну колонізацію та інфекцію.
Деякі хімічні медіатори виробляються ендогенно, тобто вони виробляються клітинами людського організму; інші виробляються екзогенно, що означає, що вони виробляються певними мікробами, що входять до складу мікробіома. Деякі медіатори виробляються постійно, купаючи область в антимікробній речовині; інші виробляються або активуються в першу чергу у відповідь на деякі подразники, такі як наявність мікробів.
Хімічні та ферментативні медіатори, знайдені в рідинях організму
Рідини, що виробляються шкірою, включають приклади як ендогенних, так і екзогенних медіаторів. Сальні залози в дермі виділяють масло, зване шкірним салом, яке виділяється на поверхню шкіри через волосяні фолікули. Це шкірне сало є ендогенним медіатором, забезпечуючи додатковий шар захисту, допомагаючи герметизувати пори волосяного фолікула, запобігаючи потраплянню бактерій на поверхні шкіри потових залоз і навколишніх тканин (рис.\(\PageIndex{1}\)). Деякі члени мікробіома, такі як бактерія Propionibacterium acnes та гриб Malassezia, серед інших, можуть використовувати ферменти ліпази для деградації шкірного сала, використовуючи його як джерело їжі. При цьому виробляється олеїнова кислота, яка створює на поверхні шкіри м'яко кисле середовище, непривітну для багатьох патогенних мікробів. Олеїнова кислота є прикладом екзогенно виробленого медіатора, оскільки вона виробляється резидентними мікробами, а не безпосередньо клітинами організму.
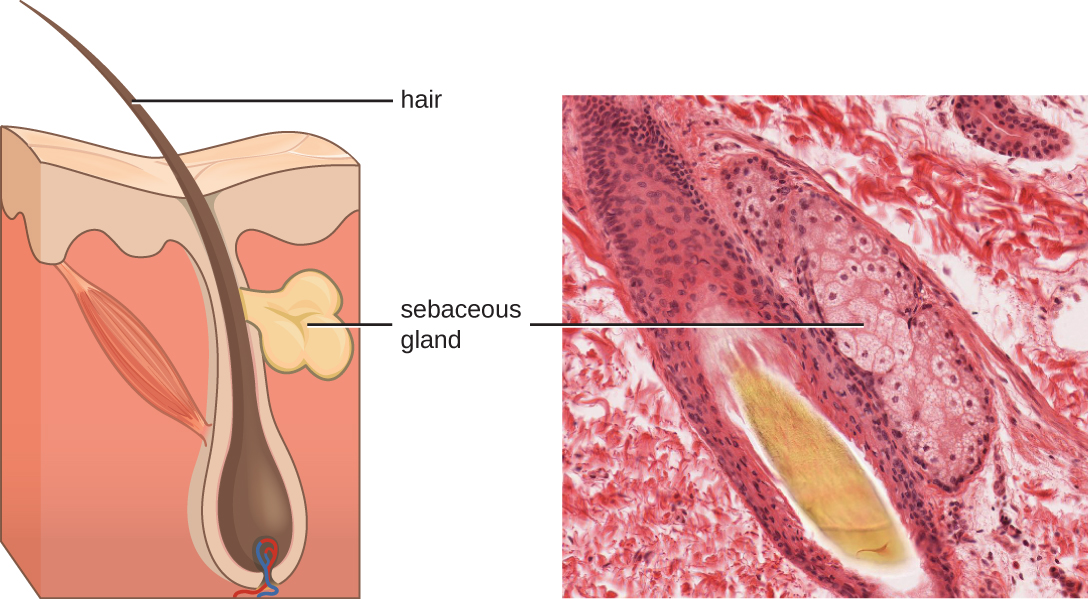
Фактори навколишнього середовища, що впливають на мікробіоту шкіри, можуть надавати прямий вплив на вироблення хімічних медіаторів. Наприклад, низька вологість або зниження вироблення шкірного сала можуть зробити шкіру менш придатною для життя мікробів, які виробляють олеїнову кислоту, тим самим роблячи шкіру більш сприйнятливою до патогенів, які зазвичай гальмуються низьким рН шкіри. Багато зволожуючих засобів для шкіри розроблені для протидії такому впливу шляхом відновлення вологи та ефірних масел для шкіри.
Травний тракт також виробляє велику кількість хімічних медіаторів, які пригнічують або вбивають мікроби. У ротовій порожнині слина містить такі медіатори, як ферменти лактопероксидази, а слиз, що виділяється стравоходом, містить антибактеріальний фермент лізоцим. У шлунку сильно кисла шлункова рідина вбиває більшість мікробів. У нижньому відділі травного тракту в кишечнику є панкреатичні і кишкові ферменти, антибактеріальні пептиди (криптини), жовч, що виробляється з печінки, і спеціалізовані клітини Панета, які виробляють лізоцим. У сукупності ці медіатори здатні усунути більшість хвороботворних мікроорганізмів, яким вдається пережити кисле середовище шлунка.
У сечовивідних шляхах сеча вимиває мікроби з організму під час сечовипускання. Крім того, незначна кислотність сечі (середній показник рН становить близько 6) гальмує ріст багатьох мікробів і потенційних збудників в сечовивідних шляхах.
Жіноча репродуктивна система використовує лактат, екзогенно вироблений хімічний медіатор, для пригнічення росту мікробів. Клітини і тканинні шари, що складають піхву, виробляють глікоген, розгалужений і більш складний полімер глюкози. Лактобактерії в цій області ферментують глікоген для вироблення лактату, знижуючи рН у піхві та пригнічуючи транзиторну мікробіоту, умовно-патогенні мікроорганізми, такі як Candida (дріжджі, пов'язані з вагінальними інфекціями) та інші патогени, відповідальні за захворювання, що передаються статевим шляхом.
В очах сльози містять хімічні медіатори лізоцим і лактоферин, обидва з яких здатні усунути мікроби, які знайшли собі шлях до поверхні очей. Лізоцим розщеплює зв'язок між NAG і NAM в пептидоглікані, компоненті клітинної стінки бактерій. Він більш ефективний проти грампозитивних бактерій, у яких відсутня захисна зовнішня мембрана, пов'язана з грамнегативними бактеріями. Лактоферин пригнічує ріст мікробів шляхом хімічного зв'язування та секвестеризації заліза. Це ефективно голодує багато мікробів, які потребують заліза для росту.
У вухах церумен (вушна сірка) проявляє антимікробні властивості завдяки наявності жирних кислот, які знижують рН до 3 і 5.
Дихальні шляхи використовують різні хімічні медіатори в носових ходах, трахеї, легенях. Слиз, що утворюється в носових ходах, містить суміш протимікробних молекул, подібних до тих, що містяться в сльозах і слині (наприклад, лізоцим, лактоферин, лактопероксидаза). Виділення в трахеї і легенях також містять лізоцим і лактоферин, а також різноманітну групу додаткових хімічних медіаторів, таких як комплекс ліпопротеїдів, званий сурфактантом, що володіє антибактеріальними властивостями.
Вправа\(\PageIndex{1}\)
- Поясніть різницю між ендогенними та екзогенними медіаторами
- Опишіть, як pH впливає на антимікробний захист
Антимікробні пептиди
Антимікробні пептиди (АМП) - це особливий клас неспецифічних клітинних медіаторів з антимікробними властивостями широкого спектру дії. Деякі АМП виробляються організмом регулярно, тоді як інші в основному виробляються (або виробляються у більшій кількості) у відповідь на наявність вторгнення збудника. Почалися дослідження, вивчаючи, як АМП можна використовувати в діагностиці та лікуванні захворювань.
АМП може індукувати пошкодження клітин у мікроорганізмів різними способами, включаючи пошкодження мембран, руйнуючи ДНК та РНК або втручаючись у синтез клітинної стінки. Залежно від конкретного антимікробного механізму, конкретний АМФ може інгібувати лише певні групи мікробів (наприклад, грампозитивні або грамнегативні бактерії) або може бути більш ефективним проти бактерій, грибів, найпростіших та вірусів. Багато АМП знаходяться на шкірі, але їх можна зустріти і в інших областях тіла.
Сімейство АМП, які називаються дефенсинами, може вироблятися епітеліальними клітинами по всьому тілу, а також клітинними захисними силами, такими як макрофаги та нейтрофіли (див. Клітинні захисні сили). Дефенсіни можуть секретуватися або діяти всередині клітин господаря; вони борються з мікроорганізмами, пошкоджуючи їх плазматичні мембрани. АМП, звані бактеріоцинами, виробляються екзогенно певними членами резидентної мікробіоти в шлунково-кишковому тракті. Гени, кодуючі для цих типів АМП, часто переносяться на плазмідах і можуть передаватися між різними видами всередині резидентної мікробіоти шляхом бічного або горизонтального перенесення генів.
Існують численні інші підсилювачі по всьому тілу. Характеристики декількох більш значущих підсилювачів зведені в табл\(\PageIndex{1}\).
| ПІДСИЛЮВАЧ | Секретується | Кузов сайту | Збудники інгібуються | Режим дії |
|---|---|---|---|---|
| Бактеріоцини | Резидентна мікробіота | шлунково-кишкового тракту | Бактерії | Порушити мембрану |
| кателіцидин | Епітеліальні клітини, макрофаги та інші типи клітин | Шкіра | Бактерії і грибки | Порушує мембрану |
| Дефенсінс | Епітеліальні клітини, макрофаги, нейтрофіли | По всьому тілу | Грибки, бактерії та багато вірусів | Порушити мембрану |
| Дерміцидин | потові залози | Шкіра | Бактерії і грибки | Порушує цілісність мембрани і іонні канали |
| Гістатини | слинні залози | Ротова порожнина | Гриби | Порушити внутрішньоклітинну функцію |
Вправа\(\PageIndex{2}\)
Чому антимікробні пептиди (АМП) вважаються неспецифічними захисними засобами?
Плазмові білкові медіатори
Багато неспецифічні вроджені імунні фактори знаходяться в плазмі, рідкій частині крові. Плазма містить електроліти, цукру, ліпіди та білки, кожен з яких допомагає підтримувати гомеостаз (тобто стабільне функціонування внутрішнього організму), а також містить білки, які беруть участь у згортанні крові. Додаткові білки, що містяться в плазмі крові, такі як білки гострої фази, білки комплементу та цитокіни, беруть участь у неспецифічній вродженій імунній відповіді.
Плазма проти сироватки
Існує два терміни для рідкої порції крові: плазма і сироватка. Чим вони відрізняються, якщо вони одночасно рідкі і не мають клітин? Рідина частина крові, що залишилася після згортання (згортання кров'яних клітин), є сироваткою крові. Хоча молекули, такі як багато вітамінів, електролітів, певних цукрів, білки комплементу та антитіла, все ще присутні в сироватці крові, фактори згортання в значній мірі виснажуються. Плазма, навпаки, ще містить всі елементи згортання. Для отримання плазми з крові необхідно використовувати антикоагулянт для запобігання згортання. Прикладами антикоагулянтів є гепарин і етилендіамін тетраоцтова кислота (ЕДТА). Оскільки згортання гальмується, після отримання зразок повинен бути обережно відкручений у центрифузі. Більш важкі, щільніші клітини крові утворюють гранулу на дні пробірки центрифуги, тоді як частина рідини плазми, яка легша і менш щільна, залишається над клітинною гранулою.
Білки гострої фази
Білки гострої фази - ще один клас антимікробних медіаторів. Білки гострої фази в основному виробляються в печінці і секретуються в кров у відповідь на запальні молекули з імунної системи. Приклади білків гострої фази включають С-реактивний білок, сироватковий амілоїд А, феритин, трансферин, фібриноген та лектин, що зв'язує маннозу. Кожен з цих білків має різну хімічну будову і якимось чином пригнічує або знищує мікроби (табл.\(\PageIndex{1}\)).
| Деякі білки гострої фази та їх функції | |
|---|---|
| С-реактивний білок | Бактерії Coats (опсонізація), готуючи їх до прийому фагоцитами |
| Амілоїд сироватки А | |
| Феритин | Зв'язують і секвеструють залізо, тим самим гальмуючи ріст хвороботворних мікроорганізмів |
| Трансферин | |
| Фібриноген | Бере участь в утворенні тромбів, які затримують бактеріальні збудники |
| Лектин, що зв'язує маннозу | Активує комплемент каскад |
Система доповнення
Система комплементу - це група медіаторів білків плазми, які можуть діяти як вроджений неспецифічний захист, а також служити для підключення вродженого та адаптивного імунітету (розглянуто в наступному розділі). Система комплементу складається з більш ніж 30 білків (включаючи C1 через C9), які зазвичай циркулюють як білки-попередники в крові. Ці білки-попередники активізуються при стимулюванні або спрацьовуванні різними факторами, включаючи наявність мікроорганізмів. Білки комплементу вважаються частиною вродженого неспецифічного імунітету, оскільки вони завжди присутні в крові та тканинних рідинях, що дозволяє їм швидко активуватися. Також при активації за допомогою альтернативного шляху (описаного далі в цьому розділі) білки комплементу націлені на патогени неспецифічним чином.
Процес, за допомогою якого циркулюючі попередники комплементу стають функціональними, називається активацією комплементу. Цей процес являє собою каскад, який може бути запущений одним з трьох різних механізмів, відомих як альтернативний, класичний та лектиновий шляхи.
Альтернативний шлях ініціюється спонтанною активацією білка комплементу С3. Гідроліз С3 виробляє два продукти, C3a і C3b. Коли мікробів загарбників немає, C3b дуже швидко деградує в реакції гідролізу, використовуючи воду в крові. Однак якщо присутні мікроби, що вторгаються, C3b прикріплюється до поверхні цих мікробів. Після приєднання C3b буде набирати інші білки комплементу в каскад (рис.\(\PageIndex{2}\)).
Класичний шлях забезпечує більш ефективний механізм активації каскаду комплементу, але він залежить від вироблення антитіл специфічними адаптивними імунними силами. Щоб ініціювати класичний шлях, специфічне антитіло повинно спочатку зв'язуватися зі збудником, утворюючи комплекс антитіло-антиген. Це активує перший білок в каскаді комплементу, комплекс С1. Комплекс С1 являє собою багатокомпонентний білковий комплекс, і кожен компонент бере участь в повній активації загального комплексу. Після набору і активації комплексу С1 решта класичного шляху протеїни комплементу набираються і активуються в каскадній послідовності (рис.\(\PageIndex{2}\)).
Шляхи активації лектину аналогічний класичному шляху, але він викликається зв'язуванням манноззв'язуючого лектину, білка гострої фази, з вуглеводами на мікробній поверхні. Як і інші білки гострої фази, лектини виробляються клітинами печінки і зазвичай регулюються у відповідь на запальні сигнали, отримані організмом під час інфекції (рис.\(\PageIndex{2}\)).
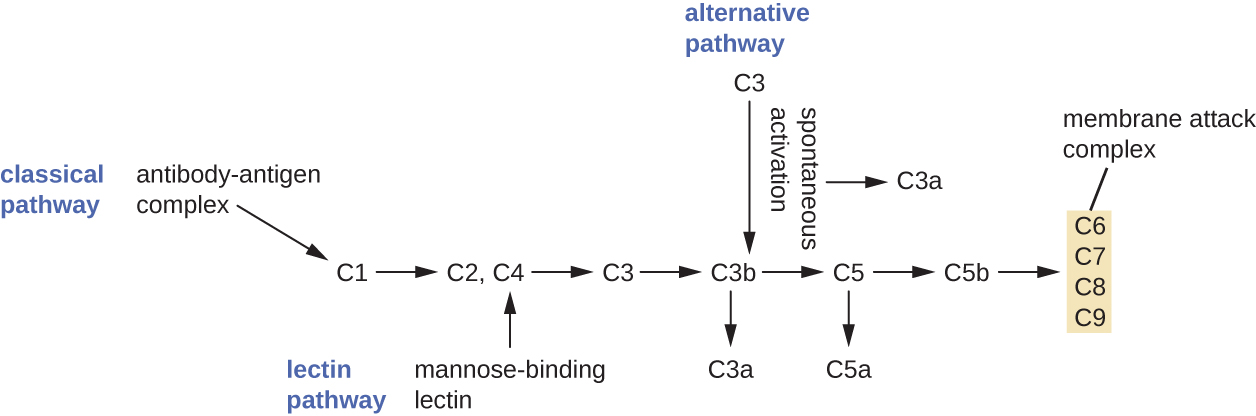
Хоча кожен шлях активації комплементу ініціюється по-різному, всі вони забезпечують однакові захисні результати: опсонізація, запалення, хемотаксис та цитоліз. Термін опсонізація відноситься до покриття збудника хімічною речовиною (називається опсоніном), що дозволяє фагоцитарним клітинам легше розпізнавати, поглинати та знищувати його. Опсоніни з комплементу каскаду включають C1q, C3b і C4b. Додаткові важливі опсоніни включають манноззв'язуючі білки і антитіла. Фрагменти комплементу C3a і C5a добре характеризуються анафілатоксинами з потужними прозапальними функціями. Анафілатоксини активують огрядні клітини, викликаючи дегрануляцію і вивільнення запальних хімічних сигналів, включаючи медіатори, що викликають розширення судин і підвищення проникності судин. C5a також є одним з найпотужніших хемоатрактантів для нейтрофілів та інших лейкоцитів, клітинних захисних сил, які будуть розглянуті в наступному розділі.
Білки комплементу С6, С7, С8 і С9 збираються в мембранний комплекс атаки (MAC), що дозволяє С9 полімеризуватися в пори в мембранах грамнегативних бактерій. Ці пори дозволяють воді, іонам та іншим молекулам вільно переміщатися всередину та виходити з цільових клітин, що в кінцевому підсумку призводить до лізису клітин і загибелі збудника (рис.\(\PageIndex{2}\)). Однак ГДК ефективний лише проти грамнегативних бактерій; він не може проникнути в товстий шар пептидоглікану, пов'язаного з клітинними стінками грампозитивних бактерій. Оскільки ГДК не представляє смертельної загрози для грампозитивних бактеріальних збудників, опосередкована комплементом опсонізація важливіша для їх очищення.
цитокіни
Цитокіни - це розчинні білки, які діють як сигнали зв'язку між клітинами. При неспецифічній вродженій імунній відповіді можуть виділятися різні цитокіни для стимуляції вироблення хімічних медіаторів або інших функцій клітин, таких як проліферація клітин, диференціація клітин, пригнічення поділу клітин, апоптоз та хемотаксис.
Коли цитокін зв'язується зі своїм рецептором-мішенню, ефект може сильно варіюватися залежно від типу цитокіну та типу клітини або рецептора, до якого він зв'язався. Функція конкретного цитокіну може бути описана як аутокринна, паракринна або ендокринна (рис.\(\PageIndex{3}\)). У аутокринній функції одна і та ж клітина, яка вивільняє цитокін, є реципієнтом сигналу; іншими словами, аутокринна функція є формою самостимуляції клітиною. На відміну від цього, паракринна функція передбачає вивільнення цитокінів з однієї клітини в інші сусідні клітини, стимулюючи деяку реакцію від клітин реципієнтів. Нарешті, ендокринна функція виникає, коли клітини вивільняють цитокіни в кров, які переносяться до клітини-мішеней набагато далі.
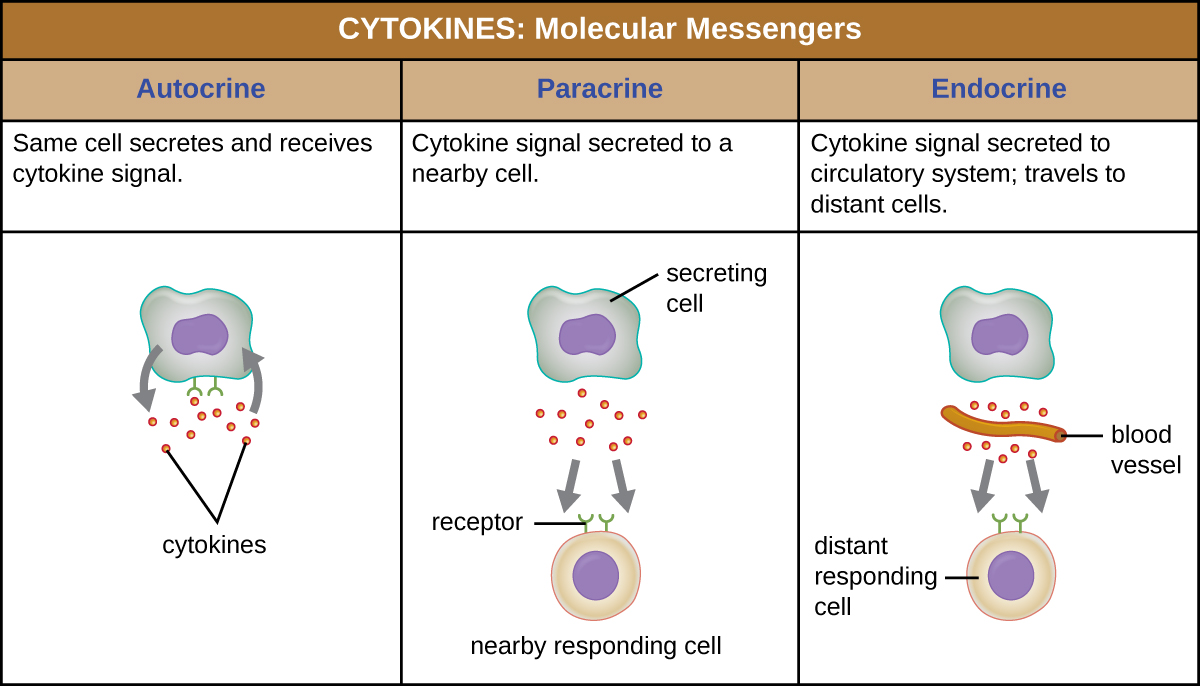
Три важливі класи цитокінів - інтерлейкіни, хемокіни та інтерферони. Спочатку вважалося, що інтерлейкіни виробляються лише лейкоцитами (лейкоцитами) і лише стимулюють лейкоцити, отже, причини їх назви. Хоча інтерлейкіни беруть участь в модуляції практично кожної функції імунної системи, їх роль в організмі не обмежується імунітетом. Інтерлейкіни також виробляються і стимулюють різноманітні клітини, не пов'язані з імунним захистом.
Хемокіни - це хемотаксичні фактори, які набирають лейкоцити до місць інфекції, пошкодження тканин та запалення. На відміну від більш загальних хемотаксичних факторів, таких як фактор комплементу C5a, хемокіни дуже специфічні в підмножині лейкоцитів, які вони набирають.
Інтерферони - це різноманітна група імунних сигнальних молекул і особливо важливі в нашому захисті від вірусів. Інтерферони I типу (інтерферон-α і інтерферон-β) виробляються і вивільняються клітинами, зараженими вірусом. Ці інтерферони стимулюють сусідні клітини зупиняти вироблення мРНК, руйнують вже вироблену РНК і зменшують синтез білка. Ці клітинні зміни гальмують вірусну реплікацію і вироблення зрілого вірусу, сповільнюючи поширення вірусу. Інтерферони I типу також стимулюють різні імунні клітини, що беруть участь у вірусному кліренсі, більш агресивно атакувати заражені вірусом клітини. Інтерферон II типу (інтерферон-γ) є важливим активатором імунних клітин (рис.\(\PageIndex{4}\)).
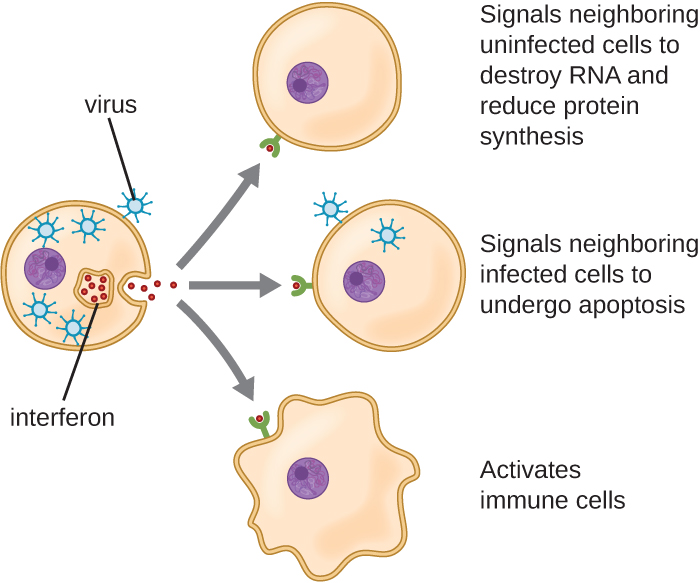
Запалення, що викликають медіатори
Багато хімічних медіаторів, розглянутих у цьому розділі, певним чином сприяють запаленню та лихоманці, які є неспецифічними імунними реакціями, більш детально розглянутими в Запаленні та лихоманці. Цитокіни стимулюють вироблення білків гострої фази, таких як С-реактивний білок і манноззв'язуючий лектин в печінці. Ці білки гострої фази діють як опсоніни, активуючи каскади комплементу через лектинний шлях.
Деякі цитокіни також пов'язують огрядні клітини і базофіли, спонукаючи їх до вивільнення гістаміну, прозапального з'єднання. Гістамінові рецептори знаходяться на різних клітині і опосередковують прозапальні події, такі як бронхозвуження (затягування дихальних шляхів) і скорочення гладкої мускулатури.
Крім гістаміну, огрядні клітини можуть виділяти інші хімічні медіатори, такі як лейкотрієни. Лейкотрієни - це прозапальні медіатори на ліпідній основі, які виробляються з метаболізму арахідонової кислоти в клітинній мембрані лейкоцитів і клітинам тканин. Порівняно з прозапальними ефектами гістаміну, лейкотрієни є більш потужними та тривалішими. Разом ці хімічні медіатори можуть викликати кашель, блювоту та діарею, які служать для вигнання хвороботворних мікроорганізмів з організму.
Деякі цитокіни також стимулюють вироблення простагландинів, хімічних медіаторів, що сприяють запальному впливу кінінів і гістамінів. Простагландини також можуть допомогти встановити температуру тіла вище, що призводить до лихоманки, яка сприяє діяльності лейкоцитів і трохи пригнічує ріст патогенних мікробів (див. Запалення та лихоманка).
Ще один медіатор запалення - брадикінін - сприяє набряку, який виникає при витоку рідини і лейкоцитів з кровотоку і в тканини. Він зв'язується з рецепторами на клітині в стінках капілярів, внаслідок чого капіляри розширюються і стають більш проникними для рідин.
Вправа\(\PageIndex{3}\)
- Що спільного три шляхи активації комплементу?
- Поясніть аутокринні, паракринні та ендокринні сигнали.
- Назвіть два важливих медіатора, що викликають запалення.
Клінічна спрямованість: Частина 2
Щоб полегшити звуження дихальних шляхів, Анжелу негайно лікують антигістамінними препаратами і вводять кортикостероїди через інгалятор, а потім контролюють протягом певного періоду часу. Хоча її стан не погіршується, препарати, здається, не полегшують її стан. Вона госпіталізується в лікарню для подальшого спостереження, тестування та лікування.
Після прийому клініцист проводить тестування на алергію, щоб спробувати визначити, чи може щось у її оточенні викликати алергічну запальну реакцію. Лікар призначає аналіз крові, щоб перевірити рівень конкретних цитокінів. Зразок мокротиння також береться і відправляється в лабораторію для мікробного фарбування, культивування та ідентифікації патогенів, які можуть викликати інфекцію.
Вправа\(\PageIndex{4}\)
- Які аспекти вродженої імунної системи можуть сприяти звуженню дихальних шляхів Анжели?
- Чому Анжелу лікували антигістамінними препаратами?
- Чому лікар цікавиться рівнем цитокінів у крові Анжели?
У таблиці\(\PageIndex{3}\) наведено короткий виклад хімічних захисних засобів, розглянутих у цьому розділі.
| Оборона | Приклади | Функція |
|---|---|---|
| Хімічні речовини та ферменти в рідинях організму | Шкірне сало з сальних залоз | Забезпечує масляний бар'єр, захищаючи пори волосяних фолікулів від пато |
| Олеїнова кислота з шкірного сала та мікробіоти шкіри | Знижує рН для інгібування патогенів | |
| Лізоцим у виділеннях | Вбиває бактерії атакуючи клітинну стінку | |
| Кислота в шлунку, сечі та піхві | Пригнічує або вбиває бактерії | |
| Травні ферменти і жовч | Вбити бактерії | |
| Лактоферин і трансферин | Зв'язують і секвестують залізо, пригнічуючи ріст бактерій | |
| Поверхнево-активна речовина в легенях | Вбиває бактерії | |
| Антимікробні пептиди | Дефенсіни, бактеріоцини, дерміцидин, кателіцидин, гістатини, | Вбивайте бактерії, атакуючи мембрани або втручаючись у функції клітин |
| Плазмові білкові медіатори | Білки гострої фази (С-реактивний білок, сироватковий амілоїд А, феритин, фібриноген, трансферин та лектин, що зв'язує маннозу) | Пригнічують ріст бактерій та допомагають у відловлюванні та знищенні бактерій |
| Доповнює C3b і C4b | Опсонізація патогенів для допомоги фагоцитозу | |
| Доповнення C5a | Хімоаттрактант для фагоцитів | |
| Доповнює С3а і С5а | Прозапальні анафілатоксини | |
| цитокіни | Інтерлейкіни | Стимулюють і модулюють більшість функцій імунної системи |
| Хемокіни | Набирайте лейкоцити в інфіковану область | |
| Інтерферони | Оповіщення клітин до вірусної інфекції, індукують апоптоз інфікованих вірусом клітин, індукують противірусний захист у інфікованих та прилеглих неінфікованих клітин, стимулюють імунні клітини атакувати заражені вірусом клітини | |
| Медиатори, що викликають запалення | Гістамін | Сприяє розширенню судин, бронхозвуженню, скороченню гладкої мускулатури, підвищенню секреції і вироблення слизу |
| лейкотрієни | Сприяють запаленню; сильніше і довше, ніж гістамін | |
| простагландини | Сприяють запаленню та лихоманці | |
| Брадикінін | Підвищує вазодилатацію і проникність судин, приводячи до набряків |
Ключові поняття та резюме
- Численні хімічні медіатори, вироблені ендогенно і екзогенно, виявляють неспецифічні антимікробні функції.
- Багато хімічних медіаторів містяться в рідинях організму, таких як шкірне сало, слина, слиз, шлункові та кишкові рідини, сеча, сльози, церумен та вагінальні виділення.
- Протимікробні пептиди (АМП), виявлені на шкірі і в інших ділянках тіла, в значній мірі виробляються у відповідь на наявність хвороботворних мікроорганізмів. До них відносяться дермцидин, кателіцидин, дефенсіни, гістатини та бактеріоцини.
- Плазма містить різні білки, які служать хімічними медіаторами, включаючи білки гострої фази, білки комплементу та цитокіни.
- Система комплементу включає численні білки-попередники, які циркулюють в плазмі. Ці білки активуються в каскадній послідовності в присутності мікробів, в результаті чого відбувається опсонізація патогенів, хемоатракціон лейкоцитів, індукція запалення і цитоліз через утворення мембранного комплексу атаки (ГДК).
- Цитокіни - це білки, які полегшують різні неспецифічні реакції вроджених імунних клітин, включаючи виробництво інших хімічних медіаторів, проліферацію клітин, загибель клітин та диференціювання.
- Цитокіни відіграють ключову роль у запальній реакції, викликаючи вироблення медіаторів, що викликають запалення, таких як білки гострої фази, гістамін, лейкотрієни, простагландини та брадикінін.
