17.3: Послідовність цілого генома
- Page ID
- 1861
Навички для розвитку
- Опишіть три типи секвенування
- Визначте секвенування цілого генома
Хоча в останні роки в медичних науках були досягнуті значні успіхи, лікарі все ще збентежені деякими захворюваннями, і вони використовують секвенування цілого генома, щоб дістатися до дна проблеми. Секвенування цілого генома - це процес, який визначає послідовність ДНК всього генома. Секвенування цілого генома - це підхід грубої сили до вирішення проблем, коли в основі захворювання є генетична основа. Зараз кілька лабораторій надають послуги для послідовності, аналізу та інтерпретації цілих геномів.
Наприклад, секвенування цілого екзому є більш дешевою альтернативою секвенування цілого генома. У секвенуванні екзомів секвенуються лише кодуючі, екзон-продукують області ДНК. У 2010 році для порятунку молодого хлопчика, у кишечнику якого були множинні таємничі абсцеси, було використано цільноекзомне секвенування. Дитині було кілька операцій товстої кишки без полегшення. Нарешті, було проведено секвенування цілого екзому, яке виявило дефект шляху, який контролює апоптоз (запрограмовану загибель клітин). Трансплантація кісткового мозку була використана для подолання цього генетичного захворювання, що призвело до лікування хлопчика. Він був першою людиною, яку успішно лікували на основі діагнозу, поставленого цільноекзомним секвенуванням. Сьогодні секвенування генома людини є більш доступним і може бути завершено за день або два приблизно за 1000 доларів.
Стратегії, що використовуються в секвенуванні проектів
Основною технікою секвенування, яка використовується у всіх сучасних проектах секвенування, є метод припинення ланцюга (також відомий як метод дідеокси), який був розроблений Фредом Сангером у 1970-х роках. Метод припинення ланцюга передбачає реплікацію ДНК однониткового шаблону з використанням праймера і звичайного дезоксинуклеотиду (dNTP), який є мономером, або єдиною одиницею ДНК. Праймер і dnTp змішуються з невеликою часткою флуоресцентно маркованих дидезоксинуклеотидів (DDNTP). DDNTP - це мономери, у яких відсутня гідроксильна група (—OH) на місці, на якому інший нуклеотид зазвичай приєднується для формування ланцюга (рис.\(\PageIndex{1}\)).
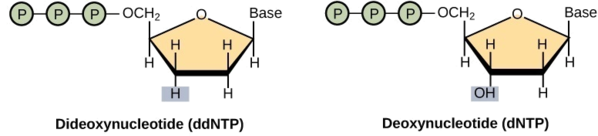
Кожен DDNTP маркується різним кольором флюорофора. Кожен раз, коли DDNTP включений у зростаючу комплементарну нитку, він припиняє процес реплікації ДНК, що призводить до декількох коротких ниток реплікованої ДНК, які припиняються в іншій точці під час реплікації. Коли реакційна суміш обробляється гелевим електрофорезом після поділу на окремі нитки, множинні знову репліковані нитки ДНК утворюють сходи через різні розміри. Оскільки DDNTP флуоресцентно позначені, кожна смуга на гелі відображає розмір ланцюга ДНК та DDNTP, який припинив реакцію. Різні кольори флюорофорових маркованих DDNTP допомагають ідентифікувати DDNTP, включений у цьому положенні. Зчитування гелю виходячи з кольору кожної смуги на драбинці виробляє послідовність шаблонної пасма (рис.\(\PageIndex{2}\)).
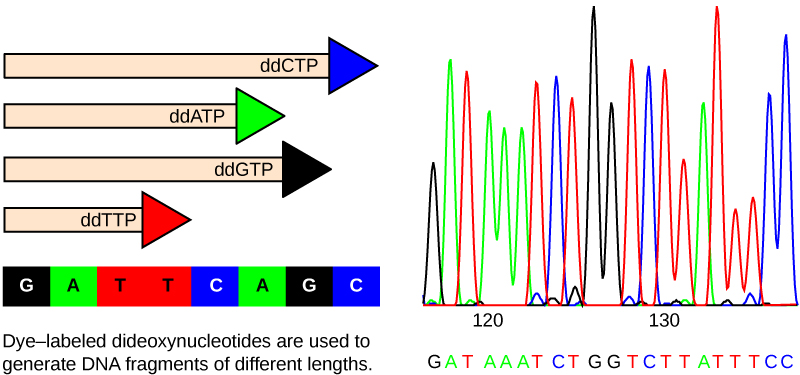
Ранні стратегії: секвенування дробовика та парне секвенування кінця
У методі секвенування дробовика кілька копій фрагмента ДНК розрізаються випадковим чином на багато менших шматочків (дещо як те, що відбувається з круглим пострілом патрона при стрільбі з дробовика). Потім всі сегменти послідовні за допомогою методу ланцюгового секвенування. Потім за допомогою комп'ютера фрагменти аналізуються, щоб побачити, де їх послідовності перекриваються. Зіставляючи послідовності, що перекриваються в кінці кожного фрагмента, можна реформувати всю послідовність ДНК. Більша послідовність, яка збирається з перекриваються коротших послідовностей, називається contig. Як аналогію вважайте, що хтось має чотири копії пейзажної фотографії, яку ви ніколи раніше не бачили, і нічого не знаєте про те, як вона повинна виглядати. Потім людина розриває кожну фотографію руками, так що з кожної копії присутні шматочки різного розміру. Потім людина змішує всі частини разом і просить вас реконструювати фотографію. В одному з менших шматочків ви бачите гору. У більшому шматку ви бачите, що та сама гора знаходиться за озером. На третьому фрагменті зображено лише озеро, але воно виявляє, що на березі озера є каюта. Тому, дивлячись на інформацію, що перекривається в цих трьох фрагментах, ви знаєте, що картина містить гору за озером, у якого на березі є будиночок. Це принцип реконструкції цілих послідовностей ДНК за допомогою секвенування дробовика.
Спочатку секвенування дробовика аналізувало лише один кінець кожного фрагмента на предмет накладок. Цього було достатньо для секвенування малих геномів. Однак прагнення до послідовності більших геномів, таких як людський, призвело до розвитку секвенування двоствольної рушниці, більш формально відомого як парне секвенування. При попарному послідовності обидва кінці кожного фрагмента аналізуються на перекриття. Тому парне послідовність є більш громіздким, ніж секвенування дробовика, але простіше реконструювати послідовність, оскільки є більше доступної інформації.
Послідовність наступного покоління
З 2005 року методи автоматизованого секвенування, що використовуються лабораторіями, знаходяться під парасолькою секвенування наступного покоління, яке є групою автоматизованих методів, що використовуються для швидкого секвенування ДНК. Ці автоматизовані недорогі секвенсори можуть генерувати послідовності сотень тисяч або мільйонів коротких фрагментів (від 25 до 500 базових пар) протягом одного дня. Ці секвенсори використовують складне програмне забезпечення, щоб пройти через громіздкий процес приведення всіх фрагментів в порядок.
Еволюція зв'язку: порівняння послідовностей
Вирівнювання послідовності - це розташування білків, ДНК або РНК; він використовується для ідентифікації областей подібності між типами клітин або видами, що може свідчити про збереження функції або структур. Для побудови філогенетичних дерев можна використовувати вирівнювання послідовностей. Наступний веб-сайт використовує програмне забезпечення під назвою BLAST (основний інструмент пошуку локального вирівнювання).
У розділі «Основний вибух» натисніть «Нуклеотидний вибух». Введіть наступну послідовність у велике поле «послідовність запитів»: ATTGCTTCGATTGCA. Під полем знайдіть поле «Види» і введіть «людина» або «Homo sapiens». Потім натисніть «BLAST», щоб порівняти введену послідовність з відомими послідовностями людського генома. Результатом є те, що ця послідовність зустрічається в більш ніж ста місцях геному людини. Прокрутіть вниз графіку з горизонтальними смугами, і ви побачите короткий опис кожного з відповідних хітів. Виберіть один з хітів у верхній частині списку і натисніть на «Графіка». Це приведе вас до сторінки, яка показує, де послідовність знаходиться в межах всього людського генома. Ви можете пересунути повзунок, який виглядає як зелений прапорець назад і вперед, щоб переглянути послідовності безпосередньо навколо вибраного гена. Потім ви можете повернутися до обраної послідовності натисканням кнопки «ATG».
Використання цільногеномних послідовностей модельних організмів
Перший геном, який був повністю секвенований, був бактеріальний вірус, бактеріофаг fx174 (5368 пар основи); це було досягнуто Фредом Сангером за допомогою секвенування дробовика. Пізніше були секвеновані кілька інших органел та вірусних геномів. Першим організмом, геном якого був секвенований, була бактерія Haemophilus influenzae; це було здійснено Крейгом Вентером у 1980-х роках. Приблизно 74 різні лабораторії співпрацювали над секвенуванням генома дріжджів Saccharomyces cerevisiae, який розпочався в 1989 році і був завершений у 1996 році, оскільки він був у 60 разів більшим, ніж будь-який інший геном, який був секвенований. До 1997 року були доступні послідовності геному двох важливих модельних організмів: бактерії Escherichia coli K12 та дріжджів Saccharomyces cerevisiae. Зараз відомі геноми інших модельних організмів, таких як миша Mus musculus, плодова муха Drosophila melanogaster, нематода Caenorhabditis elegans та людина Homo sapiens. Багато фундаментальних досліджень проводиться в модельних організмах, оскільки інформація може бути застосована до генетично схожих організмів. Модельний організм - це вид, який вивчається як модель для розуміння біологічних процесів в інших видах, представлених модельним організмом. Наявність секвенованих цілих геномів допомагає дослідницьким зусиллям цих модельних організмів. Процес приєднання біологічної інформації до послідовностей генів називається анотацією генома. Анотація послідовностей генів допомагає в базових експериментах з молекулярної біології, таких як розробка праймерів ПЛР та мішеней РНК.
Використання послідовностей геному
Мікромасиви ДНК - це методи, що використовуються для виявлення експресії генів шляхом аналізу масиву фрагментів ДНК, які фіксуються на скляному слайді або кремнієвому чіпі для ідентифікації активних генів та ідентифікації послідовностей. Майже мільйон генотипових аномалій можна виявити за допомогою мікромасивів, тоді як секвенування цілого генома може надати інформацію про всі шість мільярдів пар основ у геномі людини. Хоча вивчення медичних застосувань секвенування генома цікаве, ця дисципліна, як правило, зупиняється на аномальній функції генів. Знання всього геному дозволить виявити майбутні захворювання та інші генетичні порушення на ранньому етапі, що дозволить приймати більш обґрунтовані рішення щодо способу життя, ліків та народження дітей. Геноміка все ще знаходиться в зародковому стані, хоча коли-небудь може стати звичним використовувати секвенування цілого генома для скринінгу кожного новонародженого для виявлення генетичних відхилень.
Окрім хвороб та медицини, геноміка може сприяти розробці нових ферментів, які перетворюють біомасу на біопаливо, що призводить до збільшення виробництва врожаю та палива та зниження витрат для споживача. Ці знання повинні дозволити краще методи боротьби з мікробами, які використовуються у виробництві біопалива. Геноміка також може покращити методи, що використовуються для моніторингу впливу забруднюючих речовин на екосистеми та сприяння очищенню забруднюючих речовин навколишнього середовища. Геноміка дозволила розвивати агрохімікати та фармацевтичні препарати, які могли б принести користь медичній науці та сільському господарству.
Звучить чудово, щоб мати всі знання, які ми можемо отримати від секвенування цілого генома; однак люди несуть відповідальність за розумне використання цих знань. В іншому випадку може бути легко зловживати силою таких знань, що призведе до дискримінації на основі генетики людини, генної інженерії людини та інших етичних проблем. Ця інформація також може призвести до юридичних питань щодо здоров'я та конфіденційності.
Резюме
Секвенування цілого генома є останнім доступним ресурсом для лікування генетичних захворювань. Деякі лікарі використовують секвенування цілого генома, щоб врятувати життя. Геноміка має багато промислових застосувань, включаючи розробку біопалива, сільське господарство, фармацевтику та контроль забруднення. Основний принцип всіх сучасних стратегій секвенування передбачає метод припинення ланцюга секвенування.
Незважаючи на те, що послідовності генома людини дають ключові уявлення медичним працівникам, дослідники використовують цільногеномні послідовності модельних організмів, щоб краще зрозуміти геном виду. Автоматизація та зниження вартості секвенування цілого генома можуть призвести до персоналізованої медицини в майбутньому.
Глосарій
- метод припинення ланцюга
- метод секвенування ДНК з використанням мічених дидезоксинуклеотидів для припинення реплікації ДНК; його також називають методом дидеокси або методом Сангера
- контінг
- більша послідовність ДНК, зібрана з перекриваються коротших послідовностей
- дезоксинуклеотид
- індивідуальний мономер (єдина одиниця) ДНК
- дидезоксинуклеотид
- індивідуальний мономер ДНК, в якому відсутня гідроксильна група (—OH)
- Мікромасив ДНК
- метод, який використовується для виявлення експресії генів шляхом аналізу масиву фрагментів ДНК, які фіксуються на скляному слайді або кремнієвому чіпі для ідентифікації активних генів та ідентифікації послідовностей
- анотація геному
- процес приєднання біологічної інформації до послідовностей генів
- модель організм
- вид, який вивчається і використовується як модель для розуміння біологічних процесів в інших видах, представлених модельним організмом
- послідовність наступного покоління
- група автоматизованих методик, що використовуються для швидкого секвенування ДНК
- секвенування рушниці
- метод, який використовується для послідовності декількох фрагментів ДНК для генерації послідовності великого шматка ДНК
- секвенування цілого генома
- процес, що визначає послідовність ДНК всього генома

