8.10: Криві охолодження
- Page ID
- 21150
Метод, який використовується для відображення меж фаз на фазовій діаграмі, полягає в вимірюванні швидкості охолодження для зразка відомого складу. Швидкість охолодження буде змінюватися в міру того, як зразок (або якась його частина) почне зазнавати фазової зміни. Ці «розриви» з'являться як зміни нахилу в кривій температура-час. Розглянемо бінарну суміш, для якої діаграма стану наведена так, як показано на малюнку\(\PageIndex{1A}\). Крива охолодження зразка, яка починається при температурі і складі, заданих точкою а, показана на малюнку\(\PageIndex{1B}\).

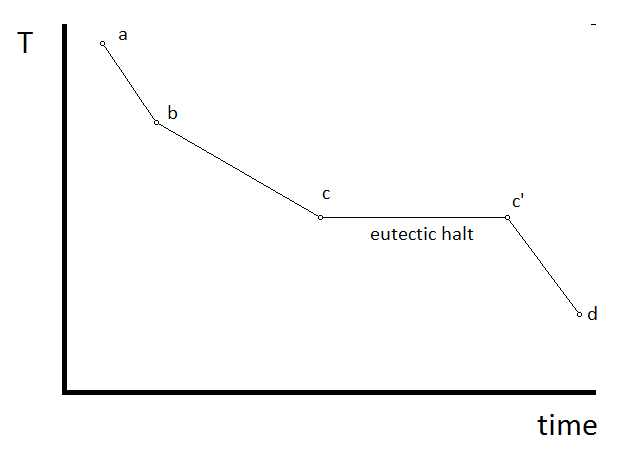
Коли зразок охолоджується з точки а, температура буде зменшуватися зі швидкістю, визначеною складом зразка, і геометрією експерименту (наприклад, очікується більш швидке охолодження, якщо зразок має більшу площу поверхні, що піддається впливу більш холодного оточення) і різниця температур між зразком і околиці.
Коли температура досягне такої в точці b, якась тверда сполука B почне утворюватися. Це призведе до уповільнення охолодження через екзотермічного характеру твердого освіти. Але також зміниться склад рідини, стаючи багатшими сполукою А, оскільки B видаляється з рідкої фази у вигляді твердої речовини. Це триватиме до тих пір, поки рідина не досягне складу в евтектичній точці (точка c на схемі.)
Коли температура досягне такої в точці c, обидва з'єднання А і В застигнуть, а склад рідкої фази залишиться постійним. Таким чином, температура перестане змінюватися, створюючи те, що називається евтектичною зупинкою. Після того, як весь матеріал затвердіє (у час, зазначений точкою c '), охолодження продовжиться зі швидкістю, визначеною теплоємністю двох твердих тіл A і B, складом і (звичайно) геометрією експериментальної установки. Вимірюючи криві охолодження для зразків різного складу, можна зіставити всю фазову діаграму.
