INTERCHAPTER: Ретросинтетичний аналіз та прогнозування метаболічних шляхів
- Page ID
- 20882
Уявіть, що ви біологічний хімік, який проводить дослідження бактеріального обміну речовин. Ви і ваші колеги ізолюєте цікаву біомолекулу з бактеріальної культури, потім використовуєте мас-спектрометрію, ЯМР та інші аналітичні методи для визначення її структури. Використовуючи свій «набір інструментів» відомих типів органічних реакцій - нуклеофільна заміщення, фосфорилювання, альдольні добавки тощо - чи можете ви з'ясувати хімічно розумний шлях, за допомогою якого ваша сполука може бути ферментативно синтезована з простих метаболічних попередників? Іншими словами, чи можете ви заповнити відсутні біохімічні кроки (або принаймні деякі з них), щоб придумати потенційний новий метаболічний шлях, який потім може бути використаний гіпотезою для майбутньої експериментальної роботи, щоб спробувати знайти та вивчити фактичні ферменти, що беруть участь?
Фактичний приклад наближення цього сценарію наведено нижче. Повний біосинтетичний шлях для ізопентенілдифосфату (IPP), молекули будівельного блоку для всіх сполук isoprenoi d, відомий з 1960-х років. цей шлях, який починається з ацетил-КоА, був показаний активним у дріжджах, рослині та багатьох інших видах, включаючи людей. Однак дослідники наприкінці 1980-х років виявили докази, що вказують на те, що відомого шляху немає у бактерій, хоча вони явно використовують IPP як молекулу будівельного блоку так само, як це роблять інші форми життя.
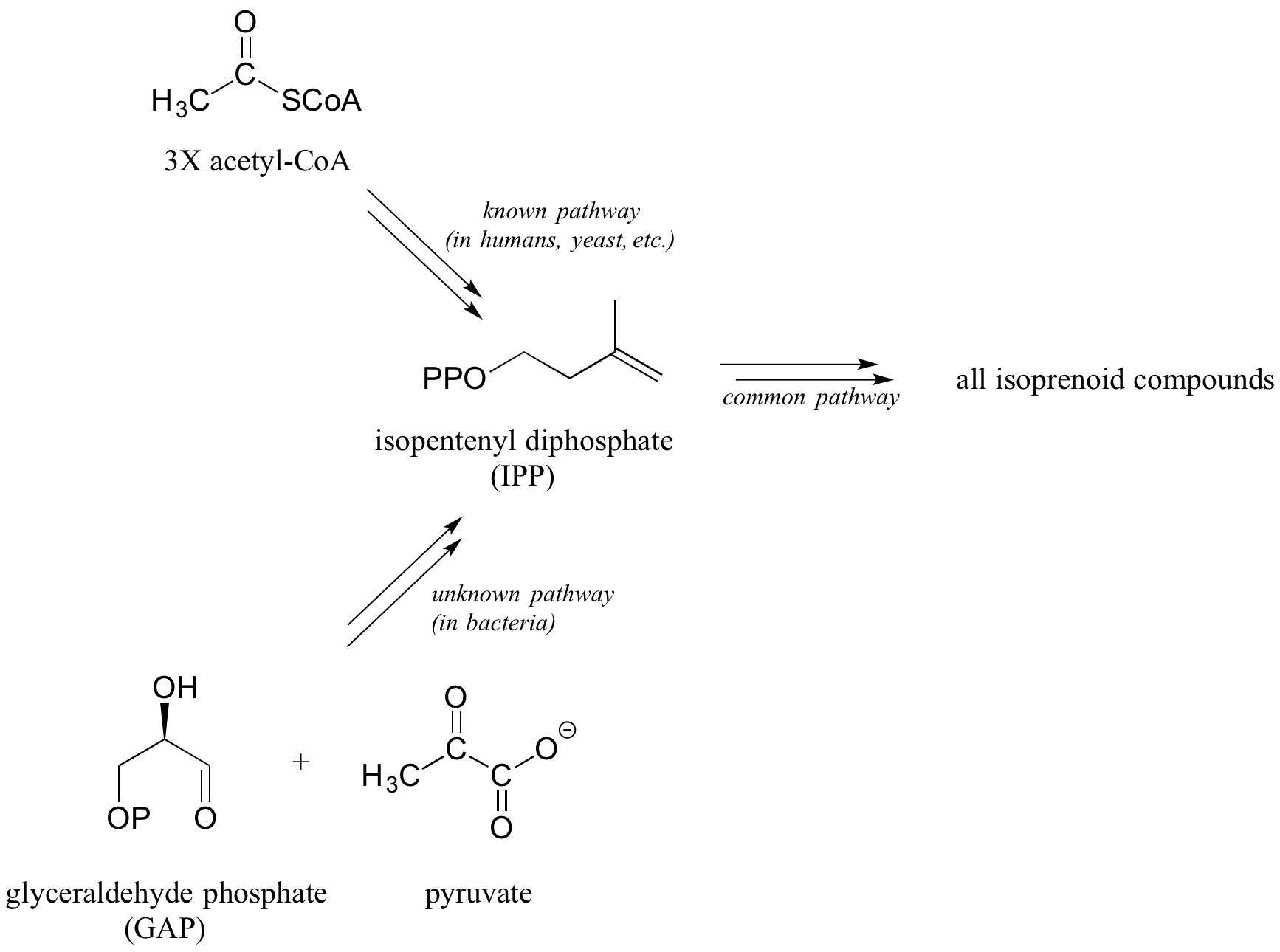
Протягом наступних кількох років дослідники провели ряд експериментів, в яких бактерії вирощували на середовищі, що містить глюкозу, «помічену» ізотопом 13 С. З результатами цих експериментів, у поєднанні з їхніми знаннями про загальні біологічні органічні типи реакцій, дослідники змогли правильно передбачити, що бактеріальний шлях починається з двох молекул попередників (пірувату та гліцеральдегіду фосфату замість ацетилу КоА), і вони також правильно передбачили перші два ферментативних етапи нововиявленого бактеріального шляху. Це досягнення врешті-решт призвело до з'ясування кожного кроку на шляху та виділення ферментів, що каталізують їх. (Біохім Дж. 1993, 295, 517; Джей Ам. Хім. Соц. 1996, 118, 2564; Ліпіди 2008, 43, 1095)
Чому вони не змогли передбачити весь шлях? Виявляється, кілька пізніших кроків були дещо незвичайними, незнайомими типами реакцій - але відкриття цих реакцій залежало на правильному прогнозі більш звичних перших двох кроків.
Багатоступінчасті проблеми трансформації цього типу дають безпрецедентну можливість використовувати наші знання з біологічної органічної хімії в поєднанні з творчими міркуваннями для вирішення складних, актуальних наукових головоломок. На даний момент у вашій кар'єрі з органічної хімії ви ще не накопичили достатньо інструментів у вашому наборі інструментів реакції для вирішення більшості реальних проблем біохімічного шляху, таких як той, про який йшлося вище - але до того часу, коли ми закінчимо хімію окислення та зменшення в розділі 15, ви зможете визнати більшість типів реакцій, з якими ви зіткнетеся в реальному метаболізмі, і буде викликано передбачити деякі реальні шляхи в кінці глави проблем.
Однак у вас зараз достатньо біоорганічного репертуару, щоб почати вивчати, як можна підійти до багатоетапних проблем шляху, використовуючи для практики деякі узагальнені, гіпотетичні приклади, в яких типи реакцій обмежені тими, з якими ви вже знайомі.
Уявіть, що ви хочете розібратися, як складаються старомодні механічні годинник. Один із способів зробити це - почати з робочого годинника, і розібрати його поштучно. Як варіант, можна було б почати з усіх розібраних частин, плюс багато інших дрібних деталей з різних годинників, і спробувати з'ясувати, як зібрати конкретний годинник, який вас цікавить. Який підхід простіше? Відповідь інтуїтивно очевидна - зазвичай легше розібрати речі, ніж скласти їх разом.
Те ж саме стосується молекул. Якщо ми хочемо з'ясувати біосинтетичний шлях, за допомогою якого велика, складна біомолекула може бути зроблена в клітці, має сенс почати з готового продукту, а потім подумки працювати назад, розбираючи його крок за кроком, використовуючи відомі, знайомі реакції, поки ми не перейдемо до більш простих молекул попередників. Починаючи з великої колекції потенційних молекул попередників і намагаючись зібрати правильні разом, щоб зробити цільовий продукт, було б грізним завданням.
Ретросинтетичний аналіз - концепція розумового демонтажу молекули крок за кроком назад до менших, простіших попередників за допомогою відомих реакцій - це потужний і широко використовуваний інтелектуальний інструмент, вперше розроблений синтетичними хіміками-органіками. Цей підхід також був адаптований для використання біологічними хіміками в спробах передбачити шляхи, за допомогою яких відомі біомолекули можуть бути синтезовані (або деградовані) в живих істотах.
У ретросинтезі ми думаємо про низку реакцій у зворотному напрямку. Хімічний крок назад (ретро) символізується «товстою» стрілкою, яку зазвичай називають ретросинтетичною стрілкою, і візуально передає фразу «може бути утворена з».

Розглянемо простий, гіпотетичний приклад: починаючи з молекули-мішені нижче, чи можемо ми придумати хімічно розумний шлях, починаючи з вказаних прекурсорів?
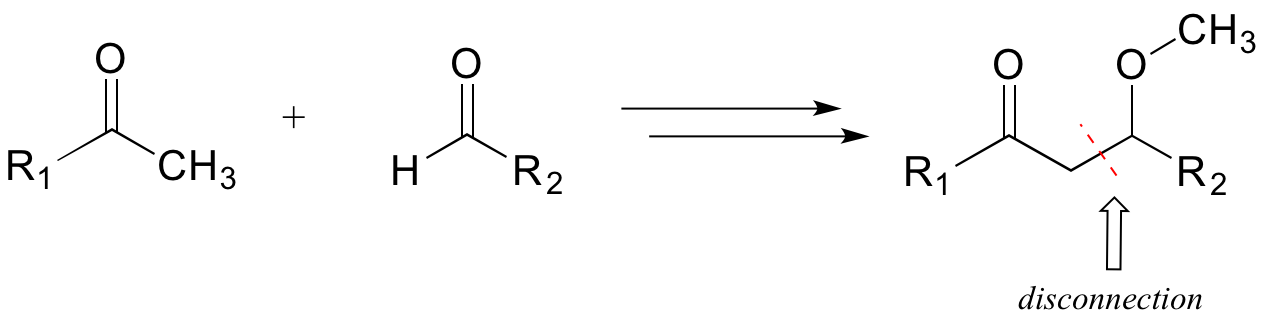
Першим кроком є виявлення відповідного відключення: ключового зв'язку (як правило, вуглецево-вуглецевого зв'язку), який повинен бути сформований, щоб зробити цільовий продукт з менших попередників. Ми шукаємо наш ментальний «інструментарій» поширених типів біохімічних реакцій і пам'ятаємо, що єдиний спосіб, про який ми знаємо (поки що!) зробити новий вуглецево-вуглецевий зв'язок відбувається через реакцію додавання альдола, яка відбувається при альфа-вуглецю. Тому ми можемо зробити ймовірне відключення поруч з альфа-вуглецем у молекулі-мішені.
Далі нам потрібно визнати, що реакція додавання альдола призводить до бета-гідроксикетону. Але наша цільова молекула - бета- метоксикетон! Працюючи назад, ми розуміємо, що бета-метоксигрупа може бути сформована з бета-гідроксигрупи реакцією метилювання SAM. Це наш перший ретросинтетичний (назад) крок.

Другий ретро-крок (альдол) пояснює роз'єднання, яке ми розпізнали раніше, і призводить до двох молекул попередника.
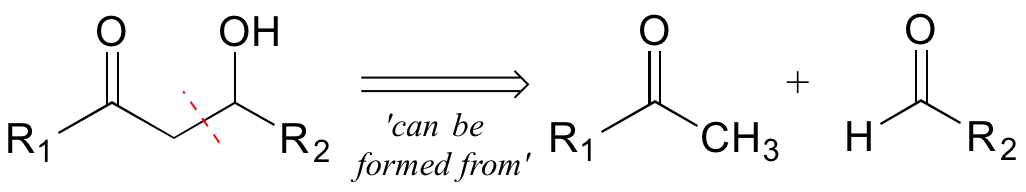
Тепер розглянемо більш залучені (але все ж гіпотетичні) біохімічні перетворення нижче:
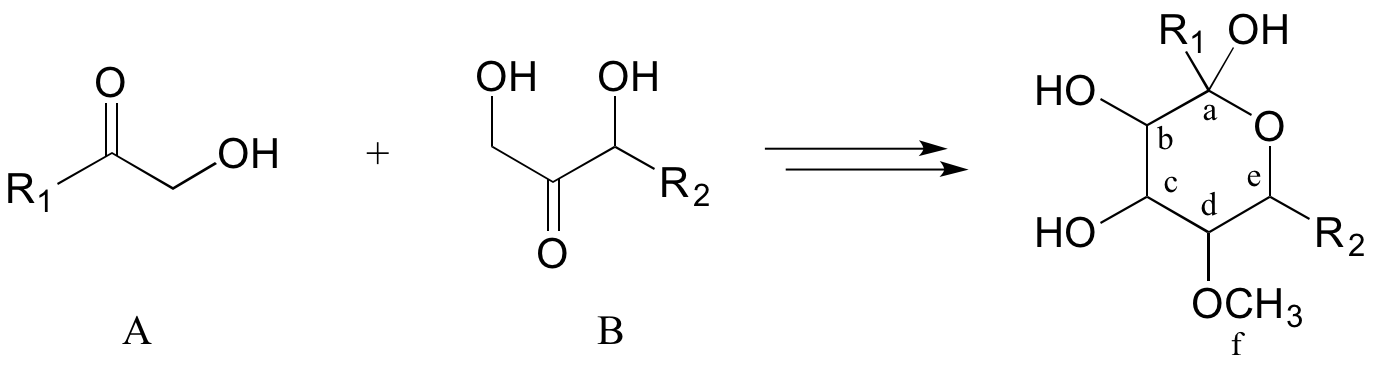
Часто найкраще, що потрібно зробити спочатку в цьому типі проблеми, - це підрахувати вуглеці в сполуках попередників і продукті - це дозволяє нам визнати, коли додаткові вуглеці з обох сторін повинні в якийсь момент враховуватися в нашому рішенні. При цьому один вуглець (позначений «f») був отриманий у вигляді метилового ефіру в продукті. Це легко пояснити: ми знаємо, що коензим S -аденозилметіонін (SAM) часто служить донором метильної групи в ферментативних реакціях O - або N -метилювання. Отже, ми можемо запропонувати наш перший зворотний (ретро) крок: продукт, як показано, може бути отриманий із SAM-залежного метилювання алкогольної групи на запропонованому проміжному рівні I.
Ретросинтетика крок 1:
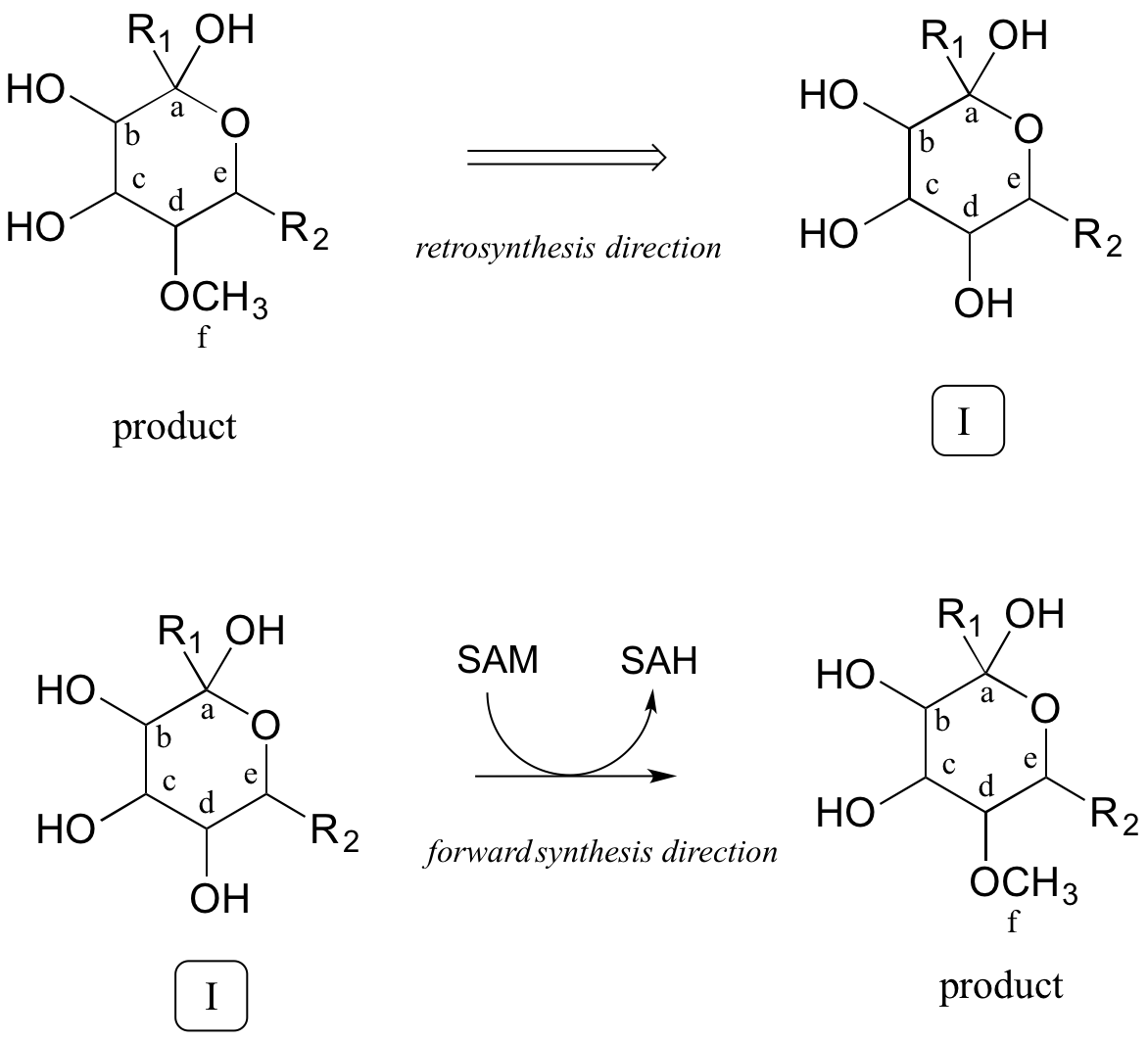
Звідки ми знаємо, що етап метилювання відбувається останнім? Ми цього не робимо - пам'ятайте, ми пропонуємо потенційний шлях, тому найкраще, що ми можемо зробити, це запропонувати кроки, які мають хімічний сенс, і які, сподіваємось, можуть бути підтверджені або визнані недійсними пізніше шляхом фактичних експериментів. Наразі ми будемо дотримуватися нашого початкового вибору, щоб зробити крок метилювання останнім.
Тепер, коли ми врахували додатковий вуглець, ключова річ, яку слід визнати щодо розглянутої трансформації, полягає в тому, що дві лінійні молекули об'єднуються, утворюючи циклічний продукт. Таким чином, між реагентами А і В потрібно зробити два з'єднання, одне з'єднати два, інше, щоб замкнути коло. Отже, наша основна робота в ретро-напрямку полягає у встановленні в продукті двох точок відключення: іншими словами, знайти дві зв'язки у продукті, які потрібно розібрати в нашому ретросинтетичному аналізі. Подивіться уважно на продукт: які функціональні групи ви бачите? Сподіваємось, ви зможете виділити дві алкогольні групи, метиловий ефір та (критично) циклічний гемікетал. Ми вже врахували метиловий ефір. Визначення циклічного гемікеталу важливо, оскільки це дозволяє нам зробити наступне «відключення»: ми знаємо, як гемікетал утворюється з кетону та алкоголю, тому ми можемо подумки працювати назад і прогнозувати проміжний проміжний II з відкритим ланцюгом, який може циклізуватися, щоб сформувати наш продукт.

Тепер, починаючи з групи R 1 і працюючи вздовж вуглецевого ланцюга, ми можемо враховувати вуглеці a-e на двох попередниках.
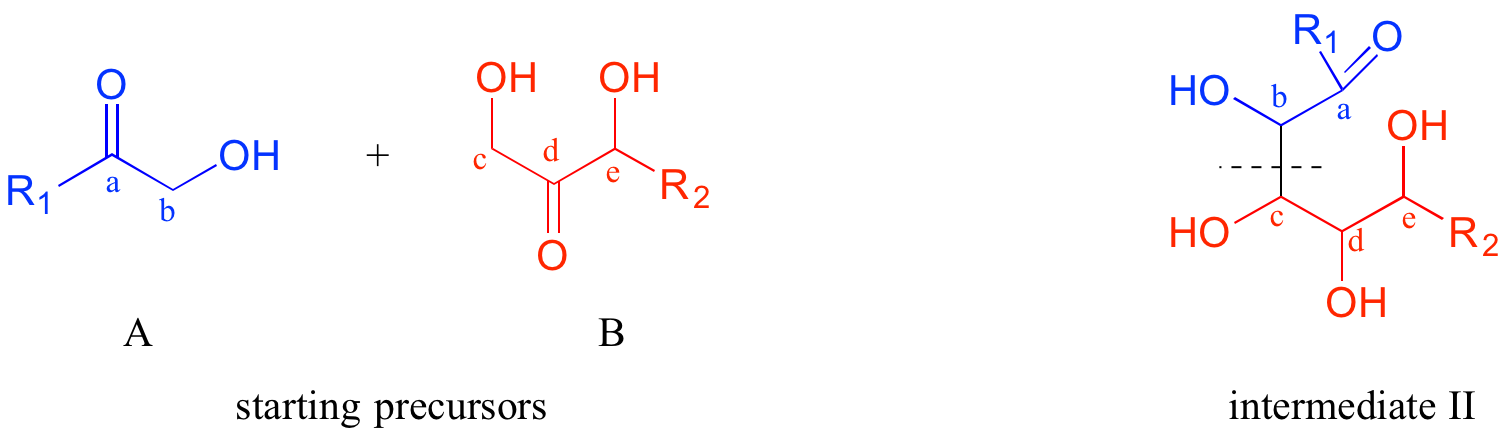
Таким чином, наступне відключення між вуглецями b і c Ось де наше володіння біологічною органічною реакційною здатністю дійсно вступає в гру: ОН при вуглецевому c проміжного II знаходиться в бета-положенні відносно карбонільного вуглецю а. алдол реакції додавання призводять до бета-гідрокси кетони або альдегіди. Тому ми можемо працювати назад ще на один крок і передбачити, що наш проміжний II утворився з реакції приєднання альдолу між проміжним III (як нуклеофіл) і молекулою попередника А (як електрофіл).

Ми проходимо більшу частину шляху додому - ми успішно врахували даний попередник A. Intermediate III, однак, не є попередником B. Чим відрізняється? І III, і В мають карбонільну і дві спиртові групи, але позиціонування різне: III - альдегід, а В - кетон. Згадайте раніше в цьому розділі: проміжний III може утворитися від ізомеризації карбонільної групи в сполуці B. Зараз ми враховуємо наш другий попередник - ми закінчили!
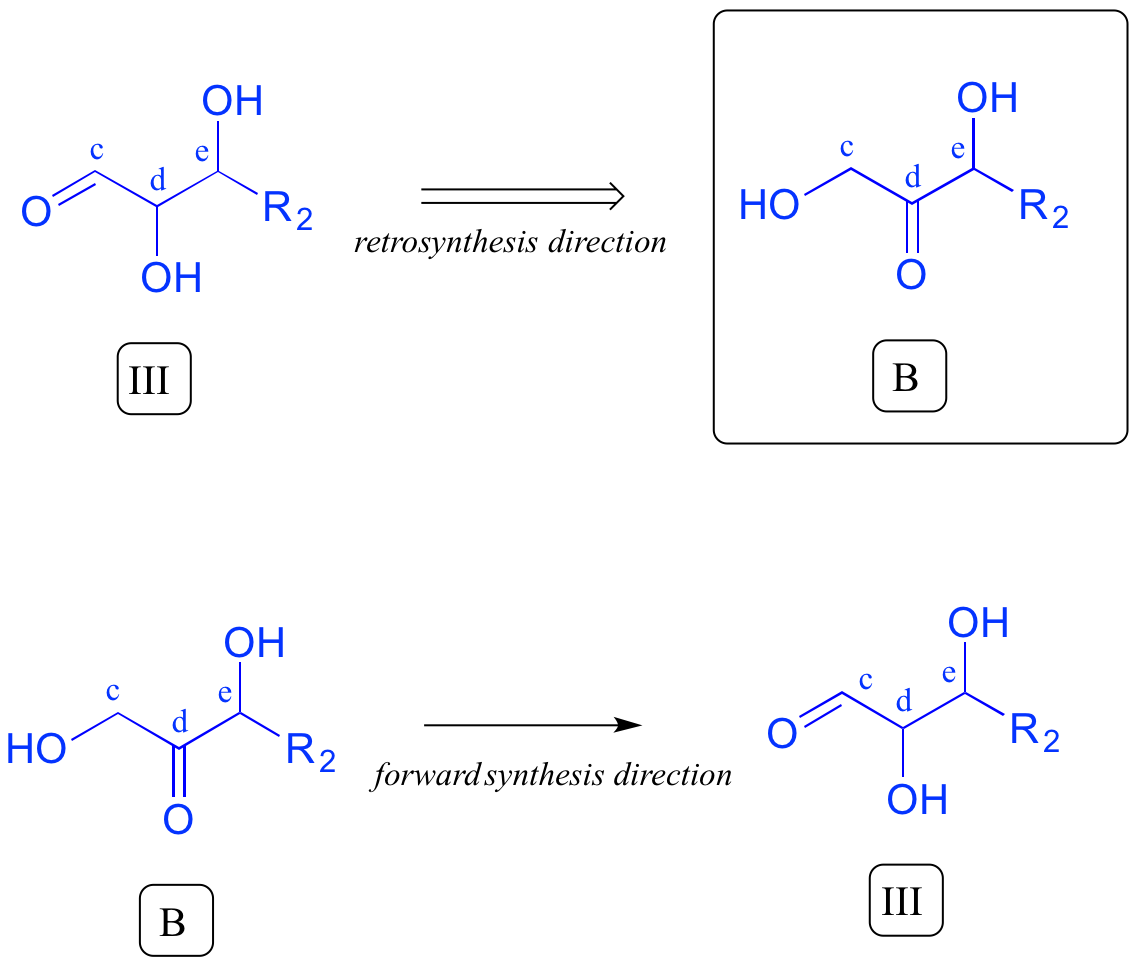
У прямому напрямку повну схему шляху можна записати наступним чином:
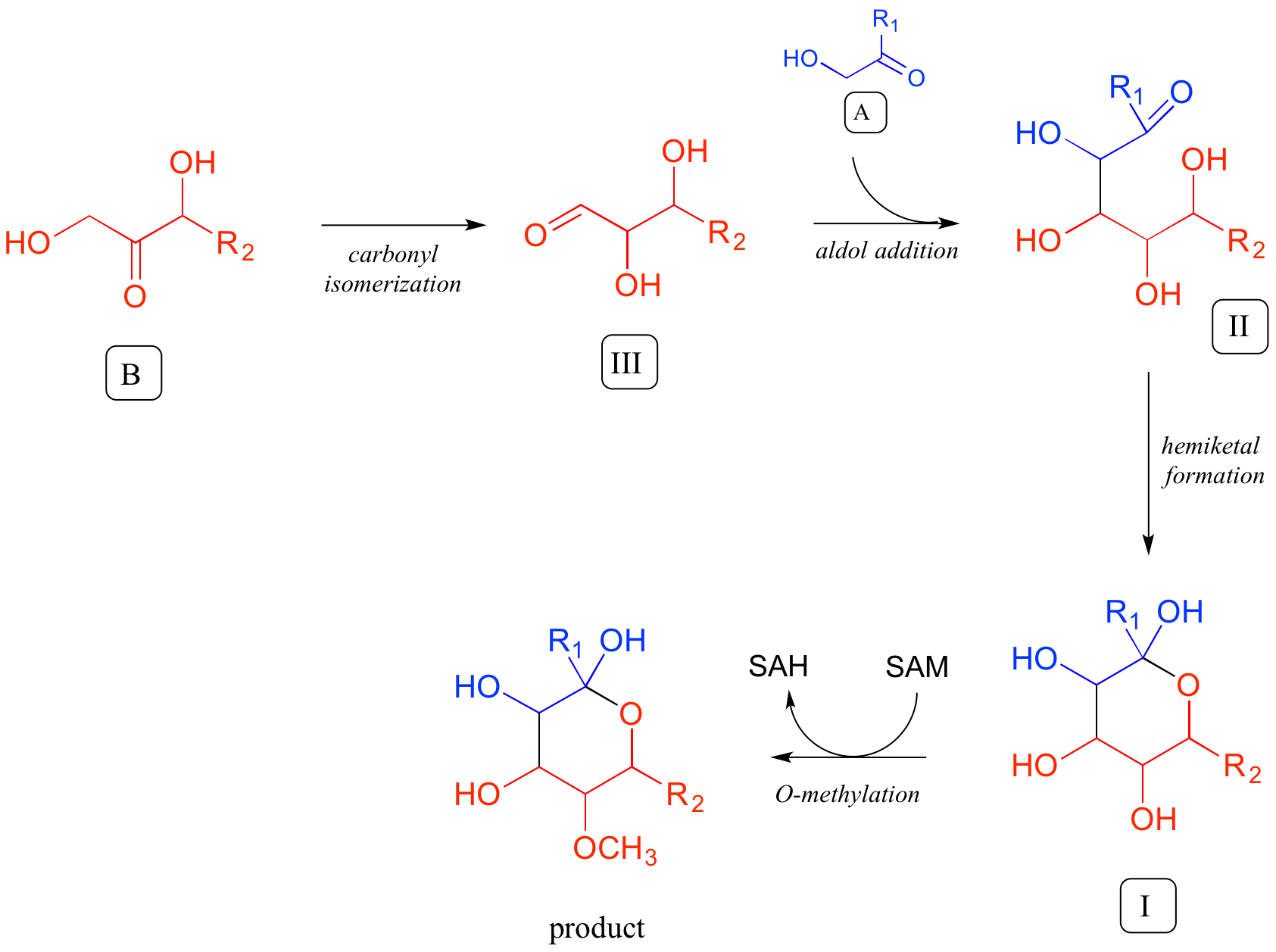
Повна діаграма «ретросинтезу» для цієї проблеми виглядає наступним чином:

Проблеми практики ретросинтезу/прогнозування шляхів
Callstack:
at (Хімія/Органічна_хімія/Органічна_хімія_з_біологічним_акцентом_(Soderberg)/INTERCHAPTER:_Ретросинтетичний_аналіз_та_прогнозування_метаболічних_шляхів), /content/body/p[43]/span, line 1, column 1
