9.1: Металеві алкенові комплекси
- Page ID
- 17688
Цілі навчання
У цій лекції ви дізнаєтеся наступне:
- Металеві алкенові комплекси.
- Взаємодія між металом та олефіном.
- Синтез та реактивність метал−олефінових комплексів.
- Взаємодії олефінів у комплексах алкенів металів.
Хоча перший металевий олефіновий комплекс датується давно початком 19-го століття, його рецептура була встановлена лише через століття в 1950-х роках. Реагуючи\(\ce{K2PtCl4}\) з eToH у 1827 році, датський хімік Зейзе синтезував відому сіль Зейсе,\(\ce{K[PtCl3(C2H4)]•H2O}\) що містить пов'язаний етиленовий фрагмент Pt і який, до речі, представляв перший комплекс метал-олефін (рис.\(\PageIndex{1}\)).
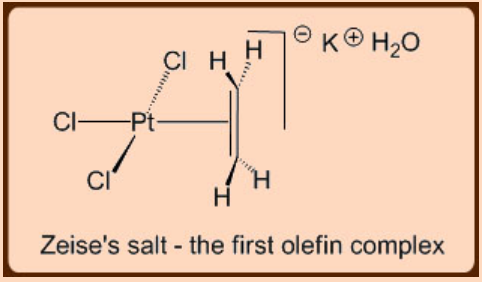
Взаємодія між металом і олефіном найкраще пояснюється моделлю Дьюара - Чатта, яка враховує дві взаємно протилежні донорства електронів, що включають σ−донорство олефінних C=C π−електронів на порожню орбіту d π металу з подальшим π−зворотним пожертвуванням із заповненого метал d π орбітальний в незайняту орбітальну C = C π*. Цілком зрозуміло, що для систем d 0 утворення метал−олефінових комплексів не спостерігається. Ступінь C = C вперед π-пожертвування металу та подальша π−зворотна пожертва від заповненої d π орбітальної до олефінної орбітальної C = C π* мають пряме відношення до зв'язку C = C металевого олефінного фрагмента у вигляді внесення змін у гібридизації, а також у відстань зв'язку C−C (рис.\(\PageIndex{2}\)).
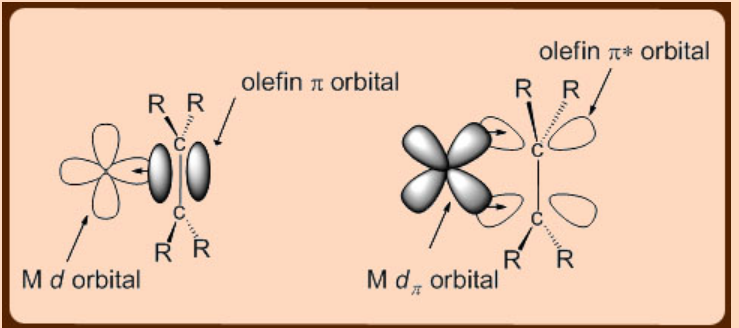
Якщо компонент донорства метал-ліганд π−назад менший, ніж ліганд до металу σ−донорство, то спостерігається подовження зв'язку C−C у зв'язаному металом олефіновому фрагмі. Це відбувається насамперед через те, що алкен до металу σ−донорство видаляє C=C π−електрони подалі від зв'язку C−C олефінового фрагмента та до центру металу, зменшуючи порядок його зв'язку та збільшуючи довжину зв'язку C−C. Крім того, у міру збільшення пожертвування металом до ліганду π−назад, посилюється електронне донорство заповненого металу d π орбіталі на π* орбіталі металевого пов'язаного олефіну. Це призводить до збільшення довжини зв'язку C−C. Подовження зв'язку C−C у зв'язаному металом олефіновому комплексі можна співвіднести з π−основністю металу. Наприклад, для слабкого π−основного металу передбачається, що подовження зв'язку C−C буде невеликим, тоді як для міцного π−основного металу подовження C−C буде значним.
Іншим наслідком донорства ліганд−металу π−назад є спостережувана зміна гібридизації на олефінових атомах С з чистого sp 2, в комплексах без металу до ліганду π−назад донорства, до sp 3, у комплексах зі значним металом до ліганду π−назад донорство, спостерігається. Зміна гібридизації від sp 2 до sp 3 центрів олефінного вуглецю супроводжується тим, що замісники трохи відігнуті від центру металу в кінцевій формі метациклопропану (рис.\(\PageIndex{3}\)). Цю зміну гібридизації можна зручно виявити за допомогою 1 Н та 13 С ЯМР-спектроскопії. Наприклад, у випадку металоциклопропанових систем, які мають міцний метал до ліганду π−назад пожертвування, вінілові протони з'являються 5 ppm (у 1 H ЯМР) та 100 ppm (у 13 C ЯМР) високе поле щодо відповідного положення вільних лігандів.
Цікавим випаданням металу з лігандним π−зворотним зв'язком є більш щільне зв'язування напружених олефінів з металевим центром, що спостерігається у випадку циклопропену та норборнену. Сильне зв'язування цих фрагментів циклопропену та норборнена з металевим центром виникає внаслідок рельєфу кільцевої деформації при зв'язуванні з металом. Нарешті, у метало-олефінових комплексах, що мають дуже мало π−зворотного зв'язуючого компонента, хімічна реакція пов'язаного з металом олефіну виявляється протилежною реакції вільного олефіну. Наприклад, вільний олефін вважається електроном багатим завдяки наявності π−електронів у його зовнішній валентній орбіталі і, отже, він піддається електрофільній атаці. Однак, пов'язані металом олефінові комплекси, що мають переважно σ−донорство олефінних π−електронів та незначну кількість металу до ліганду π−назад, олефінний С стає позитивно зарядженим і, отже, піддається нуклофільній атаці. Така природа реверсу олефіну реактивності називається umpolung характер.
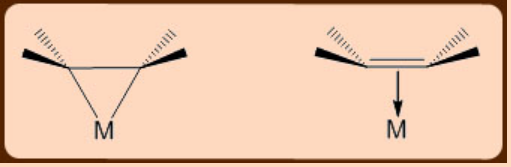
Синтез
Металеві алкенові комплекси синтезуються наступними методами.
i. заміщення в низьковалентних металах
\[\ce{AgOSO2CF3 + C2H4 -> (C2H4)AgOSO2CF3}\]
II. Зменшення високовалентного металу в присутності алкену
\[\ce{(cod)PtCl2 + C2H4 -> [PtCl3(C2H4)]- + Cl-}\]
III. Від алкілів і споріднених видів
\[\ce{Cp2TaCl3 + n-BuMgX -> {Cp2TaBu3}}\]
\[\ce{{Cp2TaBu3} ->[\Beta -elimination][reductive \: elimination] Cp2TaH(1-Butene) + Butene + Butane}\]
реакція алкенів
Металеві алкенові комплекси показують наступні реактивності.
i. Реакція вставки
Ці реакції зазвичай відображаються алкенами, коли вони вставляються в зв'язки Metal−X, утворюючи алкіли металів. Реакція відбувається легко при кімнатній температурі для X = H, тоді як для інших елементів (X = інші атоми) такі вставки стають рідкісними. Також напружені алкени та алкіни піддаються такому введенню легко.
\[\ce{PtHCl(PEt3)2 + C2H4 <=> PtElCl(PEt3)2}\]
II. Реакції Умпулунга Реакції
Умпулунга спостерігаються лише для тих метал-алкенових комплексів, для яких металевий центр є поганим π−основою і внаслідок яких олефін піддається нуклофільній атаці.
III. Окислювальну добавку
Алкени, що містять аллілові водні, піддаються окислювальному додаванню, щоб отримати комплекс аллілгідридів.
Проблеми
1. Передбачити продукт реакції.
\[\ce{AuMe(PPh3) + CF2=CF2 -> A -> B}\]
Відповідь: A = {(CF 2 = CF 2) AUME (рРН 3)} і Б = Au (CF 2 -CF 2 Ме) (рРН 3)
2. Вкажіть, чи спостерігається подовження/скорочення відстані зв'язку C−C у зв'язаному металом олефіновому фрагменту внаслідок донорства металу до ліганду π−назад?
Відповідь: Подовження.
3. Намалюйте структуру солі Зейсе.
Анс:
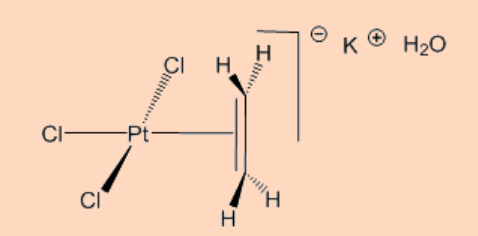
4. Зміна гібридизації при олефінному С від sp 2 до sp 3 насамперед виникає внаслідок?
Відповідь: Метал-ліганд π-назад пожертвування.
Тест на самооцінку
1. Передбачити продукт реакції.
\[\ce{PtCl2- + C2H4 ->}\]
Відповідь: [PtCl 3 (C 2 H 4)] - і Cl -
2. Вкажіть, чи спостерігається подовження/скорочення відстані зв'язку C−C у зв'язаному металом олефіновому фрагмі внаслідок донорства ліганду металу σ −?
Відповідь: Подовження.
3. Металациклопропан проміжний в металевому зв'язаному олефіновому комплексі в першу чергу утворюється завдяки якому виду взаємодії?
Відповідь: Металевий ліганд π−назад пожертвування
4. Ступінь окислення Pt в солі Зейсе є?
Відповідь: Пт II
Резюме
Алкени є важливим класом ненасичених лігандів, які зв'язуються з металом за допомогою σ−пожертвування його C = C π−електронів, а також приймає електрони з металу в його π* орбіталі зв'язку C = C. Ці симбіотичні π−донорство та π−зворотне донорство в металево-зв'язаних олефінових комплексах мають значний вплив на їх структуру та властивості реакційної здатності. Дуже важливо, що структурні прояви, що виникають внаслідок цих передніх σ- донорства та π−зворотного донорства, можна охарактеризувати за допомогою 1 H, 13 C ЯМР та ІЧ-спектроскопічних методів.
