4.7: День 33- Кислоти та основи
- Page ID
- 26583
30
День 33: Кислоти і основи
Ми застосуємо знання, які ми засвоїли досі, наприклад, термодинаміку, кінетику, молекулярну структуру тощо, щоб дослідити два поширені типи хімічних реакцій: кислотно-лужні реакції та окислювально-електрохімічні реакції.
D33.1 Визначення кислот і основ
Відповідно до кислотно-лужного визначення Brønsted-Lowry, хімічний вид, який дарує протон (іон водню, H +) іншому хімічному виду, називається кислотою, а хімічний вид, який приймає протон, є основою. (Нагадаємо, що коли атом Н втрачає електрон, залишається лише протон в ядрі, тому протон - це іон Н +.) Кислотно-лужна реакція - це перенесення протона від донора протона (кислоти) до протонного акцептора (основи).
Хімічний вид, який залишається після того, як кислота пожертвувала протон, називається кон'югатною основою цієї кислоти. Розглянемо ці приклади родової реакції кислоти + H 2 O кон'югатної основи + H 3 O +:
ВЧ + Н 2 О Ф — + Н 3 О +
Н 2 СО 4 + Н 2 О ГСО 4 — + Н 3 О +
ГСО 4 — + Н 2 О СО 4 2 - + Н 3 О + Н
4 + Н 4 + Н 2 О Н 3 + Н 3 О +
Подібним чином хімічний вид, який утворюється після того, як основа приймає протон, називається кон'югатною кислотою цієї основи. Розглянемо наступні приклади родової реакційної основи + H 2 O кон'югатної кислоти + ОН —:
Н 3 + Н 2 О Н 4 + ОН —
S 2- + Н 2 О ГС — + ОН —
СО 3 2 - + Н 2 О НСО 3 — + ОН —
Ф — + Н 2 О ВЧ + ОН —
З цих прикладів ми бачимо, що кон'югатна кислота та кон'югатна основа парні: кон'югатна основа кислоти має цю кислоту як свою кон'югатну кислоту. Наприклад, NH 3 є кон'югатною основою NH 4 +, тоді як NH 4 + - кон'югатна кислота NH 3. Аналогічно, Fє кон'югатною основою HF, тоді як HF - кон'югатна кислота F.
Можливо, ви помітили в попередніх розділах, що ми писали H + (aq) для представлення іонів водню у водному розчині, тоді як в попередніх реакціях ми писали H 3 O +. Іон H +, протон, набагато менший за будь-який інший катіон і тому є висококонцентрованим позитивним зарядом, який сильно притягує диполі молекул води і утворює міцні водневі зв'язки. Таким чином, коли кислота Бронстеда-Лоурі передає протон воді, більше, ніж одна молекула води приймає протон. Експерименти показують, що може бути задіяно цілих шість молекул води, що зробило б формулу H + (aq) H 13 O 6 +, але структура постійно змінюється, коли молекули води рухаються в рідині. Для кислотно-лужних реакцій Бронстеда-Лоурі ми будемо використовувати H 3 O + (aq), щоб підкреслити, що протон був перенесений у воду і представляти більш складну фактичну структуру. Загалом, H + (aq) доречно представляти протон, оточений багатьма молекулами води.
Нарешті, кислотно-лужні реакції Brønsted-Lowry проходять дуже швидко. Їх рівновага встановлюється швидко, і ця рівновага є важливим аспектом, коли пізніше ми розглянемо кислотні та базові сили.
D33.2 Автоіонізація води
У наведеному вище прикладі реакцій також є дві інші спряжені кислотно-лужні пари: Н 2 О є кон'югатною основою її кон'югатної кислоти Н 3 О +, а Н 2 О - кон'югатна кислота її кон'югатної основи ОН -. (Однак зауважте, що H 3 O + не є кон'югатною кислотою OH -; ці два види не є кон'югатною кислотно-лужною парою, оскільки їх структури не відрізняються одним Н +.)
Отже, H 2 O може реагувати як кислота або основа залежно від інших видів, що беруть участь у реакції. У чистій воді H 2 O діє як кислота і основа - дуже мала частка молекул води пожертвує протони іншим молекулам води:
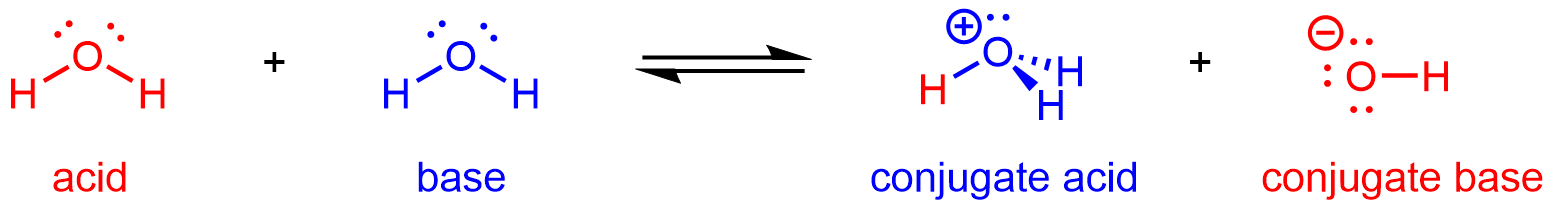
Цей тип реакції, при якій речовина іонізується, коли одна молекула речовини реагує з іншою молекулою тієї ж речовини, називається автоіонізацією.
Чиста вода піддається автоіонізації в дуже незначній мірі: лише близько двох з кожних 10 9 молекул іонізуються при 25 °С. [H 3 O +] e і [OH —] e дають константу автоіонізації для води, K w = 1,0 × 10 −14 при 25 °С, оскільки це математичний добуток концентрацій двох іонів, його також називають постійною іонного продукту для води.
Н 2 О (л) + Н 2 О (л) Н 3 О + (ак) + ОН — (ак) К ш = [Н 3 О +] е [ОН —] е = 1,0 × 10 −14 при 25 °C
Діяльність 1: Автоіонізація води
Вода є прикладом амфіпротичного хімічного виду - молекули, яка може або отримати протон, або втратити протон в кислотно-лужній реакції. Амфіпротичні види також є амфотерними, більш загальним терміном для виду, який може діяти як кислота або основа за будь-яким визначенням (а не лише визначення Бронстеда-Лоурі). Наприклад, іон бікарбонату також амфотерний:
НСО 3 — (ак) + Н 2 О (л) СО 3 2 - (ак) + Н 3 О + (ак)
НСО 3 — (ак) + Н 2 О ( л) Н 2 СО 3 (aq) + ОН — (aq)
Діяльність 2: Амфіпротичні види
D33.3 рН і pH
Концентрації H 3 O + і OH - у розчині важливі для кислотно-лужних властивостей розчину і часто впливають на хімічну поведінку інших розчинених речовин. Розчин є нейтральним, якщо його [H 3 O +] e = [ОН —] е; кислий, якщо його [H 3 O +] e > [OH —] e; і основний, якщо його [Н 3 О +] е < [ОН —] е.
Загальним засобом вираження значень, що охоплюють багато порядків, є використання логарифмічної шкали. Одна така шкала заснована на p-функції:
р X = -журнал X
де «X» - кількість відсотків, а «log» - логарифм база-10. Отже, рН розчину визначається як:
\[\text{pH}\; =\; -\text{log}\left(\dfrac{[\text{H}_3\text{O}^+]_e}{mol/L}\right) \nonumber \]
Причина ділення на одиниці «моль/л» (М) полягає в тому, що [Н 3 О +] має одиниці моль/л і приймати логарифм одиниці не має сенсу. Звідси ми будемо вважати, що ви знаєте, що лише числове значення концентрації (або іншої кількості) потрібно використовувати як аргумент логарифма, і ми не будемо явно ділити на одиниці.
Якщо відомо значення рН, то концентрацію іонів гідронію можна розрахувати:
[Н 3 О +] е = 10 -рН
Тут ми припустимо, що ви знаєте, що для концентрації, отриманої з цього рівняння, потрібні одиниці виміру, а одиниці - моль/л Аналогічно, концентрація гідроксид-іонів може бути виражена як PoH:
PoH = -лог [ОН —] е і [ОН −] е = 10 −poH
Нарешті, співвідношення між рН та pH можна вивести з виразу K w:
| К ш | = | [Н 3 О +] е [О —] е |
| -журнал (К ш) | = | -журнал ([Н 3 О +] е [ОН —] е) |
| р К ш | = | -журнал ([H 3 O +] e) + (-лог ([ОН —] е)) |
| р К ш | = | рН + pH |
При 25 °C:
р К ш = 14 = рН + pH
Тому при такій температурі:
| Класифікація | Відносні концентрації іонів | рН при 25 °C |
|---|---|---|
| кислотні | [H 3 O +] > [О −] | < 7 |
| нейтральний | [Н 3 О +] = [ОН −] | 7 |
| основні | [Н 3 О +] < [ОН −] | > 7 |
Оскільки K w залежить від температури, кореляції між значеннями рН та кислотними/нейтральні/основними прикметниками різні при різних температурах. Наприклад, [H 3 O +] в чистій воді при 80 °С становить 4,9 × 10 −7 М, що відповідає значенням рН та pH:
рН = -лог [Н 3 О +] е = -лог (4,9 × 10 −7) = 6,31
pH = -лог [ОН —] е = -лог (4,9 × 10 −7) = 6,31
При цій температурі нейтральні розчини мають рН = pH = 6,31, кислі розчини мають рН < 6.31 and pOH > 6,31, а базові розчини мають рН > 6,31 і pH < 6,31. Ця відмінність може бути важливою при вивченні певних процесів, що відбуваються при температурах, відмінних від 25° C, таких як кислотно-лужні реакції в організмі людини, де температура зазвичай становить 37° C.
Якщо не зазначено інше, посилання на значення рН вважаються значеннями при 25° C. Рисунок 1 показує співвідношення між [H 3 O +], [OH −], pH та pH та дає значення цих властивостей для деяких поширених речовин.
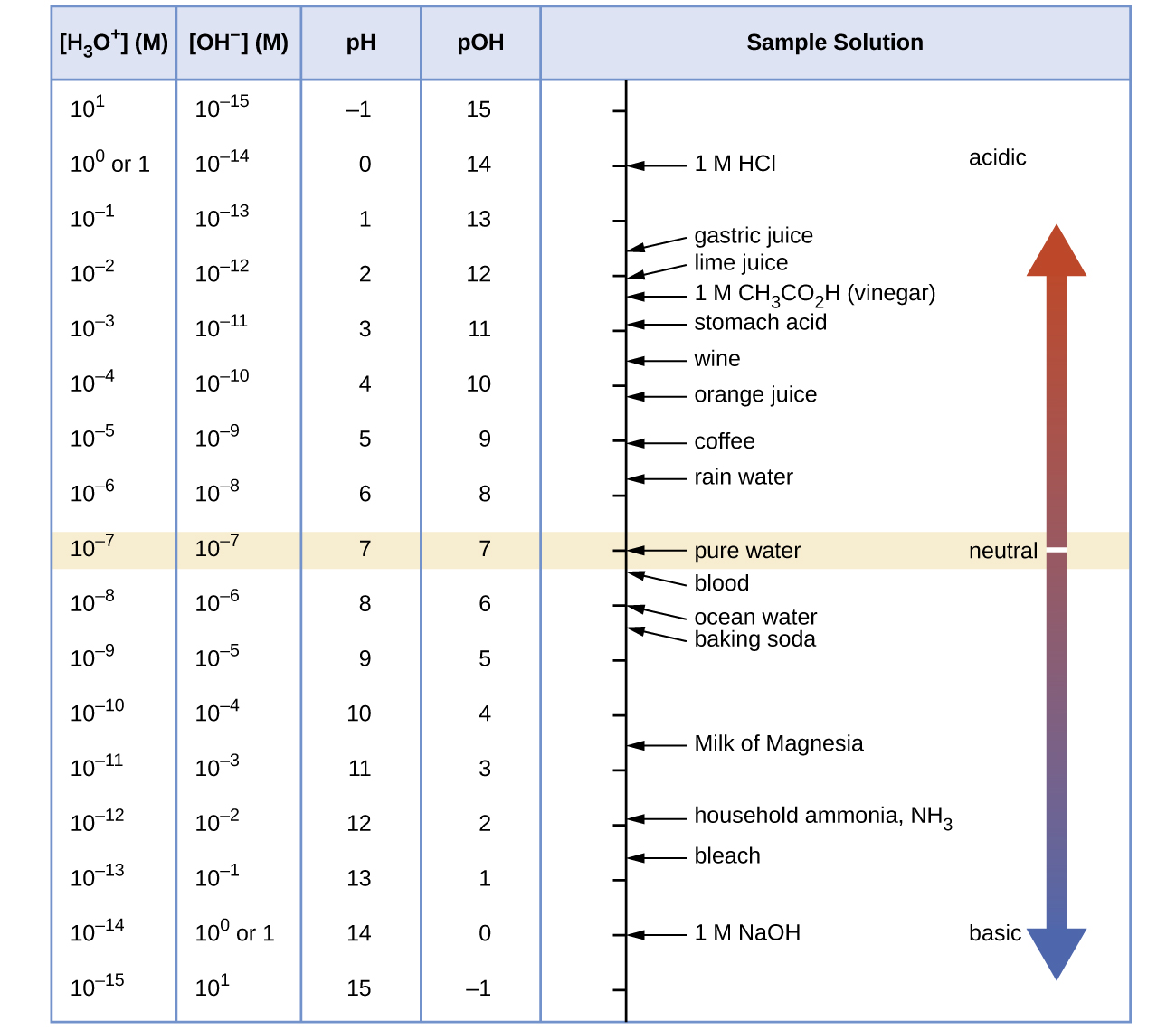
Діяльність 3: рН та відносна сила кислот
Кислотність розчину зазвичай визначається шляхом вимірювання його рН. PoH розчину зазвичай не вимірюється, але він легко обчислюється з експериментально визначеного значення рН. РН розчину можна безпосередньо виміряти за допомогою рН-метра (рис. 2), або візуально оцінити за допомогою кольорових індикаторів (рис. 3).

 Малюнок 3. Універсальним показником є суміш показників, що передбачає різний колір при різних значеннях рН. (а) Універсальний індикатор був доданий до розчинів у десяти пробірках, кожна з яких pH показаний у верхній частині кожної трубки. (б) pH папір містить інший універсальний показник, який дає різні кольори при зволоженні розчинами різних значень рН. Шкала вгорі показує кольори для парних значень рН від 2 до 10.
Малюнок 3. Універсальним показником є суміш показників, що передбачає різний колір при різних значеннях рН. (а) Універсальний індикатор був доданий до розчинів у десяти пробірках, кожна з яких pH показаний у верхній частині кожної трубки. (б) pH папір містить інший універсальний показник, який дає різні кольори при зволоженні розчинами різних значень рН. Шкала вгорі показує кольори для парних значень рН від 2 до 10.
D33.4 Кислотна постійна K a і базова постійна K b
Відносні сили кислот і підстав можна визначити шляхом порівняння констант рівноваги для їх реакцій іонізації. Для реакції родової кислоти, ГК, у воді:
ГА (ак) + Н 2 О (л) А — (ак) + Н 3 О + (aq)
запишемо константу іонізації кислоти (K a) вираз як:
\[K_{\text{a}} = \dfrac{[\text{H}_3\text{O}^{+}]_e[\text{A}^{-}]_e}{[\text{HA}]_e} \nonumber \]
(Хоча вода є реагентом у реакції, вона також є розчинником, фаза якого вказана як «л «, тому ми не включаємо [H 2 O] у вираз.)
Кислота з більшим K a мала б більшу концентрацію H 3 O + і A − відносно концентрації неіонізованої кислоти, HA. Таким чином, сильніша кислота, яка іонізується більшою мірою, має більшу постійну іонізації, ніж слабша кислота.
Наприклад, ці дані про константи кислотної іонізації:
| СН 3 СООН (кв) + Н 2 О (л) | ⇌ | СН 3 СОО — (ак) + Н 3 О + (ак) | К а = 1,8 × 10 -5 |
| ННО 2 (ак) + Н 2 О (л) | ⇌ | НІ 2 — (ак) + Н 3 О + (ак) | К а = 7,4 × 10 -4 |
| ГСО 4 — (ак) + Н 2 О (л) | ⇌ | СО 4 2 - (ак) + Н 3 О + (ак) | К а = 1,1 × 10 -2 |
вказують на те, що порядок міцності кислоти такий: оцтова кислота (CH 3 COOH) є слабшою кислотою, ніж азотна кислота (HNO 2), яка сама по собі слабша, ніж іон сульфату водню (HSO 4 -).
Ми можемо розглянути міцність основи (B) аналогічно, враховуючи розширення, що вона буде утворювати гідроксидні іони у водному розчині:
B (aq) + Н 2 О (л) НВ + (ак) + ОН — (aq)
де базова константа іонізації (K b) вираження дорівнює:
\[K_{\text{b}} = \dfrac{[\text{HB}^{+}]_e[\text{OH}^{-}]_e}{[\text{B}]_e} \nonumber \]
Більш сильна основа іонізується більшою мірою, ніж робить слабша основа. Тому більш міцна основа має більший K b, ніж більш слабке підставу.
Зверніть увагу, що K a і K b забезпечують кількісний показник міцності кислоти та основи - значно більш точні, ніж якісні описи «сильної кислоти» або «слабкої кислоти».
Розглянемо реакції іонізації для кон'югатної пари кислотної основи, HA і A −:
ГА (ак) + Н 2 О (л) А — (ак) + Н 3 О + (aq)
\[K_a = \dfrac{[\text{H}_3\text{O}^{+}]_e[\text{A}^-]_e}{[\text{HA}]_e} \nonumber \]
А — (ак) + Н 2 О (л) ГА (ак) + ОН — (aq)
\[K_b = \dfrac{[\text{HA}]_e[\text{OH}^-]_e}{[\text{A}^-]_e} \nonumber \]
Додавання цих двох хімічних рівнянь дає рівняння для автоіонізації води:
ГА (ак) + Н 2 О (л) + А — (ак) + Н 2 О (л) A — (aq) + Н 3 О + (aq) + ГА (aq) + ОН — (aq)
Коли дві рівноваги підсумовуються до третьої рівноваги, добуток перших двох констант рівноваги дорівнює третій константі рівноваги:
\[K_{\text{a}}\;\times\;K_{\text{b}} = \dfrac{[\text{H}_3\text{O}^{+}]_e[\text{A}^{-}]_e}{[\text{HA}]_e}\;\times\;\dfrac{[\text{HA}]_e[\text{OH}^{-}]_e}{[\text{A}^{-}]_e} = [\text{H}_3\text{O}^{+}]_e[\text{OH}^{-}]_e = K_{\text{w}} \nonumber \]
Наприклад, при 25° С К а оцтової кислоти (СН 3 СООН) становить 1,8 × 10 −5 М, а К б її кон'югатної основи, ацетатного аніона (СН 3 СОО —), становить 5,6 × 10 −10 М. Твір цих двох констант дійсно дорівнює K w:
К а × К б = (1,8 × 10 −5 М) × (5,6 × 10 −10 М) = 1,0 × 10 −14 = К ш
Цей зв'язок говорить нам про те, що сильніші кислоти утворюють слабші кон'югатні основи, а слабші кислоти утворюють більш міцні кон'югатні основи.
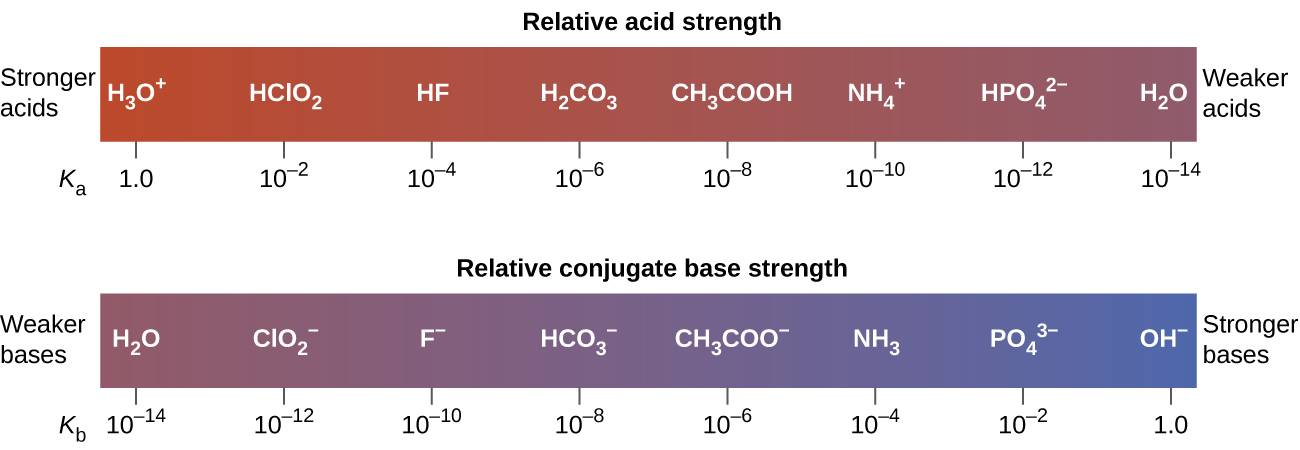
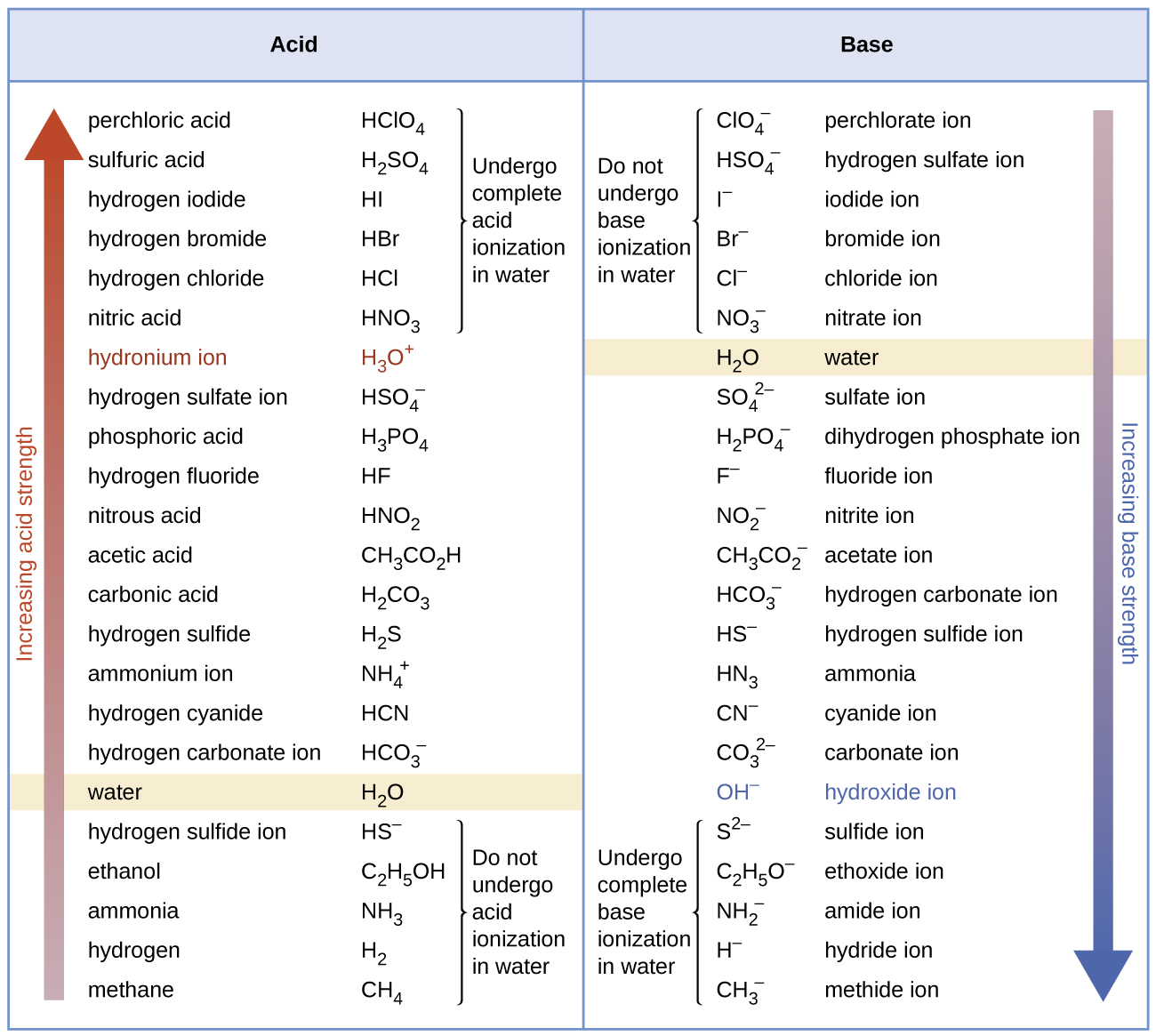
Хоча «сильні» і «слабкі» є відносними термінами, як правило, ми називаємо кислоти сильніші за H 3 O + сильними кислотами, а основи сильніші за ОН - сильними основами. Оскільки сильні кислоти і сильні основи повністю іонізуються у водних розчині, концентрація неіонізованої кислоти або основи по суті дорівнює нулю. Наприклад, в 0,10-М розчині HCl [HCl] е = 0, [H 3 0 +] e = 0,10 М, а [Cl −] е = 0,10 М.
Наслідком такої повної іонізації є те, що у водному розчині немає можливості сказати, чи одна сильна кислота сильніша за іншу: HCl, HBr і HI все повністю іонізовані. Це відомо як вирівнюючий ефект води. Однак при розчиненні в деяких інших розчинниках ці кислоти не іонізуються повністю. Ступінь іонізації збільшується в порядку HCl < HBr < HI, і тому HI є найсильнішою з цих кислот. Вода надає подібну вирівнюючу дію на міцних підставах.
Багато кислоти і основи вважаються «слабкими». Розчин слабкої кислоти у воді являє собою рівноважну суміш неіонізованої кислоти, іона гідронію і кон'югатної основи кислоти.
Діяльність 4: Визначення Ка
Діяльність 5: Використання Ka для обчислення концентрацій
Відсоток іонізації слабкої кислоти - ще одна міра сили кислоти, ГК:
\[\text{percent ionization} = \dfrac{[\text{H}_3\text{O}^{+}]_e}{[\text{HA}]_0}\;\times\;100\% \nonumber \]
Більш сильна кислота, з більш високим К а, має більш високий відсоток іонізації, ніж більш слабка кислота (при тій же концентрації).
Відсоток іонізації для розчину слабкої кислоти збільшується зі зменшенням концентрації кислоти; це можна побачити, застосувавши принцип Ле Шательє до іонізаційної рівноваги:
ГА (ак) + Н 2 О (л) А — (ак) + Н 3 О + (aq)
Збільшення об'єму розчину для заданої кількості доданої ГК призводить до зміщення рівноваги в сторону продукту, щоб частково протидіяти зменшенню загальної концентрації розчиненої речовини.
D33.5 Сила кислоти та молекулярна структура
Кислотно-лужні реакції, як і багато інших хімічних реакцій, передбачають розрив і формування зв'язків. Отже, ми можемо використовувати наше хімічне розуміння молекулярної структури та стабільності, щоб зрозуміти, що робить деякі кислоти сильнішими за інші.
Ми знаємо, що рівновага сприяє термодинамічно більш стабільній стороні реакції, і що величина постійної рівноваги відображає різницю енергії (Δ r G°) між реагентами та продуктами. Тому в кислотно-лужній рівновазі рівновага завжди сприяє стороні зі слабшою кислотою та основою (це більш стійкі види). Отже, все, що стабілізує кон'югатну основу кислоти, обов'язково зробить цю кислоту сильнішою, і все, що стабілізує кислоту, зробить її слабшою кислотою. Ця ідея проілюстрована на малюнку 6.
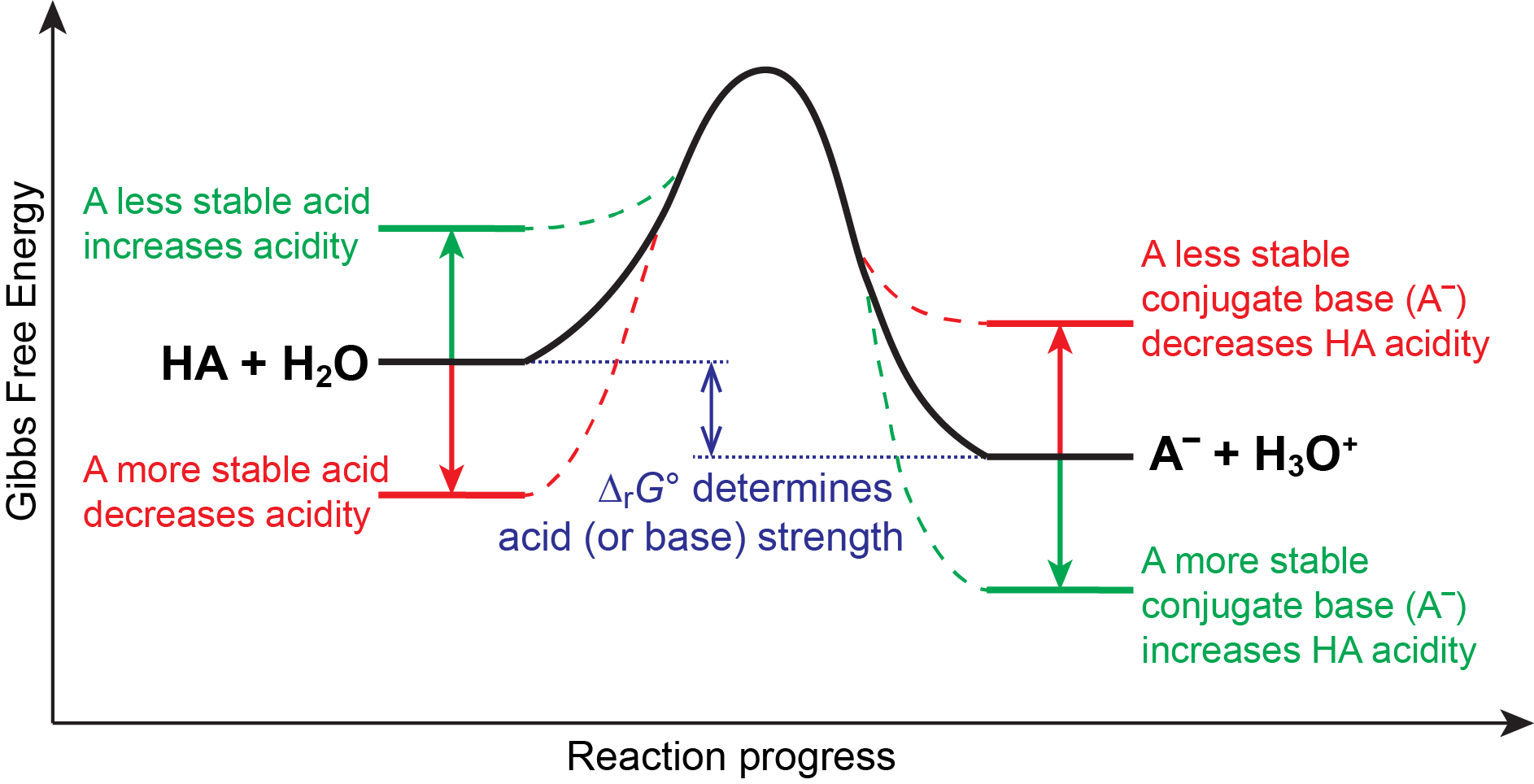
Міцність зв'язку
Розглянемо дженерик кислоти:
ГА А — + Н +
Загалом, чим міцніше зв'язок H—A, тим стабільнішою є молекула ГК, і тим менш кислою є речовина. Цей ефект ілюструють галогеніди водню:
| Відносна сила кислоти | HF | HCl | HBr | ПРИВІТ |
|---|---|---|---|---|
| Ентальпія зв'язку H—X (кДж/моль) | 566 | 431 | 366 | 299 |
| р К а | 3.2 | −6.1 | −8.9 | −9.3 |
Зверніть увагу, що значення «ентальпії зв'язку» пов'язані з іншою реакцією розриву зв'язку, яка виробляє атом водню замість іона водню:
ГА А· + Ч·
Тим не менш, міцність зв'язку корелює з кислотною міцністю. Коли ви йдете вниз по галогенідній групі, перекриття між орбіталлю водню 1 с і валентною орбіталлю атома галогену зменшується, а ентальпія зв'язку H-X зменшується, що вказує на слабші зв'язки. В результаті, HX кислотна сила збільшується, як ви йдете вниз групи.
Аналогічна тенденція спостерігається і для інших груп. Наприклад, для групи 16:
| Н 2 А ГА — + Н + | ||||
| Н 2 О | Н 2 С | Н 2 Сб | Н 2 Чт | |
| р К а | 14,0 | 7.0 | 3.9 | 2.6 |
Стабілізація надлишкового заряду на сполученій основі
Електронегативність
Коли кон'югатна основа негативно заряджена, фактори, які стабілізують надлишок негативного заряду на кон'югатній основі, сприяють дисоціації кислоти і роблять кислоту сильнішою кислотою. Наприклад, відносна кислотність кислот з елементами другого ряду становить:
| Н Н А Н Н Н -1 А — + Н + | ||||
| СН 4 | NH 3 | Н 2 О | ВЧ | |
| р К а | 50 | 36 | 14,0 | 3.2 |
Розглянемо сполуки на обох кінцях цієї серії: метан і фтористий водень. Сполученим підставою СН 4 є СН 3 -, а сполучена основа HF - F -. Оскільки фтор набагато більш електронегативний, ніж вуглець, фтор може краще стабілізувати додатковий негативний заряд в F − аніоні, ніж вуглець може стабілізувати додатковий негативний заряд в CH 3 − аніон. Отже, HF може дисоціювати і утворювати H + і F - набагато більшою мірою, ніж СН 4 може утворювати Н + і СН 3 -, що робить HF набагато сильнішою кислотою, ніж CH 4.
Така ж тенденція прогнозується і при аналізі кислот: у міру збільшення електронегативності A в H n A зв'язок A—H стає більш полярним, сприяючи дисоціації з утворенням H n-1 A − і H +. Завдяки збільшенню стабільності кон'югатної основи і зростаючій поляризації зв'язку A—H в кислоті кислотні сили бінарних гідридів збільшуються, коли ми йдемо зліва направо через ряд періодичної таблиці.
Делокалізація електронів
Значення p K a деяких карбонових кислот показані на малюнку 7.
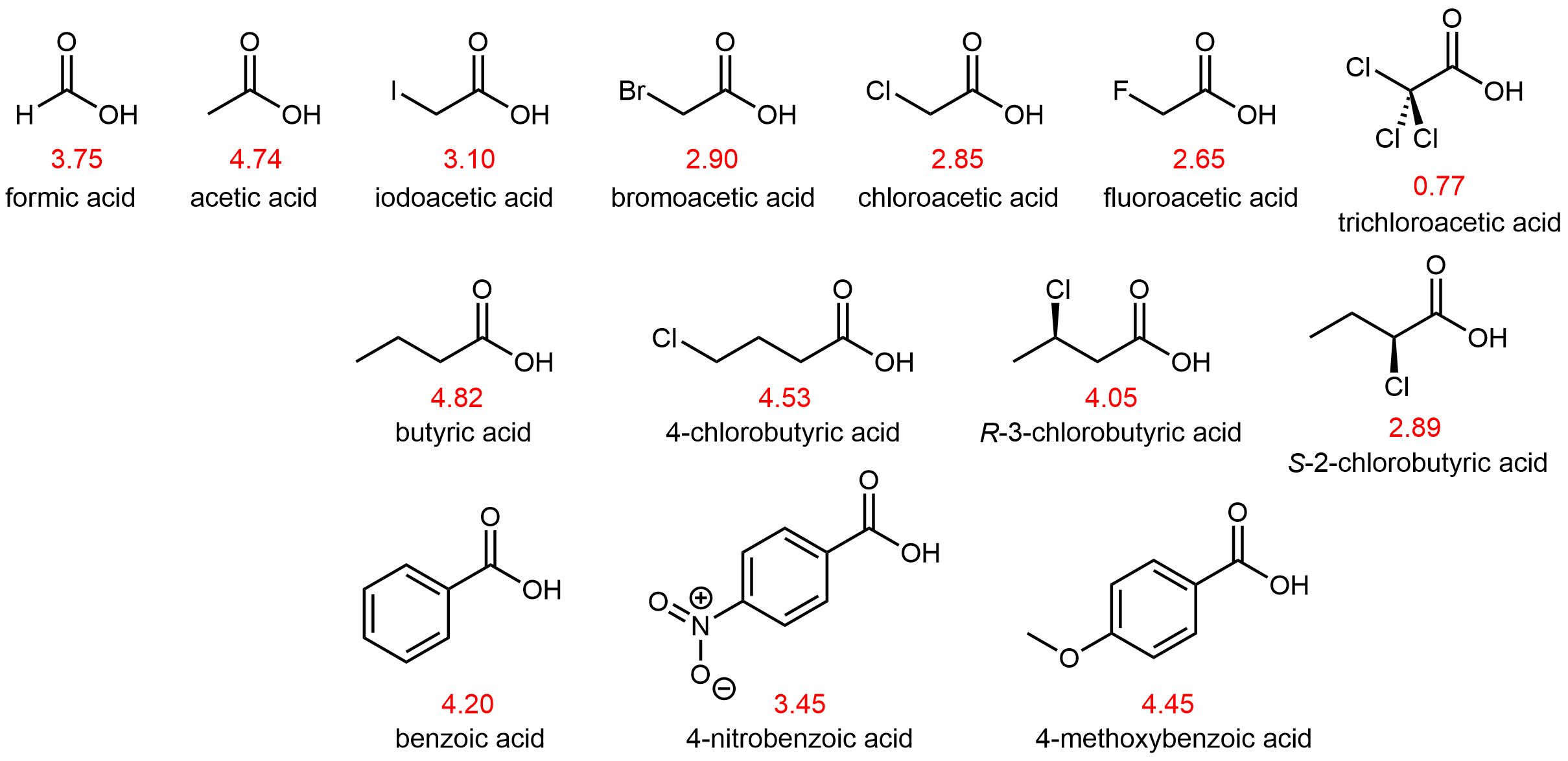
Зв'язок, який розривається в карбонової кислоти, - це зв'язок O—H:
Р-СООН Р-СОО+ Н +
Зв'язок O—H також розривається, коли спирт діє як кислота в кислотно-лужній реакції:
Р-ОН Р-О+ Н +
Однак, коли ми порівнюємо карбонову кислоту р К а з аналогічними спиртами, такими як:

зрозуміло, що карбонові кислоти є більш сильними кислотами, ніж спирти більш ніж на десять порядків. Чому наявність карбонільної групи, прилеглої до гідроксильної групи, має надавати такий глибокий вплив на кислотність гідроксильного протона?
Як карбонова кислота, так і її кон'югатна основа, карбоксилатний аніон, стабілізуються, маючи додаткові резонансні структури, що делокалізують електронні щільності. Однак стабілізація в карбоксилатному аніоні набагато більша, оскільки дві основні резонансні структури мають однаковий внесок у резонансний гібрид, а додаткова електронна щільність (негативний заряд) розподіляється порівну між двома атомами кисню, які мають високу електронегативність. Така стабілізація призводить до помітно підвищеної кислотності карбонових кислот.
Індуктивний ефект
Атоми (або групи атомів) в молекулі, які безпосередньо не пов'язані з кислим Н, також можуть впливати на кислотність молекули. Вони можуть зробити це за допомогою індуктивного ефекту, тобто індукують поляризацію в розподілі електронів всередині молекули. У цьому можна переконатися, вивчивши структури на малюнку 7 вище. Електронегативні замінники (F, Cl, Br, I) поблизу карбоксильної групи діють на підвищення кислотності карбонової кислоти. Наприклад, фтороцтова кислота, СН 2 ФСООН, значно більш кисла, ніж оцтова кислота, СН 3 СООН.
Величина індуктивного ефекту залежить як від природи, так і від кількості галоген-замінників, що показують значення р К а для декількох похідних оцтової кислоти:
| СН 3 СООН | СН 2 КЛ СООН | CHCl 2 СООН | CcL 3 СООН | CF 3 КУН | |
| р К а | 4.74 | 2.85 | 1.35 | 0,77 | 0,52 |
Фтор, який є більш електронегативним, ніж хлор, викликає більший індуктивний ефект, оскільки він відтягує електронну щільність від кислого протона в карбоксильній групі. Більш того, наявність трьох галогенів викликає більший індуктивний ефект, ніж наявність двох або одного. Відзначимо, що індуктивні ефекти можуть бути досить значними. Наприклад, заміна групи оцтової кислоти —CH 3 групою —CF 3 призводить до збільшення кислотності майже в 10 000 разів.
В іншому прикладі кислотність гіпогалових кислот (HOX OX+ H +) змінюється приблизно на три порядки за рахунок різниці електронегативності атомів галогену:
| КОРОБКА | Електронегативність X | пКа |
|---|---|---|
| HOCl | 2.73 | 7.2 |
| HoBr | 2.64 | 8.5 |
| ХОЙ | 2.11 | 10.5 |
Зі збільшенням електронегативності X електрони тягнуться сильніше до атома галогену і, в свою чергу, подалі від H у зв'язку O—H, тим самим послаблюючи зв'язок O—H, посилюючи іонізацію водню як H + і роблячи кислоту сильнішою.
Оксокислоти
Кислотність оксокислот при загальній формулі HOXO n (з n = 0−3) сильно залежить від кількості кінцевих атомів кисню, прикріплених до центрального атома X (рис. 8) внаслідок як індуктивного ефекту, так і підвищеної стабілізації сполученого підстави.
Оскільки кисень є другим найбільш електронегативним елементом, додавання термінальних атомів кисню (атоми кисню, з'єднані лише з центральним атомом) призводить до відведення щільності електронів від зв'язку O—H, тим самим збільшуючи міцність кислоти. На малюнку 9 показано, як атом Н стає стабільно більш синім від HClO до HClO 4, що полегшує кислоту втрачати водень як іон H +.
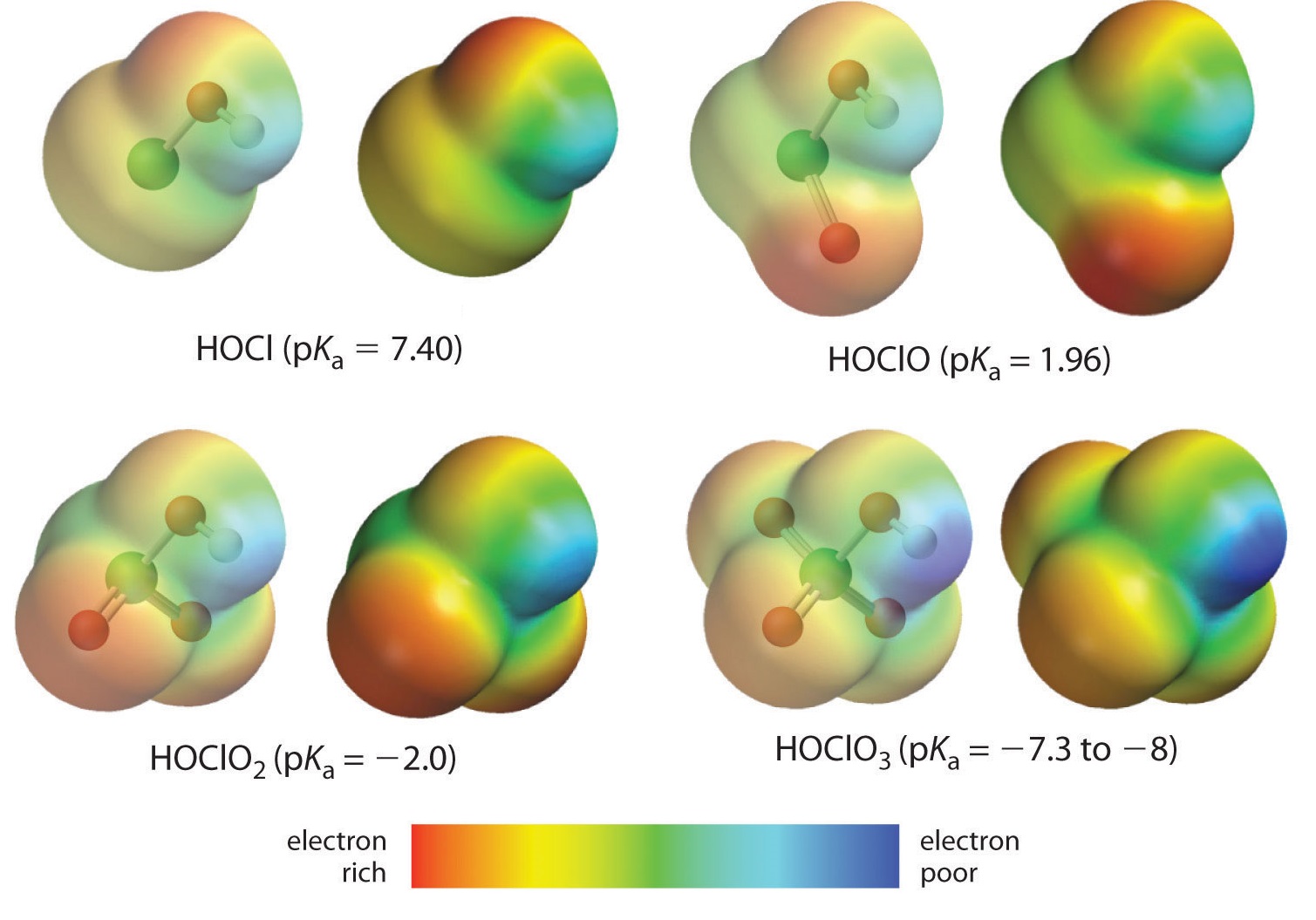
Також важливим є ефект делокалізації електронів, що стабілізує зайвий негативний заряд в сполученому підставі. Наприклад, в аніоні хлориту (ClO 2) надлишкова електронна щільність делокалізована однаково над обома атомами кисню, тоді як в іоні гіпохлориту (ClO −) негативний заряд значною мірою локалізується на одному атомі кисню:
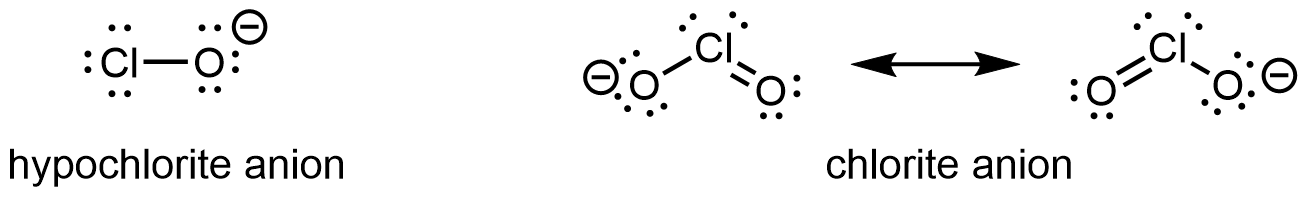
В результаті такої стабілізації кон'югатної основи, а також додаткового індуктивного ефекту хлорноватиста кислота більш ніж в 200 000 разів сильніше хлорноватистої кислоти.
Індуктивний ефект додатково відповідає за тенденцію в кислотності оксокислот, які мають таку ж кількість атомів кисню, як ми йдемо через ряд періодичної таблиці. Наприклад, H 3 PO 4 - слабка кислота, H 2 SO 4 - сильна кислота, а HClO 4 - одна з найсильніших відомих кислот. Кількість кінцевих атомів кисню неухильно збільшується по всьому ряду, що відповідає спостережуваному підвищенню кислотності. Крім того, електронегативність центрального атома неухильно зростає від P до S до Cl, що спричиняє витягування більшої щільності електронів з групи OH до центрального атома, послаблюючи зв'язок O—H та збільшуючи міцність оксокислоти.
Подія Питання
Розставляють ці кислоти в порядку зменшення кислотної сили (найменший р К перший, найбільший р К останній). Проаналізуйте фактори, що впливають на силу кожної кислоти, і на основі цього аналізу поясніть порядок кислотності.
СН 3 СН 2 ОН СФ 3 СООН ХОКЛО 3 СН 2 БРСООН ХОКЛО 2
За два дні до наступного сеансу цілого класу це питання Podia стане в прямому ефірі на Поді, де ви зможете подати свою відповідь.
