5.3: Конкретні заміни
- Page ID
- 21194
Альтернативні стратегії реагентів
Видалення лактози
Можливість видалення лактози за допомогою процесу поділу може бути досягнута шляхом приєднання глутаральдегіду (дві кінцеві альдегідні групи нижче, зліва) до амінованої частинки кремнезему (зображення праворуч), яка потім ковалентно пов'язана з ферментом галактозидази, який може бути використаний для видалення лактози з молочних продуктів з подальшим зчепленням з галактозидазою і реакцією з молоком.
Кватернізація амінів
Катіони четвертинного амонію, квати, є позитивно зарядженими іонами структури, наведеної нижче:
Група R може бути алкільною групою або аріловою групою. На відміну від амонію (NH 4 +), катіони четвертинного амонію постійно заряджені, незалежно від рН.
Комбінаторна хімія
Комбінаторна хімія - це підхід до хімічного синтезу, який дає можливість отримання великої кількості (наприклад, мільйонів) сполук за одну розгортку. Ці бібліотеки можуть бути сумішами, окремими сполуками або обчислювальними структурами.
Комбінаторна хімія може бути використана для малих молекул, а також для біомакромолекул, таких як пептиди. Синтез може швидко привести до великої кількості продуктів. Як приклад, молекула з трьома точками функціональності або різноманітності (R 1, R 2 і R 3) може генерувати структури, де N R# = числа різних використовуваних замісників. Основним принципом комбінаторної хімії є отримання великої кількості сполук, які потім використовуються для ідентифікації корисних компонентів бібліотек.
Хоча комбінаторна хімія була в грі протягом останніх 25 років, її коріння йдуть до 1960-х років, коли дослідник Рокфеллера, Брюс Мерріфілд, почав досліджувати твердофазний синтез пептидів. Він мав найбільший вплив у фармацевтичній промисловості, де дослідники оптимізують профіль активності сполуки, створивши бібліотеку багатьох різних, але споріднених сполук.
Крохмаль
Крохмаль - біоматеріал, що накопичує енергію, що утворюється з вуглекислого газу і води під час фотосинтезу. Серед широкого спектру природних полімерів крохмаль представляє значний інтерес через його біорозкладність, низьку вартість, відновлюваність та біосумісність. Тому вважається перспективним кандидатом на сталий розвиток нових функціональних матеріалів.
Крохмаль складається з двох гомополімерів D-глюкози: амілази, практично лінійного α-D- (1, 4') - глюкан, і розгалуженого амілопектину, з багатьма α-1, 6'-зв'язаними точками гілок (рис.\(\PageIndex{4}\)).
Крохмаль є поліолом: він має, отже, дві вторинні гідроксильні групи при С-2 і С-3, і один первинний гідроксил при С-6, коли він не пов'язаний. Він також досить гідрофільний і може окислюватися і відновлюватися для утворення ефірів і ефірів і багатьох інших функціональних молекул. Крохмаль має різні пропорції амілози і амілопектину приблизно з 10— 20% амілози і 80— 90% амілопектину на основі джерела. Він утворює гвинтову структуру і відбувається природно як дискретні гранули, оскільки коротко розгалужені ланцюги амілопектину можуть утворювати гвинтові структури для кристалізації. Він має МВт 500-20K, що складається з a- (1à4) -D-глюкозних одиниць, розширена форма яких має гідродинамічний радіус 7-22 нм. Спіральна форма молекули зазвичай утворює жорстку ліву єдину спіраль, структура якої, не на відміну від ДНК, підтримується H-зв'язком між атомами O2 та O6. Амілоза може піддаватися синерезису (синтезу зневоднення) між віцинальними (сусідніми) залишками глюкану, утворюючи порожнину циклодекстрину, в якій внутрішня частина підтримує гідрофобність. Цікаво, що він може утворювати двожильні кристаліти, стійкі до амілази (передбачуваного ферменту для її деконструкції), а також H-зв'язку та розчинності. Короваюча макромолекула з крохмалю, CD, - справжня зелена аптечна мрія завдяки ряду чудових властивостей. Нижче показана тороїдальна структура CD і розміри:
Як циклодекстрини роботи? https://www.youtube.com/watch?v=UaEes6cJu7k (Як працюють циклодекстрини? (1980). Циклолаб.)
Зокрема, це циклічний олігомер A-D-глюкопіранози, що утримується глікозидними зв'язками, дуже схожим на те, що спостерігається у всіх полісахаридах. Він був відкритий в 1891 році Вільє, який синтезував шляхом ферментативного перетворення амілози з подальшим селективним осадженням. Опади можуть проводитися декількома розчинниками, нехай і органічними за своєю природою і не стійкими, але з різним ступенем врожайності. Зверніть увагу, що ми розглянемо три форми компакт-дисків, як показано на графіку нижче:
| Осаджуючий агент | Вихідність (%) | |
| a- компакт-диск | 1-деканол | 40 |
| б- компакт-диск | толуолу | 50-60 |
| g -CD | Циклогексадек-8-ен-1-ол | 40-50 |
Що примітно в компакт-дисках, так це їх здатність формувати комплекси включення хоста/гостя завдяки унікальним критеріям HLB (гідрофільний ліпофільний баланс). Це досить буквально молекулярномасштабні реактори, які можуть робити багато речей. У контексті біомедичних застосувань, в центрі уваги нашої конкретної дискусії, наступні є одними з їх переваг.
- Для підвищення водної розчинності лікарських засобів
- Для підвищення хімічної стабільності лікарських засобів
- Для посилення доставки ліків до біологічних мембран та через них
- Для підвищення фізичної стабільності препаратів
- Для перетворення рідких препаратів в мікрокристалічні порошки
- Для запобігання взаємодії наркотиків та наркотиків та допоміжних речовин
- Для зменшення місцевого подразнення після місцевого або перорального застосування
- Для запобігання всмоктування препарату в шкіру або після прийому всередину
Нанореактори мають надзвичайну здатність інкапсулювати та/або робити хімію з низкою хімічних речовин, які є гідрофобними або низькою полярністю. На малюнку 5-9 зображений мультфільм, який зображує гідролітичну дію CD з молекулою фосфату.
Малюнок\(\PageIndex{6}\): Спрощене уявлення про інкапсуляцію та хімічну реакційну поведінку макромолекули CD для гідролізу фосфатів. https://commons.wikimedia.org/wiki/F...ease_Mimic.png
CD може в силу сортів за своїми розмірами вмістити відносно малі до великих гостьових молекул. На малюнку 5-10 показано наочний опис комплексу гость:хост 1:2, який бере участь у фотофізичній поведінці.
Система бере участь у передачі енергії від периферичних боросодержащих молекул до інкапсульованих молекул порфірину, який вивільняє фотон світла при резонансній передачі енергії (645 нм) від периферичних молекул.
Діаграми розчинності фаз
Дослідження фазової розчинності проводяться у водних системах при різних температурах для розрахунку постійних стабільності (рівноваги), (К с) і термодинамічних значень для утворення комплексів включення. Відомо, що якщо діаграми фазової розчинності показують, що розчинність молекули гостя зростає лінійно разом з концентрацією CD, то їх можна розглядати як фазові діаграми типу AL-типу [1], що припускають утворення комплексів 1:1, які є найбільш поширеними і найбільш зрозумілими з цих типів взаємодій. Коли дані фазової розчинності збираються при різних температурах, ми можемо отримати цінну додаткову інформацію, таку як термодинамічні параметри для формування комплексу.
Інтегрована форма рівняння Ван Гоффа дозволяє обчислити ентальпію (DH) та ентропії (DS) залежно від варіацій констант стійкості з температурою [2]:
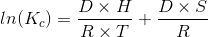
K c також може бути виражений у вигляді наступного співвідношення:
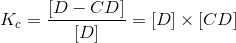
які можна наочно описати як:
при якому є комплексоутворення з D (субстратом або препаратом в даному випадку) і CD. Вищезазначене являє собою комплекс типу AL-типу, який є першим порядком щодо CD та препарату (D).
Профілі фазорозчинності типу А визначаються розчинністю субстрату (препарату), що збільшується зі збільшенням концентрації ліганду (циклодекстрину). Коли комплекс знаходиться в першому порядку відносно ліганду і першого або вищого порядку по відношенню до підкладки, то отримують профілі фазорозчинності типу A L. Якщо комплекс першого порядку по відношенню до субстрату, але другого або вищого порядку по відношенню до ліганду, отримують A P -типи. Профілі фазорозчинності типу N важко інтерпретувати. Профілі фазорозчинності B-типу свідчать про утворення комплексів з обмеженою розчинністю у водному середовищі. Водорозчинні похідні циклодекстрину утворюють профілі фазорозчинності типу А, тоді як менш розчинні циклодекстрини утворюють профілі B-типу. Ряд лікарських/циклодекстринових комплексів утворюють комплекси включення, алециклодекстрини утворюють комплекси невключення і агрегати, які розчиняють ліки через міцеллоподобние структури. Профілі фазорозчинності не перевіряють комплекси включення, а лише описують, як підвищення концентрації циклодекстрину впливає на розчинність препарату. Як ми вже обговорювали, найпоширенішим типом комплексів циклодекстрину є 1:1, де одна молекула препарату (D) утворює комплекс з однією молекулою циклодекстрину (CD). У діаграмі фазорозчинності типу AL, де нахил менше одиниці, постійну стабільності (K 1:1) комплексу можна обчислити з нахилу та внутрішньої розчинності (S0) препарату у водному середовищі (тобто розчинність препарату, коли немає циклодекстрину):
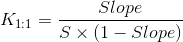
Значення К 1:1 зазвичай становить 50 < 2000 М -1 із середнім значенням 129, 490 та 355 М -1 для α-, β- і γ- циклодекстрину відповідно [3].