9.1: H₂ O - проста формула, чудова молекула
- Page ID
- 18957
Вода становить гідросферу, яка описана і розглянута в розділі 8.2. Ця глава розширює цю дискусію та вирішальну роль води в навколишньому середовищі. У цьому розділі та в інших місцях книги термін природна вода використовується для посилання на воду, яка зустрічається в навколишньому середовищі порівняно з водою в антросфері, наприклад, водою в муніципальних водорозподільних системах. Вода займає особливе місце в живих організмах і навколишньому середовищі. Якість та доступність води мають першорядне значення для людини та навколишнього середовища. Незважаючи на дефіцит і погано забруднена у багатьох куточках світу, вода, мабуть, є найбільш підлягають вторинній переробці з речовин, що складають зелений капітал Землі, і вона точно описується як кінцева зелена речовина.
У цій главі розглядаються основні аспекти стійкості води. Перший з них - забруднення води, яке погіршує якість води і може зробити її непридатною для використання або підтримки життя. Друга основна область розглянута - це те, як якість води можна підтримувати та покращувати, головним чином за допомогою різних процесів очищення води. Третя велика область - запобігання забрудненню води, а четверта - переробка водного ресурсу, який, мабуть, є найбільш переробленим матеріалом природи.
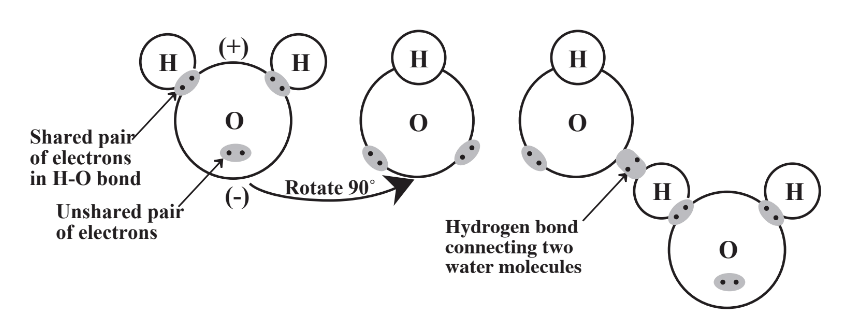
Хімічна формула води H 2 O, мабуть, найвідоміша з усіх сполук. Ця проста формула являє собою унікальне і складне в своїй поведінці речовина. Ці особливі властивості обумовлені молекулярною структурою молекули H 2 O, представленої на малюнку 9.1. У зовнішній електронній оболонці атома О в молекулі Н 2 О є чотири пари електронів, дві з яких складають зв'язки між атомами Н і О і дві з яких - одиночні пари. Розподіл цих пар якомога далі один від одного навколо уявної сфери, що представляє зовнішню електронну оболонку атомів O, призводить до того, що дві зв'язки H-O розташовані під кутом, а не прямою лінією. Сторона молекули з двома атомами Н має частковий позитивний заряд, а сторона з двома незв'язними парами має частковий негативний заряд, тому молекула полярна. Ця полярність і здатність атомів Н на одній молекулі утворювати водневі зв'язки з атомами O на інших молекулах визначають чудове хімічне і фізичне різноманіття води.
Особливо через свою здатність склеювати водню молекули води сильно притягуються один до одного. Це означає, що велика кількість теплової енергії повинна бути покладена в масу води, щоб дозволити молекулам рухатися швидше при підвищенні температури. Це дає воді дуже високу теплоємність. Дуже велика кількість енергії необхідно покласти в масу льоду, щоб розірвати водневі зв'язки, що утримують молекули на місці в твердій речовині, коли вона тане, і однаково велика кількість теплової енергії виділяється при замерзанні рідкої води. При цьому вода має дуже високу приховану теплоту плавлення. Ще більше енергії на одиницю маси потрібно для перетворення рідкої води в пару (пар) і рівну кількість енергії виділяється при конденсації водяної пари в рідину. Це означає, що вода має дуже високу теплоту випаровування.
Здатність води поглинати, виділяти та зберігати тепло має вирішальне значення для її ролі в навколишньому середовищі та її практичному застосуванні. 1 Висока теплоємність води стабілізує температуру організмів і географічних районів. Пара, що утворюється в котлі, може передаватися по ізольованих трубах у віддалені місця і конденсуватися для виділення тепла. Тепло, що виділяється при конденсації атмосферної води, зігріває навколишнє повітря і є рушійною силою тропічних штормів. Європа зобов'язана своєю відносно м'якою погодою, незважаючи на північні широти, теплом, що переноситься водою через Північний Атлантичний океан з Мексиканської затоки. Оскільки вода виділяє тепло і охолоджується вздовж європейських берегів, її щільність збільшується, і вона тече на нижніх океанських глибині назад до Мексиканської затоки, щоб повторити цикл. Висока прихована теплота плавлення води стабілізує температуру водойм при температурі замерзання води (0 °С).
Крім перерахованих вище, існують і інші унікальні і екологічно важливі якості води. Це чудовий розчинник, особливо для іонних речовин, що робить його важливим для транспортування поживних речовин та відходів у біосфері та при розчиненні, транспортуванні та відкладенні мінералів у геосфері. Вода має дуже високий поверхневий натяг, контролюючий фактор фізіології і властивість, що бере участь в утворенні крапель опадів. Співвідношення температура/щільність води призводить до того, що водойми стають стратифікованими (див. Рис. 9.4) - властивість, яка сильно впливає на хімічну поведінку води в стратифікованих водоймах. Той факт, що максимальна щільність води виникає у вигляді рідини при 4 °С, означає, що твердий лід плаває. Якби це не так, водойми в північному кліматі стали б замороженими твердими, лише поверхневий шар відтавав протягом літа. Вода значною мірою прозора для видимого світла, який може проникати в рідину на деяку глибину і дозволяє фотосинтетичному фітопланктону та деяким рослинам з нижнім корінням у мілководних районах здійснювати фотосинтез та виробляти біомасу, яка є основою водних харчових ланцюгів (див. Розділ 8.5).
