13.2: Хімія атмосфери
- Page ID
- 20598
- Опишіть азотний цикл.
- Опишіть кисневий цикл.
- Опишіть умови для температурної інверсії.
Суміш газів в атмосфері утворює складну систему, організовану в шари, які разом підтримують життя на Землі. Хоча існують численні гази, як показано в таблиці 13.1.1, чотири верхні гази складають 99,998% від обсягу чистого сухого повітря (незабрудненого повітря, що не містить водяної пари). З цього сухого складу атмосфери азот, на сьогоднішній день, є найбільш поширеним (78%). Азот розріджує кисень і запобігає швидкому або миттєвому горінню на поверхні Землі, оскільки газ кисню є необхідним реагентом процесу горіння. Азот також необхідний і використовується живими істотами для виробництва білків, хоча як азотний газ, N 2, він недоступний для більшості живих істот. Кисень використовується всім живим, щоб зробити молекули, необхідні для життя. Це також важливо для аеробного дихання, а також горіння або горіння.
Цикл азоту
Все життя вимагає азотних сполук, наприклад, білків і нуклеїнових кислот. Повітря, який становить 79% азоту (N 2), є основним резервуаром азоту. Але більшість організмів не можуть використовувати азот в такому вигляді. Малюнок\(\PageIndex{1}\) ілюструє весь цикл азоту. Рослини повинні забезпечувати свій азот у «фіксованій» формі, тобто включений у такі сполуки, як: нітратні іони (NO 3 −), іони амонію (NH 4 +) та сечовина (NH 2) 2 СО. Тварини закріплюють свої азотні (і всі інші) сполуки від рослин (або тварин, які харчувалися рослинами).
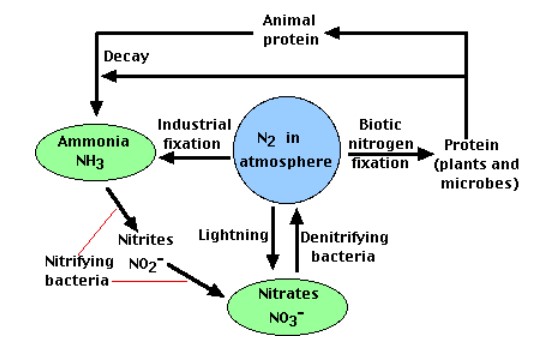
У циклічному циклі азоту через біосферу беруть участь чотири процеси: (1) фіксація азоту, (2) розпад, (3) нітрифікація та (4) денітрифікація. Мікроорганізми відіграють головну роль у всіх чотирьох з них.
Фіксація азоту
Молекула азоту (N 2) досить інертна. Щоб розбити його, щоб його атоми могли поєднуватися з іншими атомами, потрібно введення значної кількості енергії. За більшу частину фіксації азоту в біосфері відповідають три процеси:
- фіксація атмосфери блискавкою
- біологічна фіксація певними мікробами самостійно або в симбіотичному взаємозв'язку з деякими рослинами і тваринами
- промислова фіксація
Атмосферна фіксація
Величезна енергія блискавки розбиває молекули азоту і дозволяє їх атомам поєднуватися з киснем у повітрі, утворюючи оксиди азоту. Вони розчиняються в дощі, утворюючи нітрати, які переносяться на землю. Фіксація атмосферного азоту, ймовірно, сприяє деяким 5-8% від загального зафіксованого азоту.
Промислова фіксація
Під великим тиском, при температурі 600° C і з використанням каталізатора, атмосферний азот і водень (зазвичай отримують з природного газу або нафти) можуть бути об'єднані з утворенням аміаку (NH 3). Аміак можна використовувати безпосередньо як добриво, але більша його частина додатково переробляється до сечовини і аміачної селітри (NH 4 NO 3).
Біологічна фіксація
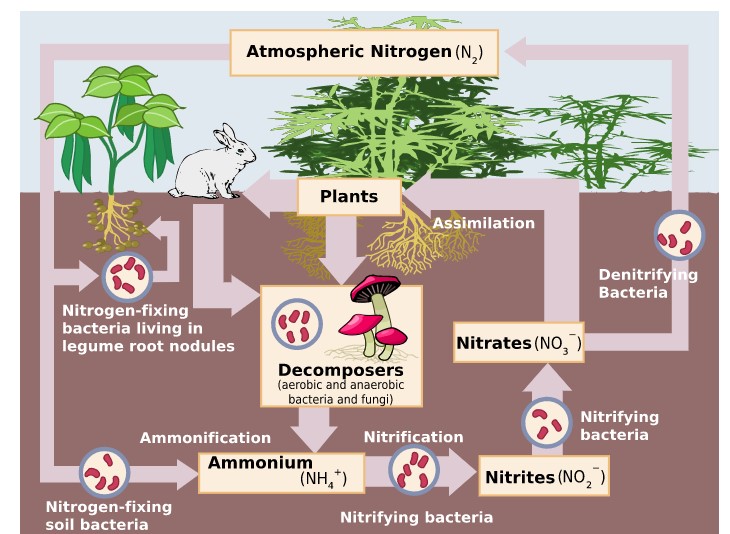
Здатність фіксувати азот в грунті (рис.\(\PageIndex{2}\)) тільки у певних бактерій і архей.
- Деякі живуть в симбіотичних стосунках з рослинами сімейства бобових (наприклад, соя, люцерна).
- Деякі встановлюють симбіотичні відносини з рослинами, відмінними від бобових (наприклад, вільхи).
- Деякі встановлюють симбіотичні відносини з тваринами, наприклад, термітами та «корабельними черв'яками» (двостулкові дрова).
- Деякі азотфіксуючі бактерії живуть вільно в грунті.
- Ціанобактерії, що фіксують азот, мають важливе значення для підтримки родючості напівводних середовищ, таких як рисові поля.
Біологічна азотфіксація вимагає складного набору ферментів і величезних витрат АТФ. Хоча першим стабільним продуктом процесу є аміак, він швидко включається в білок та інші органічні сполуки азоту.
Розпад
Білки, вироблені рослинами, входять і проходять через харчові мережі так само, як і вуглеводи. На кожному трофічному рівні їх метаболізм виробляє органічні сполуки азоту, які повертаються в навколишнє середовище, головним чином у виділеннях. Кінцевими бенефіціарами цих матеріалів є мікроорганізми гниття. Вони розщеплюють молекули в виділеннях і мертвих організмах на аміак.
нітрифікація
Аміак може бути прийнятий безпосередньо рослинами - як правило, через їх коріння. Однак велика частина аміаку, що утворюється при розпаді, перетворюється в нітрати. До недавнього часу вважалося, що це завжди досягається в два етапи:
- Бактерії роду Nitrosomonas окислюються\(\ce{NH3}\) до нітритів (\(\ce{NO2^{−}}\)).
- Бактерії роду Nitrobacter окислюють нітрити до нітратів (\(\ce{NO3^{−}}\)).
Ці дві групи автотрофних бактерій називаються нітрифікуючими бактеріями. Завдяки своїй діяльності (яка постачає їх усіма енергетичними потребами) азот стає доступним до коріння рослин. Однак у 2015 році дві групи повідомили про виявлення того, що бактерії роду Nitrospira змогли виконувати обидва етапи: аміак до нітриту і нітрит до нітрату. Ця здатність називається «comammox» (для повного окислення аміаку).
Крім того, як ґрунт, так і океан містять археальні мікроби, призначені для Кренархеота, які перетворюють аміак в нітрити. Вони більш рясні, ніж нітрифікуючі бактерії і можуть виявитися відігравати важливу роль у циклі азоту.
Багато бобових, крім фіксації атмосферного азоту, також виконують нітрифікацію - перетворюючи частину свого органічного азоту в нітрити та нітрати. Вони досягають ґрунту, коли скидають листя.
Денітрифікація
Три вищевказані процеси видаляють азот з атмосфери і пропускають його через екосистеми. Денітрифікація знижує нітрати і нітрити до газу азоту, тим самим заповнюючи атмосферу. В процесі утворюється кілька проміжних продуктів:
- оксид азоту (NO)
- закис азоту (N 2 O) (парниковий газ в 300 разів потужніший, як СО 2)
- азотна кислота (HONO)
Знову ж таки, бактерії є агентами. Вони живуть глибоко в грунті та у водних відкладах, де умови анаеробні. Вони використовують нітрати як альтернативу кисню для кінцевого акцептора електронів у диханні.
Анаммокс (аеробні боєприпаси)
В анаеробних умовах в морських і прісноводних відкладах інші види бактерій здатні окислювати аміак (з\(\ce{NO2^{−}}\)) утворюючи газ азоту.
\[\ce{NH4^{+} + NO2^{−} → N2 + 2H2O} \nonumber \]
Анаммоксна реакція може становити цілих 50% денітрифікації, що відбувається в океанах. Всі ці процеси беруть участь в закритті азотного циклу.
Чи підтримують денітрифікатори?
Сільське господарство тепер може нести відповідальність за половину фіксації азоту на землі за рахунок використання добрив, вироблених промисловою фіксацією, та вирощування бобових культур, таких як соя та люцерна. Це неабиякий вплив на природний цикл. Чи підтримують денітрифікатори цикл азоту в рівновазі? Напевно, ні. Безумовно, є приклади збагачення азотом в екосистемах. Один тривожний приклад: «цвітіння» водоростей в озерах і річках як азотні добрива вимивають з грунту сусідніх господарств (і газонів). Накопичення розчинених поживних речовин у водоймі називається евтрофікацією.
Кисневий цикл
Кисень - найпоширеніший елемент на земній корі. Земна поверхня складається з кори, атмосфери та гідросфери. Близько 50% маси земної кори складається з кисню (поєднаного з іншими елементами, головним чином кремнієм). Кисень виникає у вигляді молекул O 2 і, в обмеженій мірі, як молекули O 3 (озону) в повітрі. Вона утворює близько 20% маси повітря. Близько 89% води по масі складається з комбінованого кисню. У поєднанні з вуглецем, воднем і азотом кисень становить велику частину рослин і тварин.
Кисень - це безбарвний газ без запаху та смаку при звичайних температурах. Він трохи щільніше повітря. Хоча він лише слабо розчинний у воді (49 мл газу розчиняється в 1 л при STP), розчинність кисню дуже важлива для водної життєдіяльності.
Кисень необхідний в таких процесах горіння, як спалювання палива. Рослини і тварини використовують кисень з повітря при диханні (рис.\(\PageIndex{4}\)). Основний спосіб вільного кисню втрачається з атмосфери через і, механізми, при яких життя і споживають кисень і виділяють вуглекислий газ.
Процес дихання представлений у вигляді:
\[\ce{6O2+C6H12O6→6CO2+6H2O} \nonumber \]
Зелені рослини постійно поповнюють кисень в атмосфері процесом, званим фотосинтезом (рис.\(\PageIndex{3}\)). Продукти фотосинтезу можуть відрізнятися, але, в цілому, процес перетворює вуглекислий газ і воду в глюкозу (цукор) і кисень, використовуючи енергію світла:
&\ ce {6CO2} (г)\ :+\: &&\ ce {6H2O} (л)
\:\ mathrm {\ underset {світло} {\ xrightarrow {хлорофіл}}\:
&&\ ce {C6H12O6} (q)\ :+\: &\ ce {6O2} г)\\
&\ mathrm {вуглець\\ діоксид} &\ ce {вода} &&\ ce { глюкоза} &&\ ce {кисень}
\ кінець {alignat}\ number\]
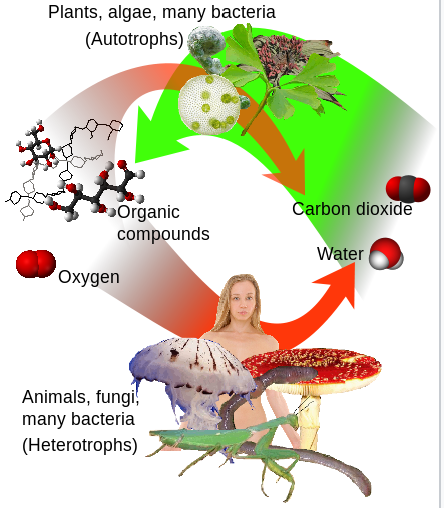
Огляд і фотосинтезу (зелений) і дихання (червоний).
Вода (праворуч) разом з вуглекислим газом (СО 2) утворюють кисень і органічні сполуки (зліва),
які можна віддихати до води і (СО 2). Джерело: Вікіпедія
Таким чином, кисень, який став вуглекислим газом і водою в результаті обмінних процесів у рослин і тварин, повертається в атмосферу шляхом фотосинтезу. Фотосинтезуючі організми включають рослинне життя сухопутних районів, а також океанів. Крихітний морський піхотинець був відкритий в 1986 році і становить більше половини фотосинтезу відкритого океану.
Кисень є ключовим реагентом у різних реакціях окислення, згаданих у розділі 8.5. Атмосферний вільний кисень також споживається хімічним вивітрюванням і поверхневими реакціями. Прикладом поверхневого вивітрювання є утворення іржі:
Озон утворюється природним чином у верхній атмосфері під дією ультрафіолетового світла сонця на кисень там. Більшість атмосферного озону відбувається в стратосфері, шарі атмосфери, що простягається приблизно від 10 до 50 кілометрів над земною поверхнею. Цей озон діє як бар'єр для шкідливого ультрафіолетового світла від сонця, поглинаючи його за допомогою хімічної реакції розкладання:
\[\ce{O3}(g)\xrightarrow{\ce{ultraviolet\: light}}\ce{O}(g)+\ce{O2}(g) \nonumber \]
Температурні інверсії
У метеорології інверсія, також відома як інверсія температури, - це відхилення від нормальної зміни атмосферного властивості з висотою. Практично завжди мається на увазі інверсія швидкості теплового проміжку. У нормі температура повітря знижується зі збільшенням висоти. Під час інверсії тепліше повітря утримується над більш холодним повітрям; нормальний температурний профіль з висотою перевернутий.
Інверсія затримує забруднення повітря, наприклад, смог, близько до землі. Інверсія також може пригнічувати конвекцію, виступаючи в ролі «ковпачка». Якщо ця кришка зламана з будь-якої з кількох причин, конвекція будь-якої присутньої вологи може потім вибухнути в сильні грози Інверсія температури може, як відомо, призвести до замерзання дощу в холодному кліматі.
Резюме
- Різні форми азоту, які можуть бути використані в обміні речовин, виробляються в процесі фіксації азоту.
- Бактерії в ґрунті здійснюють процес, відомий як денітрифікація, яка перетворює нітрати назад в газ азоту.
- Кисень виробляється в основному за допомогою фотосинтезу. Додаткове джерело атмосферного вільного кисню надходить з, завдяки якому високоенергетичне випромінювання розщеплює атмосферну воду і закис азоту.
- Кисень утилізується під час клітинного дихання і розпаду. А також під час хімічного вивітрювання і різних реакцій окислення.
- Температурна інверсія - це коли шар прохолодного повітря потрапляє під шар більш теплого повітря. Прохолодне щільне повітря може затримувати і накопичувати забруднювачі повітря.
Автори та атрибуція
- Template:ContribKimball
- Template:ContribOpenStax
- Template:ContribAgnewM
- TextMap: Microbiology (Boundless)
- Wikipedia
