13.1: Амінокислоти
Результати навчання
- Визначте структурні компоненти амінокислоти.
- Визначте цвіттеріон і ізоелектричну точку.
- Визначте заряд на амінокислоті, коли її немає в ізоелектричної точці.
- Позначте амінокислоти як полярні та неполярні та як кислі, основні або нейтральні.
Легка атлетика дуже конкурентоспроможні в ці дні на всіх рівнях, від шкільних видів спорту до профі. Кожен шукає той край, який зробить їх швидшими, сильнішими, більш фізично придатними. Один підхід, прийнятий багатьма спортсменами є використання амінокислотних добавок. Теорія полягає в тому, що збільшення амінокислот в раціоні призведе до збільшення білка для м'язів. Однак єдина реальна вигода приходить до людей, які роблять і продають таблетки. Дослідження не показали жодної переваги, отриманої самими спортсменами. Вам набагато краще просто підтримувати здорову дієту.
Амінокислоти
Амінокислота - це з'єднання, яке містить як амінну групу, так\left( \ce{-NH_2} \right) і карбоксильну групу\left( \ce{-COOH} \right) в одній молекулі. Хоча будь-яку кількість амінокислот можна уявити, біохіміки, як правило, резервують термін для групи з 20 амінокислот, які утворюються і використовуються живими організмами. На малюнку нижче показано загальну будову амінокислоти. Будь-яка структура вважається правильною для амінокислоти.

Амін і карбоксильні групи амінокислоти обидва ковалентно пов'язані з центральним атомом вуглецю. Цей атом вуглецю також пов'язаний з атомом водню та\ce{R} групою. Саме ця\ce{R} група варіюється від однієї амінокислоти до іншої і називається амінокислотним бічним ланцюгом.

Характер бічних ланцюгів пояснює мінливість фізичних і хімічних властивостей різних амінокислот. Кожна амінокислота групується виходячи з властивостей бічного ланцюга. Групи позначаються як полярні (гідроксильні, сірковмісні, амідні), неполярні (аліфатичні і ароматичні), кислі, або основні.
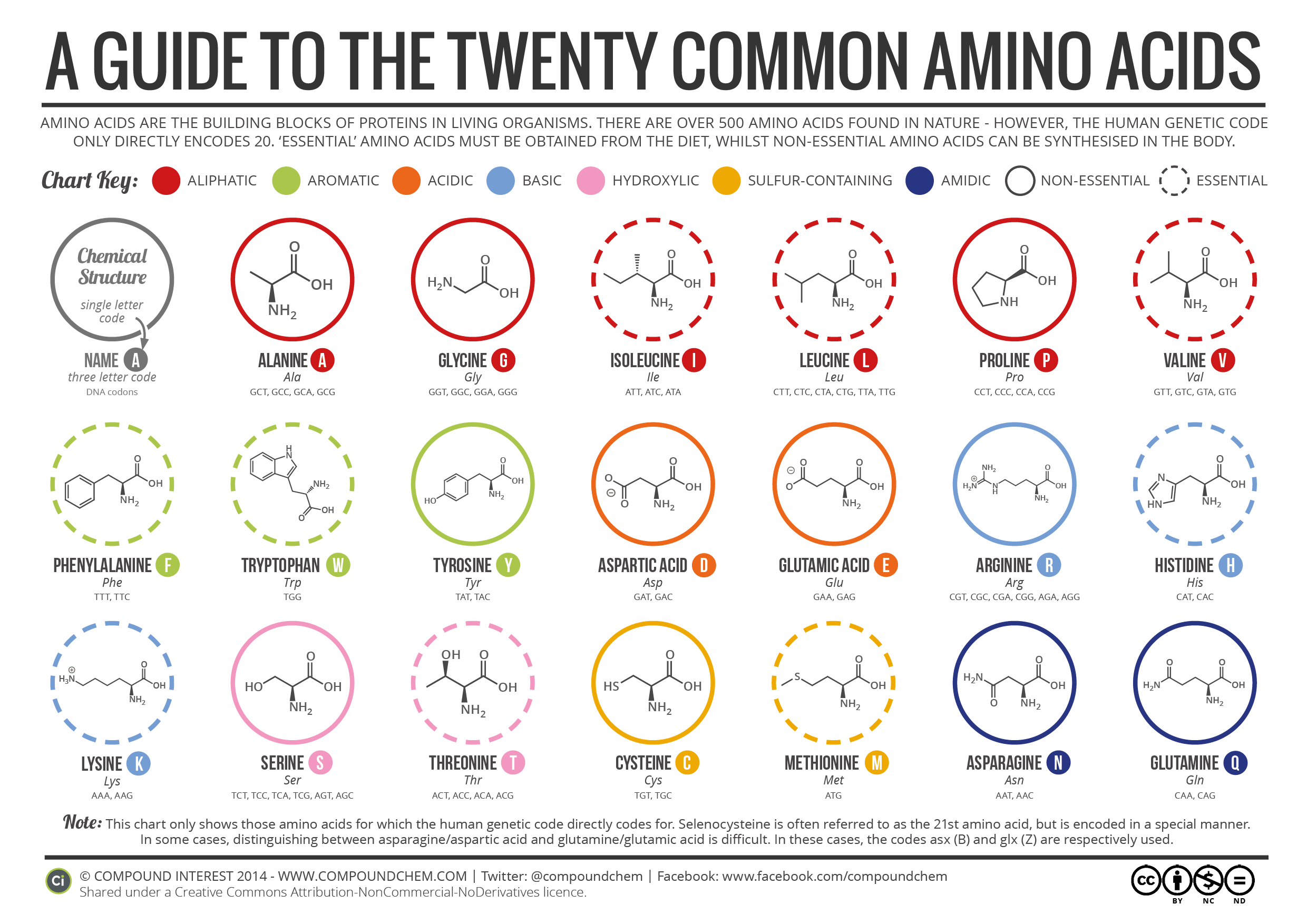
Крім повної назви амінокислоти, існують також однобуквені і трибуквені абревіатури для кожної. Ці скорочення особливо корисні при перерахуванні амінокислот в білку (ланцюжок багатьох амінокислот, про яку піде мова далі).
Правила класифікації амінокислот
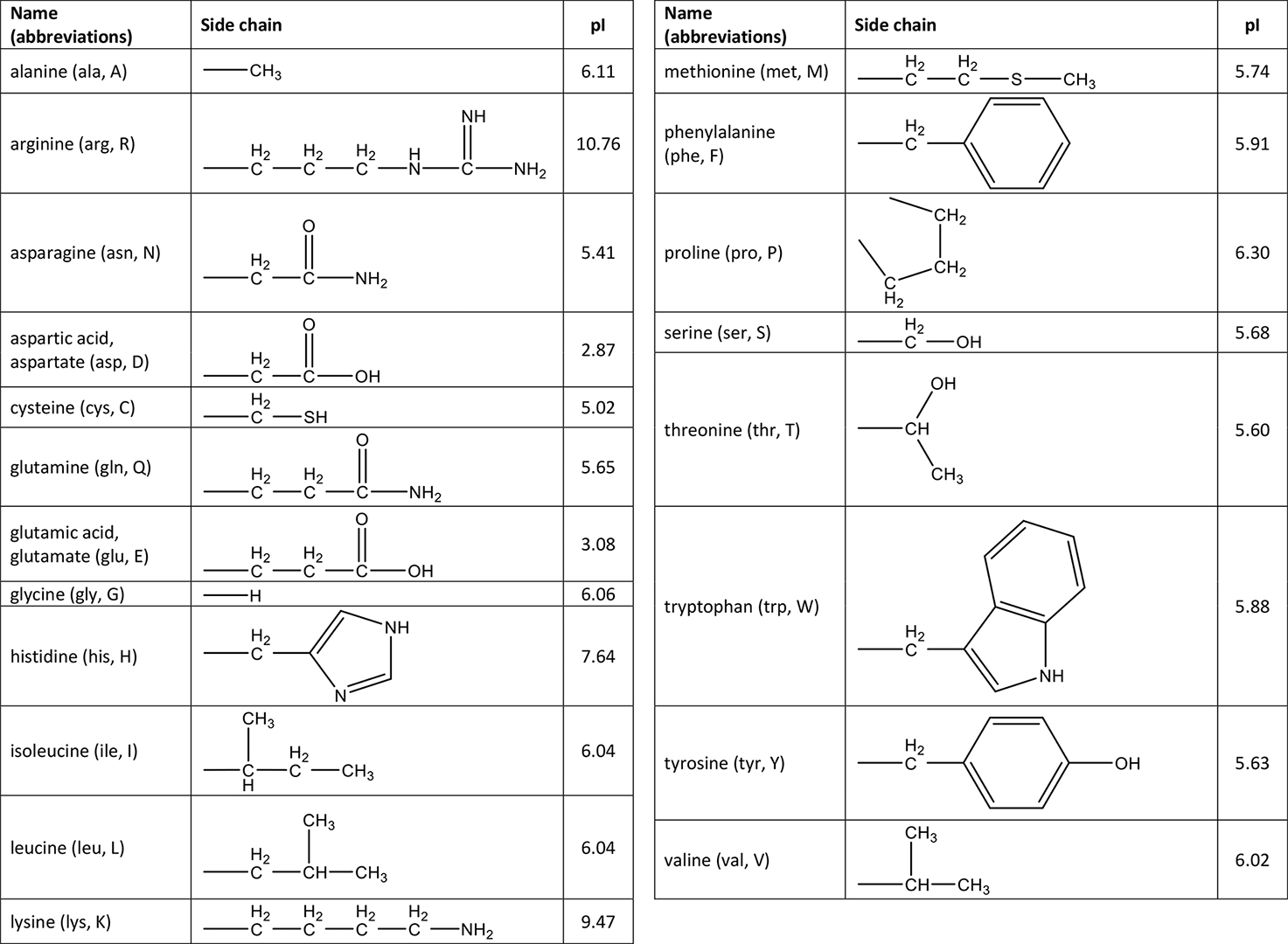
Наступні правила (поряд з двома винятками) можуть допомогти вам класифікувати амінокислоти як неполярні, полярні кислі (іноді їх називають кислотними), полярними основними (іноді називають основними) або полярними нейтральними. Ми розглянемо два винятки, але зауважте, що перехід від неполярної до полярної нейтральної є поступовим переходом (як кольори веселки), тому ви можете побачити варіації в тому, як класифікуються амінокислоти, якщо ви подивитеся на інші джерела.
- Неполярні амінокислоти (їх 9) містять аліфатичні (вуглеводневі) ланцюги або ароматичні кільця.
- Полярні кислотні амінокислоти (2) містять групу карбонових кислот (або карбоксилатів) в бічному ланцюзі (група R). Це на додаток до тієї, що знаходиться в кістці амінокислоти.
- Полярні основні амінокислоти (3) містять амінну (може бути нейтральною або зарядженою) групу в бічному ланцюзі (група R). Це на додаток до тієї, що знаходиться в кістці амінокислоти.
- Полярні нейтральні амінокислоти (6) містять гідроксил (-ОН), сірку або амід в групі R).
З перерахованих вище правил є два важливих винятки.
- Тирозин має ароматичну групу і групу -OH і вважається полярно-нейтральним.
- Метіонін містить сірку, але як частина вуглецевого ланцюга. Сірка має таку ж електронегативність, як і вуглець, тому вважається неполярною.
Цвіттеріон
Амінокислоти зазвичай витягуються або без зарядів, або з плюсовим і мінусовим зарядом (див. Малюнок 13.1.1). Коли амінокислота містить і плюс, і мінус заряд в «хребті», вона називається цвиттеріон і має загальний нейтральний заряд. Цвіттеріон амінокислоти існує при рН, рівному ізоелектричної точці. Кожна амінокислота має своє значення pI, засноване на властивостях амінокислоти. При значеннях рН вище або нижче ізоелектричної точки молекула матиме чистий заряд, який залежить від її значення pI, а також рН розчину, в якому знаходиться амінокислота.
рН <pI
Коли рН менше pH, спостерігається надлишкова кількість\ce{H^+} в розчині. Надлишок\ce{H^+} притягується до негативно зарядженого карбоксилатного іона, що призводить до його протонації. Іон вуглеводів протонується, роблячи його нейтральним, залишаючи тільки позитивний заряд на амінну групу. В цілому, амінокислота буде мати заряд+1.

рН > pH
Коли рН більше pH, спостерігається надлишкова кількість\ce{OH^-} в розчині. Надлишок\ce{OH^-} притягується до позитивно зарядженої амінної групи, що призводить до видалення\ce{H^+} іона з утворенням (\ ce {H_2O}\). Амінна група має нейтральний заряд, що залишає на карбоксилатній групі тільки негативний заряд. В цілому, амінокислота буде мати заряд-1.

Приклад\PageIndex{1}
- Визначте амінокислоту, зображену нижче.
- Знайдіть значення pI для амінокислоти.
- Визначте, як буде існувати амінокислота при рН = 3,52
- Визначте, як буде існувати амінокислота при рН = 9,34
- Визначте, як буде існувати амінокислота при рН = 5,02

Рішення:
а. подивіться на бічний ланцюг, щоб визначити амінокислоту. Бічний ланцюг містить\ce{-CH_2SH}, який відповідає структурі цистеїну.
б Значення pI для амінокислот знаходяться в таблиці амінокислот. Для цистеїну pI = 5,02.
с. при рН = 3,52\ce{H^+} концентрація висока (низький рН = більш кислий = більше\ce{H^+}). Тому\ce{H^+} додадуть до карбоксилату іон і нейтралізують негативний заряд. Амінокислота матиме позитивний заряд на лівій групі аміну і матиме загальний заряд+1.

d При рН = 9,34\ce{OH^-} концентрація висока (високий рН = більш основний = менше\ce{H^+} = більше\ce{OH^-}). Тому\ce{OH^-} будуть притягуватися до позитивно зарядженої групи амінів і будуть «вкрасти»\ce{H^+} з неї. В результаті єдиний залишився заряд буде на карбоксилатний іон, тому амінокислота матиме-1 заряд.

e При рН = 5,02 рН = pI, тому амінокислота буде існувати як цвіттеріон як з позитивними, так і з негативними зарядами, як показано вище.