10.4: Фізико-хімічні зміни
- Page ID
- 22897
Результати навчання
- Розрізняють фізичні та хімічні зміни.
- Наведіть приклади фізичних і хімічних змін.
Фізичні зміни
Коли кубик льоду тане, його форма змінюється в міру набуття здатності протікати. Однак його склад не змінюється. Плавлення - приклад фізичної зміни. Фізична зміна - це зміна зразка матерії, в якій змінюються деякі властивості матеріалу, але ідентичність матерії - ні. Фізичні зміни можна додатково класифікувати як оборотні або незворотні. Розплавлений кубик льоду може бути повторно заморожений, тому танення є оборотною фізичною зміною. Фізичні зміни, які передбачають зміну стану, є оборотними. Інші зміни стану включають випаровування (від рідини до газу), заморожування (від рідини до твердої речовини) та конденсацію (від газу до рідини). Розчинення також є оборотною фізичною зміною. Коли сіль розчиняється у воді, сіль, як кажуть, увійшла у водний стан. Сіль можна відновити, кип'ятивши воду, залишивши сіль позаду.

Коли шматок дерева подрібнюється в тирсу, ця зміна є незворотною, оскільки тирса не може бути відновлена в той самий шматок дерева, який був раніше. Стрижка трави або подрібнення породи були б іншими незворотними фізичними змінами. Дрова також являють собою незворотну фізичну зміну, оскільки шматки не можна скласти назад, щоб сформувати дерево.

Хімічні зміни
При впливі повітря предмет з заліза з часом почне іржавіти (див. Малюнок нижче).

Оскільки іржа утворюється на поверхні заліза, вона відшаровується, щоб оголити більше заліза, яке буде продовжувати іржавіти. Іржа - це явно речовина, яка відрізняється від заліза. Іржавіння - приклад хімічної зміни.
Хімічна властивість описує здатність речовини зазнавати специфічні хімічні зміни. Хімічна властивість заліза полягає в тому, що воно здатне поєднуватися з киснем утворювати оксид заліза, хімічна назва іржі. Більш загальним терміном для іржавіння та інших подібних процесів є корозія. Інші терміни, які зазвичай використовуються в описі хімічних змін, - це опік, гниття, вибух та бродіння. Хімічні властивості дуже корисні як спосіб ідентифікації речовин. Однак, на відміну від фізичних властивостей, хімічні властивості можна спостерігати лише в міру зміни речовини на іншу речовину.
Хімічна зміна також називається хімічною реакцією. Хімічна реакція - це процес, який відбувається при зміні одного або декількох речовин на одне або кілька нових речовин. Цинк\(\left( \ce{Zn} \right)\) - сріблясто-сірий елемент, який можна подрібнити в порошок. Якщо цинк змішати при кімнатній температурі з порошкоподібною сіркою\(\left( \ce{S} \right)\), яскраво-жовтим елементом, результатом буде просто суміш цинку і сірки. Ніякої хімічної реакції не відбувається. Однак, якщо енергія надається суміші у вигляді тепла, цинк буде хімічно реагувати з сіркою, утворюючи з'єднання сульфіду цинку\(\left( \ce{ZnS} \right)\). На фото нижче представлені речовини, що беруть участь в цій реакції.
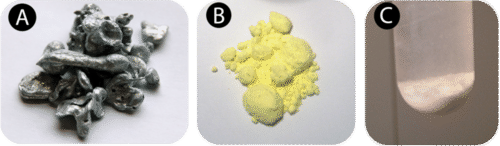
Реакцію між цинком і сіркою можна зобразити в чомусь, званому хімічним рівнянням. Словами, ми могли б написати реакцію так:
\[\text{zinc} + \text{sulfur} \rightarrow \text{zinc sulfide}\]
Більш зручним способом вираження хімічної реакції є використання умовних позначень і формул задіяних речовин:
\[\ce{Zn} + \ce{S} \rightarrow \ce{ZnS}\]
Речовина (и) зліва від стрілки в хімічному рівнянні називаються реагентами. Реагент - це речовина, яка присутня на початку хімічної реакції. Речовина (и) праворуч від стрілки називаються продуктами. Продукт - це речовина, яка присутня в кінці хімічної реакції. У наведеному вище рівнянні цинк і сірка - це реагенти, які хімічно з'єднуються, утворюючи сульфід цинку як продукт.
Розпізнавання хімічних реакцій
Як можна визначити, чи відбувається хімічна реакція? Певні візуальні підказки вказують на те, що хімічна реакція ймовірно (але не обов'язково) відбувається, включаючи наступні приклади:
- Зміна кольору відбувається під час реакції.
- Під час реакції утворюється газ.
- В реакції утворюється твердий продукт, званий осадом.
- Видима передача енергії відбувається у вигляді світла в результаті реакції.
Коли цинк реагує з соляною кислотою, реакція бурхливо бульбашки, коли утворюється водневий газ (див. Малюнок нижче). Виробництво газу також є свідченням того, що може відбуватися хімічна реакція.

При додаванні безбарвного розчину нітрату свинцю (II) в безбарвний розчин йодистого калію миттєво утворюється жовте тверде речовина, зване осадом (див. Малюнок нижче). Осад - це твердий продукт, який утворюється в результаті реакції і осідає з рідкої суміші. Освіта осаду також може свідчити про виникнення хімічної реакції.
\[\ce{Pb(NO_3)_2} \left( aq \right) + 2 \ce{KI} \left( aq \right) \rightarrow \ce{PbI_2} \left( s \right) + 2 \ce{KNO_3} \left( aq \right)\]
