2.2: Матерія
Результати навчання
- Визначте матерію.
- Класифікувати чисті речовини як елементи або сполуки.
- Класифікують суміші як однорідні або гетерогенні.
- Знайте назви та символи елементів, зазначених у «Речах для запам'ятовування» на полотні.
- Розрізняють серед металів, неметали, металоїди.
Живі істоти зроблені з матерії. По суті, матерія - це «матеріал», з якого зроблені всі речі (див. Малюнок нижче. Все, що займає простір і має масу, відомо як матерія. Матерія, в свою чергу, складається з хімічних речовин. Хімія - це вивчення речовини та змін, які вона зазнає.
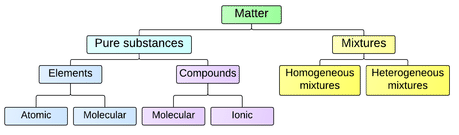
Чисті речовини
Чиста речовина - це матеріал, який має певний хімічний склад. Він також однорідний, тому однаковий хімічний склад знаходиться рівномірно по всьому речовині. Чистим речовиною може бути елемент або хімічна сполука.
Елементи
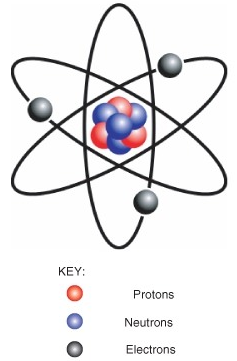
Елемент - це чиста речовина, яка не може бути розщеплена на різні типи речовин. Приклади елементів включають вуглець, кисень, водень та залізо. Кожен елемент складається тільки з одного типу атома. Атом - це найдрібніша частинка елемента, яка все ще характеризує елемент. Як показано на малюнку нижче, в центрі атома знаходиться ядро. Ядро містить позитивно заряджені частинки, звані протонами, і електрично нейтральні частинки, звані нейтронами. Навколишнє ядро - набагато більша електронна хмара, що складається з негативно заряджених електронів. Атом електрично нейтральний, якщо він має таку ж кількість протонів, що і електронів. Кожен елемент має атоми з характерною кількістю протонів. Наприклад, всі атоми вуглецю мають шість протонів, а всі атоми кисню мають вісім протонів.
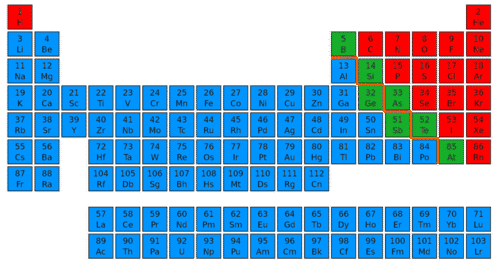
Існує майже 120 відомих елементів (див. Малюнок нижче) і кожен представлений в таблиці Менделєєва символом однієї або двох букв. Більшість відомих елементів класифікуються як метали. Метали - це елементи, які є блискучими, або блискучими. Вони також є хорошими провідниками електрики і тепла. Приклади металів включають залізо, золото та мідь. Менше 20 елементів класифікуються як неметали. Неметали позбавлені властивостей металів. Приклади неметалів включають кисень, водень та сірку. Деякі інші елементи мають властивості як металів, так і неметалів. Вони відомі як металоїди. Приклади металоїдів включають кремній і бор.
Нову пісню періодичної таблиці можна почути за адресою https://youtu.be/zUDDiWtFtEM
Том Лерер виконав оригінальну пісню стихії в 1967 році. Ви можете почути це за адресою https://youtu.be/DYW50F42ss8.
Хімічні сполуки
Хімічна сполука - це чиста речовина, яка утворюється, коли атоми двох і більше елементів реагують один з одним. З'єднання завжди має унікальний і фіксований хімічний склад, а атоми сполуки утримуються хімічними зв'язками. Існують різні типи хімічних зв'язків, і вони різняться тим, наскільки сильно вони утримують атоми сполуки. Два типи зв'язків - ковалентні і іонні зв'язки. Ковалентні зв'язки утворюються, коли атоми поділяють електрони і виникають між двома або більше неметалами. Іонні зв'язки утворюються, коли електрони передаються від одного атома до іншого і зазвичай утворюються між металом і неметалом.
Прикладом хімічної сполуки є вода. Молекула води утворюється, коли(H) атоми кисню(O) та водню реагують і утримуються разом ковалентними зв'язками. Як і інші сполуки, вода завжди має однаковий хімічний склад: співвідношення атомів водню до атомів кисню 2:1. Це виражається в хімічній формулі для води,H2O. Співвідношення елементів в з'єднанні задається хімічною формулою. Наприклад,NaCl має співвідношення 1:1 між атомами натрію та хлору. Відсутність індексованого числа у формулі вказує на те, що є один з цих елементів.
Суміші
Як і хімічна сполука, суміш складається не з одного хімічної речовини. На відміну від з'єднання, суміш не має фіксованого хімічного складу. Речовини в суміші можна поєднувати в будь-яких пропорціях. Однією з характеристик сумішей є те, що їх можна розділити на складові фізичними методами. Оскільки кожна частина суміші не вступила в реакцію з іншою частиною суміші, тотожності різних речовин залишаються незмінними.
Наступні приклади ілюструють ці відмінності між сумішами та сполуками. Обидва приклади включають однакові два елементи: металеве залізо(Fe) та неметалеву сірку(S).
- Коли залізні пломби і порошок сірки змішуються між собою в будь-якому співвідношенні, вони утворюють суміш (див. Малюнок нижче). Ніякої хімічної реакції не відбувається, і обидва елементи зберігають свої індивідуальні властивості. Магніт може бути використаний для фізичного відокремлення двох елементів, притягуючи залізні наповнювачі з суміші і залишаючи сірку позаду.
- При змішуванні заліза і сірки в певному співвідношенні і нагріванні відбувається хімічна реакція. Це призводить до утворення унікального нового з'єднання, званого сульфідом заліза (II)(FeS) (див. Малюнок нижче). Магніт не може бути використаний для механічного відділення заліза від сульфіду заліза (II), оскільки в сполуці не існує ні заліза, ні сірки. Замість цього потрібна інша хімічна реакція для відділення заліза і сірки.


однорідні суміші
Однорідна суміш являє собою суміш, в якій склад рівномірний по всій суміші. Суміш солі і води однорідна, оскільки розчинена сіль рівномірно розподіляється по всій пробі солоної води. Часто легко сплутати однорідну суміш з чистою речовиною, оскільки вони обидва однорідні. Різниця полягає в тому, що склад речовини завжди однаковий, при цьому склад суміші може змінюватися. Кількість солі в солоній воді може варіюватися від одного зразка до іншого, тоді як вода, наприклад, завжди має однаковий склад.
гетерогенні суміші
Гетерогенна суміш - це суміш, в якій склад неоднорідний по всій суміші. Одним із прикладів неоднорідної суміші є овочевий суп. Будь-яка дана ложка супу буде містити різну кількість різних овочів та інших компонентів супу. Іншим прикладом неоднорідної суміші є грунт, який складається з різних речовин і часто має різний склад залежно від взятого зразка. Одна лопата може придумати бруд і траву, тоді як наступна лопата може містити дощового хробака.
Дивіться більше прикладів гетерогенних сумішей на www.buzzle.com/articles/homog... -examples.html
Додаткові ресурси
Дізнатися більше
- Девід Боданіс, E = mc2: Біографія найвідомішого питання у світі. Уокер і Ко, 2005
- Джон Емслі, Будівельні блоки природи: A-Z Керівництво по стихіям. Преса Оксфордського університету, 2003.
- Невін Кац, Елементи, сполуки та суміші: середня та середня школа (містер Бірдлі викладає науку). Стимулюючі публікації, 2007.
- Наука про салат з макаронів: що в суміші? http://youtu.be/Vt7IN4QPU0k
- Гетерогенні суміші антуан.frostburg.edu/chem/se... однорідний.shtml
- Елемент флеш-карти http://education.jlab.org/elementflashcards/