8.3: Період напіввиведення радіоізотопів
- Page ID
- 25609
Період напіврозпаду (t 1/2) радіоізотопу - це час, необхідний для половини зразка розпаду.
Це говорить про швидкість розпаду радіоізотопу — чим швидше швидкість розпаду, тим коротший період напіврозпаду.
Загальні особливості періоду напіввиведення
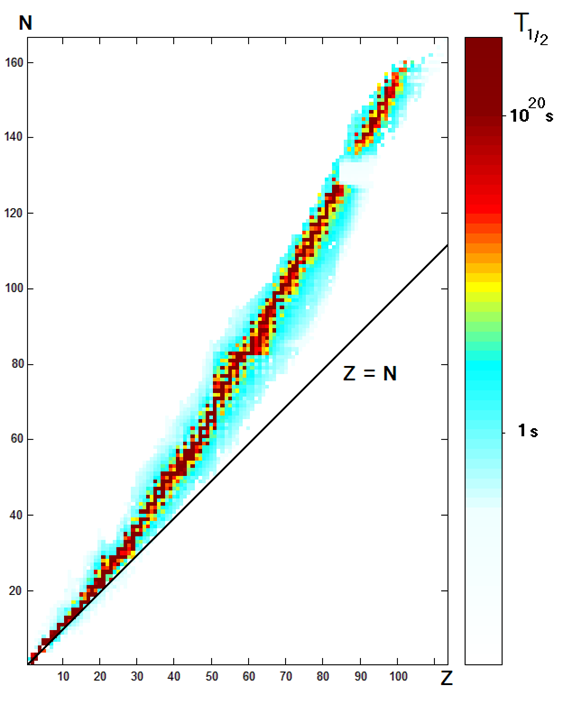
- Період напіввиведення різний для різних нуклеоїдів, як показано на рис. 8.3.1, і в таблиці 1. Вона варіюється від частки секунди до більш ніж 10 20 с, тобто більше 3 трильйонів років.
- Чим далі нуклеоїд знаходиться далеко від стійкого нуклеоїда (показано чорними точками на рис. 8.3.1), тим він менш стійкий, і тим швидше розпадається.
- Період напіврозпаду не залежить від концентрації, температури та тиску, тобто t 1/2 є характерною константою радіоізотопу.
- Природні радіоактивні ізотопи зазвичай мають більш тривалий період напіврозпаду, наприклад, t 1/2 вуглецю-14 становить 5730 років, а уран-235 - 7,0 х 10 8 років.
- Радіоізотопи, що використовуються для візуалізації та лікування в медичних науках, зазвичай синтезуються і мають короткий період напіврозпаду, так що вони не можуть зберігатися в організмі протягом надмірно тривалого часу. Наприклад, фосфор-32, йод-131 і технецій-99м мають період напіврозпаду 14,3 дня, 8,1 дня і 6,0 годин відповідно.
|
Радіоізотоп |
Символ |
Період напіврозпаду |
Використовувати |
|---|---|---|---|
|
Вуглець-14 |
\(\ce{_6^14C}\) |
5730 років |
Радіоізотопні знайомства |
|
Водень-3 |
\(\ce{_1^3H}\) |
12,3 років |
Радіоізотопні знайомства |
|
Калій-40 |
\(\ce{_19^40K}\) |
1,3 х 10 9 років |
Радіоізотопні знайомства |
|
Реній-187 |
\(\ce{_75^187Re}\) |
4,3 х 10 років |
Радіоізотопні знайомства |
|
Уран-238 |
\(\ce{_92^238U}\) |
4,5 х 10 9 років |
Радіоізотопні знайомства |
|
Уран-235 |
\(\ce{_92^235U}\) |
7,0 х 10 8 років |
Паливо для ядерних реакторів |
|
Кобальт-60 |
\(\ce{_27^60Co}\) |
5,3 років |
Медичний (зовнішнє джерело випромінювання) |
|
Йод-131 |
\(\ce{_53^131I}\) |
8,1 днів |
Медичний |
|
Залізо-59 |
\(\ce{_26^59Fe}\) |
45 днів |
Медичний |
|
Молібден-99 |
\(\ce{_42^99Mo}\) |
67 годин |
Медичний |
|
Натрій-24 |
\(\ce{_11^24Na}\) |
15 годин |
Медичний |
|
Техноній-99М |
\(\ce{_43^{99m}Te}\) |
6 годин |
Медичний |
|
Фосфор-32 |
\(\ce{_15^32P}\) |
14,3 днів |
Медичний |
Крива розпаду радіоізотопів
Протягом кожного наступного періоду напіврозпаду половина початкової кількості буде радіоактивно розпадатися, як показано на рис. 8.3.2. для випадку фосфору-32, який розпадається з періодом напіврозпаду 14,3 днів наступною ядерною реакцією
\[\ce{_15^32P -> _16^32S + _{-1}^{0}{e}}\nonumber\]
Припустимо, на початку є 100 мг фосфору-32; 50 мг залишиться після 14,3 дня, тобто після 1 періоду напіввиведення; і 25 мг залишиться через 28,6 дня, тобто через 2 періоди напіввиведення. Мізерно мала кількість батьківського ізотопу фосфору-32 залишається після 9 періодів напіврозпаду.
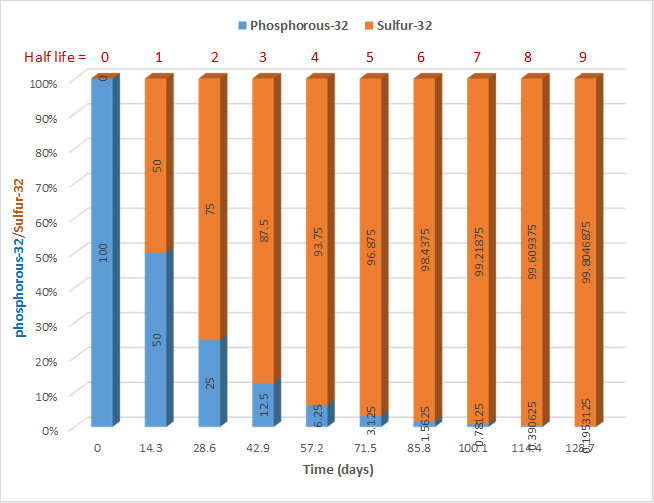
Кількість радіоізотопу, що залишився після заданого часу, можна розрахувати з відомої початкової кількості і витраченого часу, за такою формулою:
\[m_{f}=m_{i}(0.5)^{n}\nonumber\]
де m i - початкова сума, m f - кінцева сума, а n - кількість пройдених періодів напіврозпаду. Формула працює, навіть якщо кількість періодів напіврозпаду не є цілим числом.
Якщо для лікування вводили 50,0 мг йоду-131, скільки міліграмів залишиться через 40,5 дня? (Період напіввиведення йоду-131 становить 8.1 днів)
Рішення
Дано: m i = 50.0 мг, Час = 40,5 дня, Бажано? м ф
Рівність: 1 напівжива = 8,1 дня, дає наступні коефіцієнти перерахунку. \[\frac{1 \text { half-life }}{8.1 \text { days }} \quad\text{and}\quad \frac{8.1 \text { days }}{1 \text { half-life }}\nonumber\]
Для розрахунку періоду напіврозпаду помножте заданий час з коефіцієнтом перетворення, який скасовує час:
\[n=40.5 \cancel{\text { days }} \times \frac{1 \text { half-life }}{8.1 \cancel{\text { days }}}=5 \text { half-lives }\nonumber\]
Для розрахунку залишеної суми підключіть значення в формулу:
\[m_{f}=m_{i}(0.5)^{n}=50.0 \mathrm{mg}(0.5)^{5}=1.56 \mathrm{~mg}\nonumber\]
Радіоізотопні знайомства
Природна радіоактивність використовується для встановлення віку об'єктів археологічного, антропологічного або історичного інтересу. Всі живі об'єкти мають в своєму складі вуглець. Вуглець-14 - радіоактивний ізотоп вуглецю з періодом напіврозпаду 5730 років. Вуглець-14 отримують шляхом трансмутації азоту-14 при бомбардуванні нейтронами космічними променями, як показано на рис. 8.3.3. Його концентрація в джерелі вуглецю для живого організму залишається майже постійною, оскільки його розпад врівноважує його вироблення космічними променями. Живі організми безперервно поповнюють вуглець, тому концентрація вуглецю-14 залишається майже постійною до тих пір, поки об'єкт живий. Після того як об'єкт гине, вуглець-14 зменшується з часом, скорочуючись до половини після одного періоду напіввиведення. Ізотоп вуглець-12 не радіоактивний, тому його концентрація залишається постійною. Вимірювання співвідношення вуглець-14/вуглець-12 дозволяє розрахувати вік об'єкта після його загибелі. Вік ранніх цивілізацій, як і приклади цивілізації долини Інду, показані на рис. 8.3.4, визначалися методом датування вуглець-14.

Оскільки вуглець-14 зменшується з часом, об'єкт старше 20 000 років не має достатньої кількості вуглецю-14, щоб точно визначити їх вік. Інші радіоізотопи з більш тривалим періодом напіврозпаду, наприклад, уран-238 з періодом напіврозпаду 4,5 х 10 9 років, використовуються для визначення віку стародавніх об'єктів. Наприклад, вік зразків порід з Місяця, як показано на рис. 8.3.5, визначали за допомогою радіоізотопного датування урану-238.

