7.5: Іони перехідних металів
Що це за монета?
Більшість з нас знайомі з звичайними монетами: копійки, нікелю, копійки, чверті. У деяких районах (наприклад, Лас-Вегасі) ви можете побачити великі суми срібних доларів (вони стають трохи важкими у вашій кишені). Але більшість з нас, мабуть, ніколи не бачили платинового орла - монету із зображенням орла, яка утримується в першу чергу колекціонерами. Якщо ви повинні були взяти одну унцію платиновий орел в магазин, щоб купити сто доларів на суму предметів, власник магазину, швидше за все, не повірить вам, коли ви стверджуєте, що монета коштує сто доларів. Це також було б незручно і дратує, якщо ви втратили одну з цих монет з кишені. Платина - це лише один з декількох перехідних металів, який коштує чималих грошей (золото - це ще один).
Елементи групи 1 і 2 утворюють катіони за допомогою простого процесу, який передбачає втрату однієї або декількох електронів зовнішньої оболонки. Ці електрони надходять зs орбіти і видаляються дуже легко.
Іони перехідних металів
Більшість перехідних металів відрізняються від металів груп 1, 2 і 13 тим, що вони здатні утворювати не один катіон з різними іонними зарядами. Як приклад, залізо зазвичай утворює два різних іона. Іноді він може втрачати два електрони, щоб утворитиFe2+ іон, тоді як в інший час він втрачає три електрони для утворенняFe3+ іона. Олово і свинець, хоч іp входять в блок, а не dблок, також здатні утворювати множинні іони.
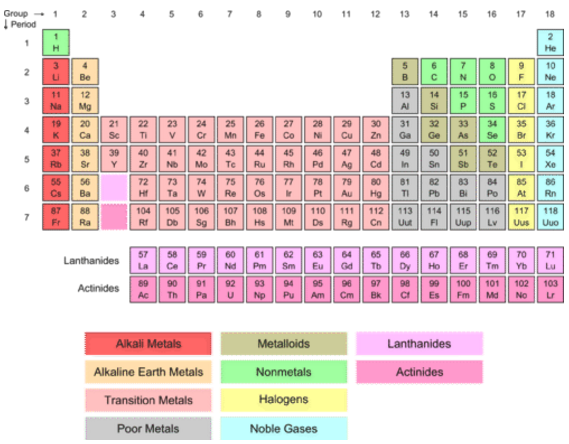
Іонне утворення для перехідних металів ускладнюється тим, що ці елементи мають незаповнені внутрішніd оболонки. Хоча наступні вищіs орбіталі насправді знаходяться на нижчому енергетичному рівні, ніжd рівень, ціs електрони є тими, які видаляються під час іонізації.
У таблиці нижче наведені назви і формули деяких поширених іонів перехідних металів:
| Таблиця7.5.1: Загальні іони перехідних металів | |||
|---|---|---|---|
| \ (\ pageIndex {1}\): Загальні іони перехідних металів"> 1+ | 2+ | 3+ | 4+ |
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="вертикальне вирівнювання: middle; ">мідь (I),Cu+ | кадмій,Cd2+ | хром (III),Cr3+ | свинець (IV),Pb4+ |
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="вертикальне вирівнювання: середина; ">золото (I),Au+ | хром (II),Cr2+ | кобальт (III),Co3+ | олово (IV),Sn4+ |
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="вертикальне вирівнювання: middle; ">ртуть (I),Hg2+2 | кобальт (II),Co2+ | золото (III),Au3+ | |
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="вертикальне вирівнювання: середина; "> срібло,Ag+ | мідь (II),Cu2+ | залізо (III),Fe3+ | |
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | залізо (II),Fe2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | свинець (II),Pb2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | марганець (II),Mn2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | ртуть (II),Hg2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | нікель (II),Ni2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | платина (II),Pt2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | олово (II),Sn2+ | ||
| \ (\ pageIndex {1}\): Загальні іони перехідних металів» style="vertical-align:middle; "> | цинк,Zn2+ | ||
Використання для перехідних металів
Оскільки в цій групі так багато металів, існує широкий спектр застосувань. Багато металів використовуються в електроніці, а інші (наприклад, золото і срібло) використовуються в грошових системах. Залізо - універсальний конструкційний матеріал. Кобальт, нікель, платина та інші метали використовуються як каталізатори в ряді хімічних реакцій. Цинк є значущим компонентом акумуляторів.
Резюме
- Перехідні метали мають незаповнені внутрішніd електронні оболонки.
- Іони утворюються насамперед через втратуs електронів.
- Багато перехідні метали можуть утворювати більше одного іона.
- Перехідні метали мають найрізноманітніші області застосування.
Рецензія
- Чим унікальні електронні конфігурації перехідних металів?
- Які електрони елементів перехідних металів найімовірніше втрачаються при утворенні іонів?
- Скільки іонів може утворюватися залізо?
- Який перехідний метал утворює тільки один іон?
- Перерахуйте кілька застосувань для перехідних металів.
