5.18: Конфігурації електронів
- Page ID
- 19413
Наскільки великий файл?
Якщо ви зберігаєте свої папери в папках маніли, ви можете підібрати папку і подивитися, скільки вона важить. Якщо ви хочете знати, скільки різних паперів (статей, банківських записів або що-небудь ще ви зберігаєте в папці), вам доведеться все вийняти і порахувати. Комп'ютерний каталог, з іншого боку, говорить вам точно, скільки у вас є в кожному файлі. Ми можемо отримати таку ж інформацію про атоми. Якщо ми використовуємо діаграму орбітального заповнення, нам доведеться рахувати стрілки. Коли ми дивимося на дані електронної конфігурації, ми просто складаємо числа.
Конфігурації електронів
Позначення електронної конфігурації виключає коробки і стрілки діаграм орбітального заповнення. Кожне позначення зайнятого підрівня пишеться за ним верхній індекс, який є кількістю електронів у цьому підрівні. Наприклад, воднева конфігурація є\(1s^1\), тоді як конфігурація гелію є\(1s^2\). Кілька зайнятих підрівнів записуються один за одним. Електронна конфігурація літію є\(1s^2 2s^1\). Сума надскриптів в електронній конфігурації дорівнює кількості електронів в тому атомі, яке, в свою чергу, дорівнює його атомному номеру.
Приклад\(\PageIndex{1}\)
Намалюйте орбітальну діаграму заповнення вуглецю та напишіть його електронну конфігурацію.
Рішення
Крок 1: Перерахуйте відомі величини та плануйте проблему.
Відомий
- атомний номер вуглецю, Z = 6
Використовуйте діаграму порядку заповнення, щоб намалювати діаграму орбітального заповнення із загальною кількістю шести електронів. Дотримуйтесь правила Гунда. Запишіть електронну конфігурацію.
Крок 2: Побудувати діаграму.
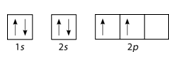
Конфігурація електронів\(1s^2 2s^2 2p^2\)
Крок 3: Подумайте про свій результат.
Слідом за\(2s\) підрівнем йде\(2p\), а\(p\) підрівні завжди складаються з трьох орбіталей. Всі три орбіталі потрібно намалювати, навіть якщо одна або кілька незайняті. Згідно з правилом Гунда, шостий електрон потрапляє на другу з цих\(p\) орбіталей, з таким же спіном, як і п'ятий електрон.
Елементи другого періоду
Періоди відносяться до горизонтальних рядків таблиці Менделєєва. Перший період таблиці Менделєєва містить тільки елементи водень і гелій. Це пояснюється тим, що перший основний енергетичний рівень складається тільки з\(s\) підрівня, і тому для заповнення всього основного енергетичного рівня потрібні лише два електрони. Кожен раз, коли починається новий основний енергетичний рівень, як і у третього елемента літію, в таблиці Менделєєва запускається новий період. Коли один рухається через другий період, електрони послідовно додаються. З\(\left( Z=4 \right)\) берилієм\(2s\) підрівень завершений і\(2p\) підрівень починається з бору\(\left( Z=5 \right)\). Так як є три\(2p\) орбіталі і кожна орбіталь утримує два електрона, то\(2p\) підрівень заповнюється після шести елементів. Таблиця\(\PageIndex{1}\) показує електронні конфігурації елементів у другому періоді.
| Назва елемента | Символ | Атомний номер | Конфігурація електрона |
|---|---|---|---|
| Літієві | \(\ce{Li}\) | 3 | \(1s^2 2s^1\) |
| Берилій | \(\ce{Be}\) | 4 | \(1s^2 2s^2\) |
| Бор | \(\ce{B}\) | 5 | \(1s^2 2s^2 2p^1\) |
| Вуглець | \(\ce{C}\) | 6 | \(1s^2 2s^2 2p^2\) |
| Азот | \(\ce{N}\) | 7 | \(1s^2 2s^2 2p^3\) |
| Кисень | \(\ce{O}\) | 8 | \(1s^2 2s^2 2p^4\) |
| Фтор | \(\ce{F}\) | 9 | \(1s^2 2s^2 2p^5\) |
| Неонові | \(\ce{Ne}\) | 10 | \(1s^2 2s^2 2p^6\) |
Резюме
- Позначення електронної конфігурації спрощує вказівку того, де електрони знаходяться в конкретному атомі.
- Надскрипти використовуються для позначення кількості електронів в даному підрівні.
Рецензія
- Що усуває позначення електронної конфігурації?
- Як ми знаємо, скільки електронів в кожному підрівні?
- Атом має електронну конфігурацію\(1s^2 2s^2 2p^5\). Скільки електронів в цьому атомі?
- Який елемент має електронну конфігурацію\(1s^2 2s^2 2p^6 3s^2\)?