5.11: Квантова механічна атомна модель
- Page ID
- 19401
Уявіть, що спалах новин перериває вашу улюблену телепрограму... «У Першому Національному банку відбулася затримка. Підозрюваний втік в машині і, як вважають, знаходиться десь в центрі міста. Всіх просять бути напоготові». Розбійник може перебувати тільки в межах певної області - у поліції немає точного місцезнаходження, просто загальне уявлення про місцезнаходження злодія.
Квантова механічна атомна модель
У 1926 році австрійський фізик Ервін Шредінгер (1887-1961) використовував хвильово-частинкову подвійність електрона для розробки і вирішення складного математичного рівняння, яке точно описувало поведінку електрона в атомі водню. Квантова механічна модель атома походить від розв'язку рівняння Шредінгера. Квантування енергій електронів є вимогою для вирішення рівняння. Це на відміну від моделі Бора, в якій квантування просто припускалося без математичної основи.
Нагадаємо, що в моделі Бора точний шлях електрона був обмежений дуже чітко визначеними круговими орбітами навколо ядра. Квантова механічна модель є радикальним відходом від цього. Розв'язки хвильового рівняння Шредінгера, званого хвильовими функціями, дають лише ймовірність знаходження електрона в заданій точці навколо ядра. Електрони не рухаються навколо ядра по простих кругових орбітах.
Розташування електронів в квантово-механічній моделі атома часто називають електронною хмарою. Електронну хмару можна придумати таким чином: Уявіть, що на підлозі розміщуєте квадратний аркуш паперу з крапкою в колі, що представляє ядро. Тепер візьміть маркер і неодноразово опустіть його на папір, роблячи невеликі позначки в кожній точці, на яку потрапляє маркер. Якщо ви скинете маркер багато-багато разів, загальний візерунок точок буде приблизно круглим. Якщо ви прагнете до центру досить добре, біля ядра буде більше точок і поступово менше точок, коли ви віддаляєтеся від нього. Кожна точка являє собою місце, де електрон може знаходитися в будь-який момент. Через принцип невизначеності немає можливості точно знати, де знаходиться електрон. Електронна хмара має змінну щільність: високу щільність, де найімовірніше буде електрон, і низьку щільність, де електрон найменш імовірний (див. Нижче).
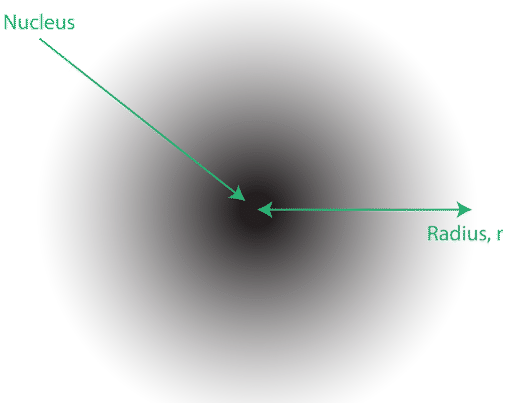
Для того щоб конкретно визначити форму хмари, прийнято відносити область, в межах якої є\(90%\) ймовірність знаходження електрона. Це називається орбітальною, тривимірною областю простору, яка вказує, де є висока ймовірність знаходження електрона.
Резюме
- Хвильове рівняння Шредінгера замінило уявлення Бора про розташування електронів на коефіцієнт невизначеності.
- Розташування електрона можна задати тільки як ймовірність того, що електрон знаходиться десь в певній області.
Рецензія
- Що вимагає квантово-механічний погляд атома?
- Що таке хвильова функція?
- Що говорить електронна хмара високої щільності?