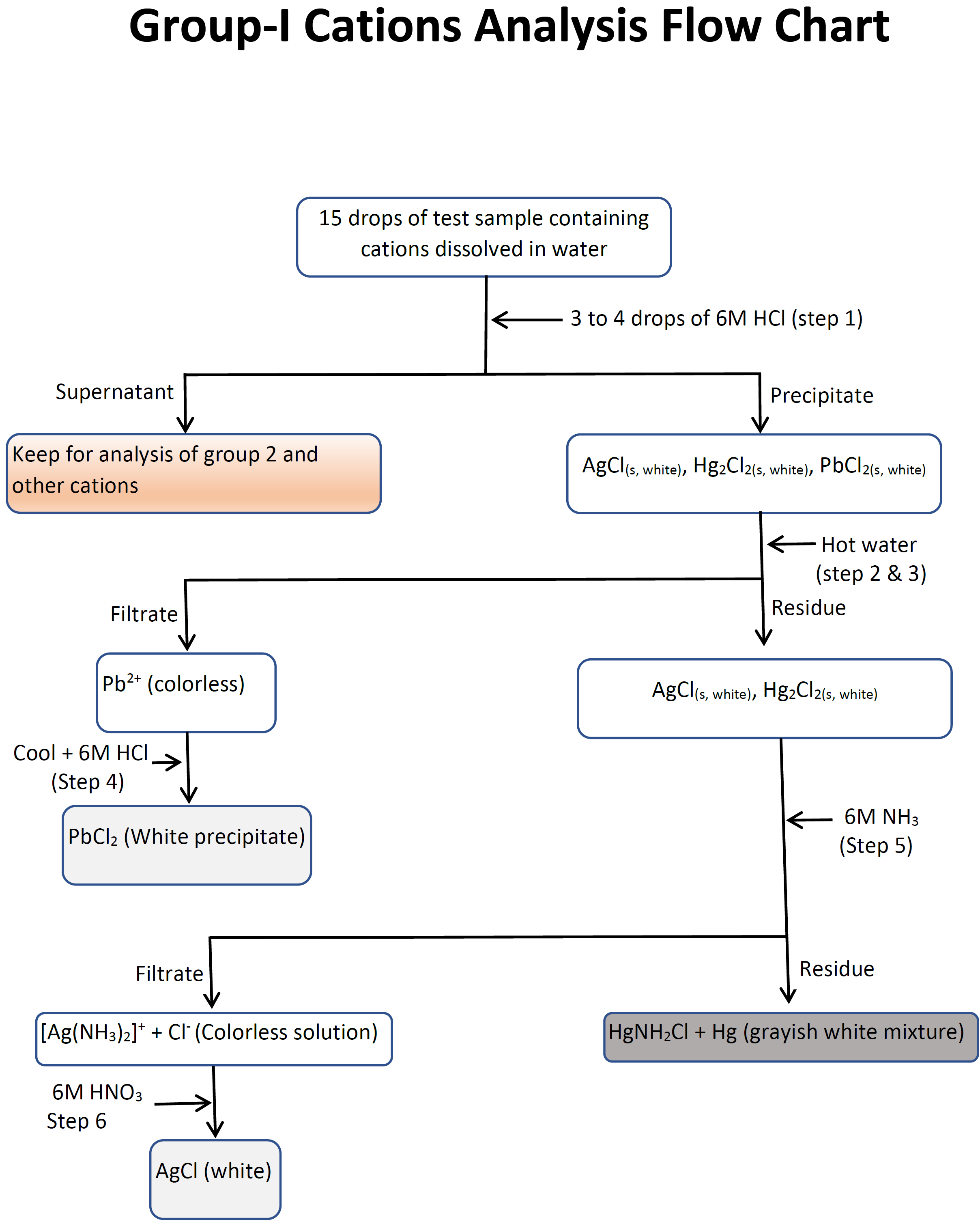
3.3: Процедура, блок-схема та таблиці даних для поділу та підтвердження катіонів групи I
- Page ID
- 25099
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \) \( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)\(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\) \(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\)
|
Хімічна |
небезпека |
|---|---|
|
0.1M нітрату свинцю (II) в 0,1 М азотної кислоти |
Токсичний, подразнюючий і окислювач |
|
0.1M Ртуть (I) нітрат в 0,1 М азотної кислоти |
Високотоксичний і окислювач |
|
0,1 М нітрату срібла в 0,1 М азотної кислоти |
Токсичні, корозійні та окислювачі |
- * Небезпеки 6M аміаку, 6M соляної кислоти та 6M азотної кислоти перераховані в загальній таблиці реагентів у розділі 2.
- Використовувані іонні розчини важких металів або опади утилізуються в маркованому контейнері для утилізації металевих відходів, не зливайте ці розчини в каналізацію або в звичайне сміття.
- Візьміть 15 крапель невідомого розчину в пробірці і додайте в нього 3 - 4 краплі 6М\(\ce{HCl}\) по краплях при помішуванні. Центрифуга протягом 2 хв і без зціджування додати ще 1 краплю 6М,\(\ce{HCl}\) щоб перевірити, чи немає більше утворення опадів. Якщо утворюється більше осаду, центрифугують і перевіряють ще раз, поки більше не утворюється осад при додаванні краплі 6М\(\ce{HCl}\) до супернатанту. Ретельно зціджують і зберігають супернатант для аналізу катіонів групи 2, а осад використовують на наступному етапі для поділу і конформації катіона групи 1\(\ce{AgCl(s, white)}\)\(\ce{Hg2Cl2(s, white)}\), т. Е\(\ce{PbCl2(s, white)}\). Запишіть спостереження в таблицю даних.
- Додайте 2 мл (40 крапель) дистильованої води в осад з кроку 1 в пробірці, розмішайте чистим скляним стрижнем, щоб повторно підвісити осад, і нагрійте пробірку на киплячій водяній бані протягом 3 хв при перемішуванні. Додайте 15 мл дистильованої води у 2-у пробірку і нагрійте її також на киплячій водяній бані.
- Підготуйте установку гравітаційної фільтрації та пропустіть ~ 5 мл гарячої води з 2-ї пробірки кроку 2, щоб зробити її нагрітою установкою гравітаційної фільтрації. Відмовтеся від фільтрату, який є просто гарячою водою. Помістіть порожню пробірку з написом «Свинець (II) підтвердження тесту» під нагріту воронку фільтра, відфільтруйте вміст першої пробірки кроку 2 і зберіть її і зберігайте фільтрат для\(\ce{Pb^{2+}}\) тесту в пробірці з маркуванням «Свинець (II) тест підтвердження». Зберігають залишки, якщо такі є, для\(\ce{Ag^{+}}\) і\(\ce{Hg2^{2+}}\) тестів. Якщо осаду не залишилося, значить\(\ce{Ag^{+}}\) і\(\ce{Hg2^{2+}}\) іони були відсутні в досліджуваному зразку.
- Дайте 2 мл фільтрату в пробірці з міткою «Свинець (II) підтвердження тесту», охолонути до кімнатної температури, помістивши пробірку на водяну баню кімнатної температури. Якщо білі кристали/осад утворюються, то фільтрат при охолодженні\(\ce{Pb^{2+}}\) присутній в досліджуваному зразку. Якщо при охолодженні не утворюється кристал, додайте від 2 до 3 крапель 6М\(\ce{HCl}\) до фільтрату при перемішуванні скляним стрижнем. Якщо в тестовому зразку\(\ce{Pb^{2+}}\) були присутні білі кристали/форми осаду. Якщо відсутні білі кристали/осад, то на цьому етапі в досліджуваному зразку не\(\ce{Pb^{2+}}\) спостерігалося. Відкиньте суміш в металеву ємність для сміття. Запишіть спостереження в даташит.
- Повторно призупиніть залишок, якщо такий є, з кроку 3 в ~ 5 мл гарячої води з 2-ї пробірки кроку 2, щоб розчинити залишки,\(\ce{PbCl2}\) а потім відфільтрувати його. Змийте залишки залишком ~ 5 мл гарячої води з 2-ї пробірки кроку 2. Відкиньте фільтрат, який є просто промивної рідиною з домішками в ньому, і залиште осад на фільтрувальному папері. Покладіть чисту порожню пробірку під фільтраційну воронку і додайте 40 крапель (2 мл) 6М\(\ce{NH3}\) на залишок крапелькою при загальному перемішуванні скляним стрижнем. Зберігайте фільтрат для\(\ce{Ag^{+}}\) тесту. Якщо залишок все ще залишився на фільтрувальному папері і змінює колір з білого на сірувато-чорний\(\ce{Hg2^{2+}}\) був присутній в досліджуваному зразку, в іншому випадку,\(\ce{Hg2^{2+}}\) був відсутній в досліджуваному зразку. Відкиньте сірий залишок в контейнері для металевих відходів. Запишіть спостереження на таблицю даних.
- Додайте 6M\(\ce{HNO3}\) краплю за краплею до 2 мл фільтрату з кроку 5, перемішуючи і продовжуйте тестування з синім лакмусовим папером, поки розчин не перетвориться з лужного на кислотний, вказаний зміною кольору лакмусового паперу з синього на червоний. Якщо на цьому етапі спостерігається біла суспензія/осад, це підтверджує, що\(\ce{Ag^{+}}\) була присутня в досліджуваному зразку, інакше в досліджуваному зразку не\(\ce{Ag^{+}}\) було. Відкиньте суміш в контейнер для металевих відходів. Запишіть спостереження в таблицю даних.
- Номер кроку відноситься до відповідного номера кроку в підрозділі процедури.
- У стовпці «очікувана хімічна реакція та очікувані спостереження» напишіть загальне чисте іонне рівняння реакції, яке відбудеться, якщо іон, що обробляється на етапі, напишіть очікувану зміну кольору розчину, очікуваний осад і його очікуваний колір тощо.
- У стовпці «фактичні спостереження та висновок» напишіть зміну кольору, утворений осад та його колір тощо, що насправді спостерігається як доказ, і вкажіть конкретний іон як присутній або відсутній.
- У рядку «загальний висновок» напишіть один за іншим символ іонів, що перевіряються, із твердженням «присутній» або «відсутній», а потім доказами/с, щоб підтвердити ваш висновок.