6.4: Реальні гази
Насправді жоден газ не поводиться ідеально. Тому ідеальна EOS не корисна для практичного застосування, хоча вона важлива як основа нашого розуміння поведінки газу. Незважаючи на те, що ідеальна модель не є надійною для реальних інженерних застосувань, ми повинні мати на увазі, що ідеальний газ EOS є відправною точкою всіх сучасних підходів.
Якщо ми озирнемося назад на рис. 6.3.2 і згадаємо наші дискусії про p-v поведінку чистих речовин, щось повинно привернути вашу увагу. Рисунок 6.4.3 показує нам типову поведінку p-v чистої речовини для полегшення нашого обговорення.
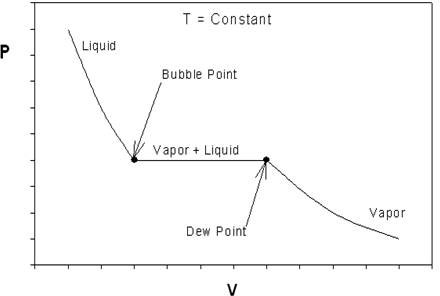
Що можна зробити висновок про ідеальну EOS при контрастуванні малюнка 6.3.2 до 6.4.3? Крива на малюнку 6.3.2 суцільна; рис. 6.4.3 має явний розрив (при переході пар+рідина). Отже, одне, що ми вже можемо сказати, це те, що ідеальна EOS принаймні якісно неправильна. Для реальної речовини, коли тиск збільшується, повинна бути точка розриву, яка представляє зміну фази. Ідеальний газ не буде конденсуватися, незалежно від того, якого тиску він піддається, незалежно від температури системи. Іншими словами, ми не можемо сподіватися відтворити поведінку p-v на малюнку 6.4.3, використовуючи ідеальне рівняння (6.3.3), оскільки розриву не знайдено. Однак реальну ізотерму p-v можна наблизити ідеальною поведінкою при низьких тисках, як ми бачимо з графіків.
Ми також можемо встановити деякі кількісні відмінності між ідеальною та реальною поведінкою PVT. Наприклад, для більшості умов, що цікавлять при заданому обсязі і температурі, ідеальна газова модель перепрогнозує тиск системи:
PIdealGas>PRealGas
Ми можемо пояснити цю різницю, нагадавши, що справжній газ дійсно має сили взаємодії між молекулами. По-друге, нагадаємо, що поняття «тиск» газу є наслідком кількості молекулярних зіткнень на одиницю площі об стінку ємності. Така кількість зіткнень є, в свою чергу, мірою свободи молекул подорожувати всередині газу. Ідеальний газ - це стан повної молекулярної свободи, де молекули навіть не знають про існування інших. Отже, гіпотетичний ідеальний газ буде чинити більш високий тиск, ніж реальний газ при будь-якому заданому обсязі та температурі. Коли молекули збираються разом (справжній газ), це зменшує наявний вільний простір для молекул і тиск знижується.
Крім того, ідеальна модель передбачає, що фізичний простір, який займають самі молекули, мізерно малий. Насправді молекули є фізичними частинками, і вони займають простір. Як тільки ми знайдемо спосіб обліку простору, який займають самі молекули, ми зможемо обчислити «реальний» вільний об'єм, доступний для переміщення молекул через газ. В ідеальному випадку цей вільний об'єм дорівнює об'єму самої ємності, оскільки молекулярний обсяг не враховується. У реальному випадку цей вільний об'єм повинен бути меншим за обсяг самого контейнера після того, як ми враховуємо фізичний простір, який займають молекули. Тому:
Vreal,free<VIdeal=VContainer
Vreal,free<VContainer=Voccupiedbymolecules
