9.7: Проблеми
- Page ID
- 29336
9.1. Розчин об'ємом 50 л містить\(^+\) іони\(8 \cdot 10^{19}\) Н. Обчисліть рН. Це розчин кислий або основний?
9.2. Флакон містить 3 літри хімічного розчину з рН 8.
(а) Чи містить пляшка кислоту або основу?
(б) Приблизно скільки\(^+\) іонів Н знаходиться в пляшці?
(c) Чи буде 3-літрова пляшка з рН 9 містити більше або менше іонів Н,\(^+\) ніж пляшка з рН 8?
(d) Скільки разів більше/кілька\(^+\) іонів Н знаходяться у пляшці з розчином pH 8, ніж у пляшці з розчином рН 9?
9.3. Розглянемо акумулятор з літієвим електродом і електродом з хлориду срібла (AgCl). Припустимо, що в акумуляторі відбуваються наступні хімічні реакції, і показано окислювально-відновний потенціал для кожної реакції.
\(\text{AgCl} + e^- \rightarrow \text{Ag} + \text{Cl}^-\)\(V_{rp} = 0.22 V\)
\(\text{Li} \rightarrow \text{Li}^+ + e^-\)\(V_{rp} = 3.04 V\)
(а) Яка реакція, ймовірно, відбудеться на катоді, і яка реакція, ймовірно, відбудеться на аноді? Обґрунтуйте свою відповідь.
(b) Яка загальна теоретична напруга комірки?
(c) Якщо акумулятор підключений до\(1 k\Omega\) навантаження, приблизно яка потужність подається на це навантаження?
9.4. Припустимо, хімічні реакції та відповідні окислювально-відновні потенціали в акумуляторі задаються [137]:
\(\text{Li} \rightarrow \text{Li}^+ + e^-\)\(V_{rp} = 3.04 V\)
\(\text{S} + 2e^- \rightarrow \text{S}^{2-}\)\(V_{rp} = -0.57 V\)
(а) Знайдіть загальну теоретичну питому ємність акумулятора в\(\frac{C}{g}\).
(b) Знайдіть загальну теоретичну питому енергію акумулятора в\(\frac{J}{g}\).
(c) Який матеріал, літій або сірка, окислюється, а який матеріал зменшується?
9.5. Акумулятор має питому ємність 252\(\frac{C}{g}\) і масу 50 м Його загальна щільність становить 2,245\(\frac{g}{m^3}\).
(а) Знайти конкретну ємність в\(\frac{mA \cdot h}{g}\).
(б) Знайти ємність в\(mA \cdot h\).
(c) Знайти щільність заряду в\(\frac{mA \cdot h}{m^3}\).
9.6. Акумулятор має питому ємність 55\(\frac{mA \cdot h}{g}\) і номінальну напругу 2,4 В., Акумулятор має масу 165 м Знаходимо енергію, що зберігається в акумуляторі, в Дж.
9.7. Батарея має сірчаний катод, де\(\text{S} + 2e^- \rightarrow \text{S}^{2-}\) відбувається реакція. Анод зроблений з таємничого матеріалу\(X\), а на аноді\(X \rightarrow X^{2+} + 2e^-\) відбувається реакція. Теоретична питома ємність реакції сірки становить 1,76,\(\frac{A \cdot h}{g}\) а теоретична питома ємність матеріалу Х - 0,819\(\frac{A \cdot h}{g}\). Теоретична питома ємність комбінованих матеріалів становить 0,559\(\frac{A \cdot h}{g}\). Що таке матеріал\(X\), і що таке\(V_{rp}\), окислювально-відновний потенціал акумулятора? (Підказка: Використовуйте періодичну таблицю та список окислювально-відновних потенціалів.)
9.8. У чому різниця між кожним з пунктів у парах нижче?
- Акумулятор і паливний елемент
- Первинний акумулятор і вторинний акумулятор
- Окислювально-відновний потенціал і хімічний потенціал
9.9. Розглянемо полімерну електролітну мембрану паливного елемента, показану нижче. Реакції на електродах бувають:
\(\text{H}_2 \rightarrow 2\text{H}^+ + 2e^-\)
\(4e^- + 4\text{H}^+ + \text{O}_2 \rightarrow 2\text{H}_2\text{O}\)
Зіставте мітку на зображенні з назвою компонента.
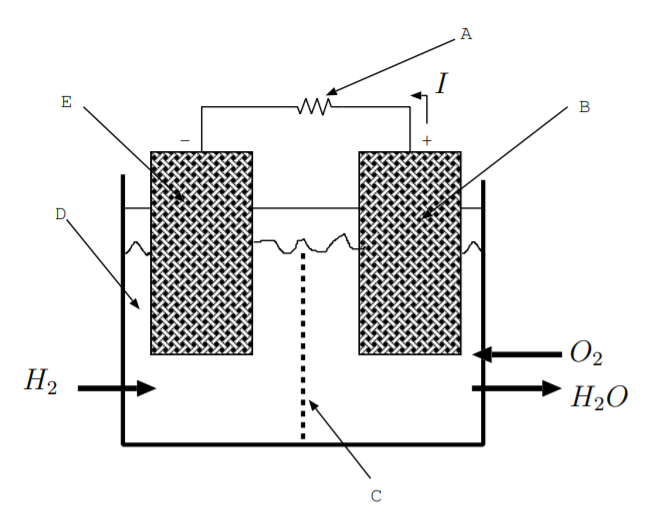
| Назва компонента | Етикетка |
|---|---|
| 1. Анод | |
| 2. Катод | |
| 3. Електроліт | |
| 4. Навантаження | |
| 5. Полімерна електролітна мембрана |
9.10. Зіставте назву компонентів паливного елемента з матеріалом, який використовується для виготовлення цього компонента.
| Назва компонента паливного елемента | Матеріал |
|---|---|
| 1. Анод | A. Платина |
| 2. Побічний продукт (відходи виробництва) | B. вуглець (твердий, але пористий) |
| 3. Каталізатор | C. Вода |
| 4. Електроліт | D. сірчана кислота |
| 5. Паливо | E. Рідкий водень |
